-
在一定体积的密闭容器中,进行如下化学反应:2X(g)+Y(s)
 Z(g)+W(g),若其化学平衡常数K和温度t的关系如下表
Z(g)+W(g),若其化学平衡常数K和温度t的关系如下表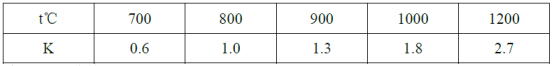
下列叙述不正确的是( )
A.上述反应的正反应是吸热反应
B.该反应的化学平衡常数表达式为K=
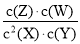
C.若在1L的密闭容器中通入X和Y各1mol,5min后温度升高到800℃,此时测得X为0.33mol,该反应达到平衡状态
D.混合气体的密度保持不变可作为该反应达到平衡的标志之一
高二化学单选题困难题查看答案及解析
-
常温下,浓度均为0.10 mol/L、体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随
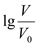 的变化如图所示,下列叙述正确的是( )
的变化如图所示,下列叙述正确的是( )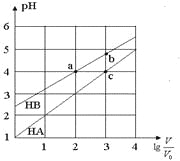
A.该温度下HB的电离平衡常数约等于1.11×10-5
B.当
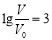 时,若两溶液同时升高温度,则
时,若两溶液同时升高温度,则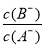 减小
减小C.相同条件下NaA溶液的pH大于NaB溶液的pH
D.溶液中水的电离程度:a=c>b
高二化学单选题困难题查看答案及解析
-
为探究外界条件对反应:mA(g) +nB(g)
 cZ(g) △H的影响,以A和B物质的量之比为 m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是( )
cZ(g) △H的影响,以A和B物质的量之比为 m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是( )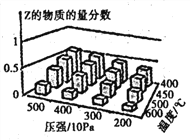
A.在恒温恒容条件下,向已达到平衡的体系中加入少量Z,平衡正向移动,Z的含量增大
B.升高温度,正、逆反应速率都增大,平衡常数增大
C.△H<0 m + n >c
D.△H>0 m +n<c
高二化学单选题困难题查看答案及解析
-
常温下,向10 mL 0.2mol•L-1 的MOH中逐滴加入0.2 mol•L-1的CH3COOH溶液,溶液的导电能力如图1所示,溶液的pH 变化如图2所示(已知:常温时,NH3∙H2O和CH3COOH的电离常数均为1.8×10-5), 下列说法正确的是
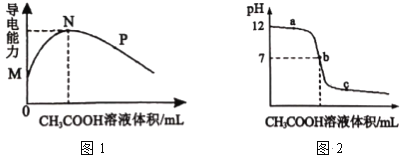
A.图l中N点时,加入CH3COOH溶液的体积为l 0 mL
B.MOH是一种弱碱,相同条件下其碱性弱于 NH3•H2O 的碱性
C.图2中b点时,加入CH3COOH溶液的体积为l 0 mL
D.若c点对应醋酸的体积是15 mL,则此时溶液中:c(CH3COOH) + c(CH3COO-) < 0.1 mol•L-1
高二化学单选题困难题查看答案及解析
-
短周期主族元素 X、Y、Z、M、R 的原子半径和最外层电子数之间的关系如图所示。
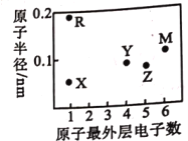
下列说法正确的是
A.化合物 RX 中含有共价键
B.Y、Z、M 的氧化物均能溶于水
C.化合物R2M 是弱电解质,其水溶液显碱性
D.试管壁上残留的M 单质可以用热的NaOH溶液除去
高二化学单选题困难题查看答案及解析
-
下列解释事实的方程式正确的是
A.用稀硫酸除去硫酸钠溶液中少量的硫代硫酸钠:Na2S2O3+2H++ SO2↑+S↓+2Na+ + H2O
B.氢氧化亚铁暴露于空气中会变色:4Fe(OH)2 + O2 + 2H2O= 4Fe(OH)3
C.将少量的 SO2气体通入NaClO溶液中:SO2 +H2O+ 2ClO- = SO
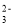 + 2HC1O
+ 2HC1OD.草酸使酸性KMnO4溶液褪色: 2MnO
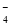 + 16H++ 5 C2O
+ 16H++ 5 C2O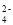 = 2Mn2+ + 10CO2↑+ 8H2O
= 2Mn2+ + 10CO2↑+ 8H2O高二化学单选题困难题查看答案及解析
-
下列化学反应的能量变化符合如图所示关系的是

A.CaCO3
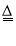 CaO + CO2↑
CaO + CO2↑B.2CH3CH2OH + O2
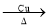 2CH3CHO+ 2H2O
2CH3CHO+ 2H2OC.2NH4Cl+ Ba(OH)2 = BaCl2+ 2NH3• H2O
D.2Na+2H2O =2NaOH + H2↑
高二化学单选题困难题查看答案及解析
-
下列图中的实验方案,能达到实验目的的是:( )
A
B
C
D
实验方案
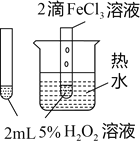
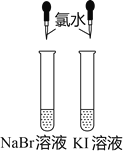
实验目的
验证FeCl3对H2O2分解反应有催化作用
验证单质氧化性:
Cl2>Br2>I2
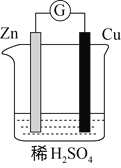
证实Zn与稀硫酸反应可以将化学能转化为电能
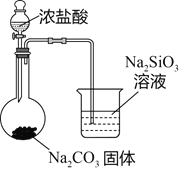
比较HCl、H2CO3和H2SiO3的酸性强弱
A. A B. B C. C D. D
高二化学单选题困难题查看答案及解析
-
GaAs晶体的熔点很高, 硬度很大, 密度为ρ g·cm-3,Ga 和As 的摩尔质量分别为MGag·mol-1和MAs g·mol-1, 原子半径分别为rGa pm 和rAs pm, 阿伏加德罗常数值为NA, 其晶胞结构如下图所示, 下列说法错误的是
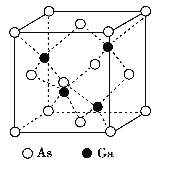
A. 该晶体为原子晶体
B. 在该晶体中,Ga和As均无孤对电子,Ga和As的配位数均为4
C. 原子的体积占晶胞体积的百分率为
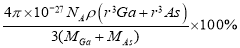
D. 所有原子均满足8电子稳定结构
高二化学单选题困难题查看答案及解析
-
分子式为C9H18O2的有机物A有下列变化关系

其中B、C的相对分子质量相等,则A的可能结构有
A.9种 B.8种 C.7种 D.6种
高二化学单选题困难题查看答案及解析