-
化合物A[KxFe(C2O4)y·zH2O,其中铁元素为+3价]是一种重要的光化学试剂。
(1)制备化合物A的实验流程如下:
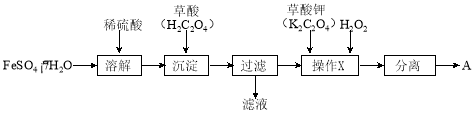
① 上述流程中,检验“过滤”后的固体已洗涤干净的方法是 。
② 上述流程“操作X”中加入H2O2的目的是
。
(2)测定化合物A的化学式实验步骤如下:
a、准确称取A样品4.91g,干燥脱水至恒重,残留物质的质量为4.37g;
b、将步骤a所得固体溶于水,加入还原铁粉0.28g,恰好完全反应;
c、另取A样品4.91g置于锥形瓶中,加入足量的3 mol/L的H2SO4溶液和适量蒸馏水,再加入0.50mol/L的KMnO4溶液24.0 mL,微热,恰好完全反应:
2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
通过计算填空,请写出解题过程。
① 4.91g A样品中含结晶水的物质的量为 mol。
② A样品中
= 。
③ A的化学式为 。
高二化学填空题极难题查看答案及解析
-
NaHSO4和NaHCO3是常见的酸式盐,是水溶液中离子平衡部分重要的研究对象。请运用相关原理,回答下列有关小题。
(1)NaHSO4在水中的电离方程式为 。室温下,pH=5的NaHSO4溶液中水的电离程度 (填“>”、”=”或“<”)pH=9的氨水中水的电离程度。
(2)等体积等物质的
量浓度的NaHSO4与氨水混合后,溶液呈酸性的原因为 (用离子方程式表示)。
(3)室温下,若一定量的NaHSO4溶液与氨水混合后,溶液pH=7,则c(Na+)+c(NH
) c(SO
)(填“>”、“=”或“<”)。
(4)室温下,用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO
完全沉淀,则反应后溶液的pH__________7(填“>”、”=”或“<”)。
(5)室温下,0.1 mol/L 的NaHCO3溶液的pH为8.4,同浓度的NaAlO2溶液的pH为12.4,同浓度的Na2CO3溶液的pH是11.4。
①将NaHCO3溶液和NaAlO2溶液等体积混合,可能发生的现象是 ,其主要原因是 (用离子方程式表示)。
②上述溶液中,由NaHCO3水解产生的c(OH-)是由 Na2CO3水解产生c(OH-)的 倍。
高二化学填空题极难题查看答案及解析
-
(9分)某种碳酸锰矿的主要成分有MnCO3、MnO2、FeCO3、MgO、SiO2、Al2O3等。已知碳酸锰难溶于水。一种运用阴离子膜电解法的新技术可用于从碳酸锰矿中提取金属锰,流程如下:
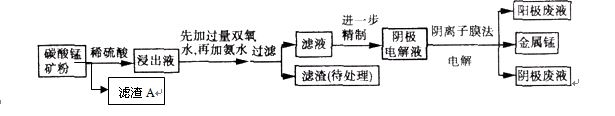
阴离子膜法电解装置如下图所示:
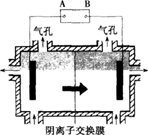
(1)写出用稀硫酸溶解碳酸锰反应的离子方程式:。
(2)已知Ksp (Fe(OH)3) = 4 ´10–38,假设溶液中Fe3+离子浓度为0.1 mol·L–1,则开始生成Fe(OH)3 沉淀的pH是_________,沉淀完全的pH是_________。(可能用到的数据:lg
= -0.1 lg
=0.2)
(3)已知不同金属离子生成氢氧化物沉淀所需的pH如下表:
离子
Fe3+
A13+
Fe2+
Mn2+
Mg2+
开始沉淀的pH
1.2
3.7
7.0
7.8
9.3
沉淀完全的pH
3.7
4.7
9.6
9.8
10.8
加氨水调节溶液的pH等于6,则“滤渣(待处理)”的成分是________ (写化学式),滤液中含有的阳离子有H+和________(写符号)。
(4)在浸出液里锰元素只以Mn2+的形式存在,且滤渣A中也无MnO2,请用离子方程式解释原因:________。
(5)电解装置中箭头表示溶液中阴离子移动的方向,则A电极是直流电源的________极。实际生产中,阳极以稀硫酸为电解液,阳极的电极反应式为________。
(6)该工艺之所以采用阴离子交换膜,是为了防止Mn2+进入阳极区发生副反应生成MnO2造成资源浪费,写出该副反应的电极反应式:________。
高二化学填空题极难题查看答案及解析
-
(10分)工业上合成氨的反应:N2(g)+3H2(g)
2NH3(g)ΔH=-92.60 kJ·mol-1。
(1)在绝热、容积固定的密闭容器中发生反应:N2(g)+3H2(g)
2NH3(g),下列说法能说明上述反应向正反应方向进行的是____________________(填序号)。
①单位时间内生成2n mol NH3的同时生成3n mol H2
②单位时间内生成6n mol N—H键的同时生成2n mol H—H键
③用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1∶3∶2
④混合气体的平均摩尔质量增大
⑤容器内的气体密度不变
(2)已知合成氨反应在某温度下2 L的密闭容器中进行,测得如下数据:
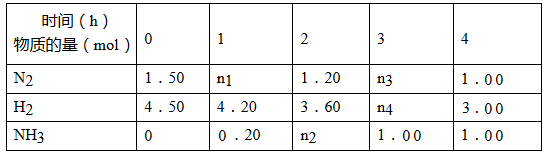
根据表中数据计算:
①反应进行到2 h时放出的热量为_________________kJ。
②此温度下该反应的化学平衡常数K=_________________(保留两位小数)。
③反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00 mol,化学平衡将向________________方向移动(填“正反应”或“逆反应”或“不移动”)。
④有甲、乙两个完全相同的容器,向甲容器中加入1 mol N2 (g)和6mol H2 (g),在一定条件下达到平衡时的热效应(吸热或放热)为Q,在相同条件下向乙容器中加入2 mol NH3 (g)和3mol H2 (g),达到平衡时的热效应(放热或吸热)为4Q。则甲容器中H2的转化率为________________。
高二化学填空题极难题查看答案及解析
-
已知杯芳烃是由苯酚和甲醛经缩合反应而生成的一类环状化合物,因其分子形状与希腊圣杯相似,且是由多个苯环构成的芳香族分子,由此得名。杯芳烃以“杯[n]芳烃”的形式命名,n是芳环的数目。下图所示的是叔丁基[—C(CH3)3]取代的杯[n]芳烃的结构简式。
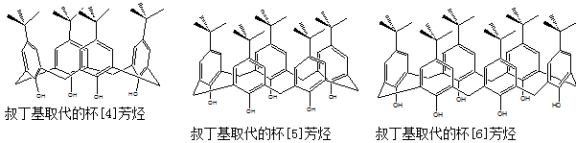
回答下列问题:
(1)杯[n]芳烃的通式是: ;
(2)若叔丁基取代的杯[n]芳烃在光照情况下和氯气反应时不取代苯环上的氢和酚羟基上的氢,则其一氯代物有 种;若存在叔丁基取代的杯[2015]芳烃,则光照情况下,其二氯代物有 种。
高二化学填空题极难题查看答案及解析
-
(16分)甲醇(CH3OH)是一种重要的化工原料,也是一种比较理想的燃料。甲醇在各个领域有着广泛的应用。
(1)实验测得:32 g甲醇在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出726.4 kJ的热量,试写出甲醇燃烧的热化学方程式:________________。
(2)燃料电池是一种连续地将燃料和氧化剂的化学能直接转换成电能的化学电池。下图是一个化学过程的示意图。2CH3OH+3O2+4KOH
K2CO3+6H2O
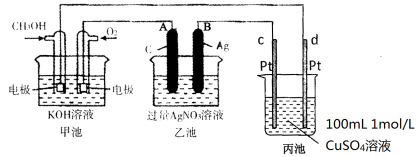
①A(石墨)电极的名称是 。
②通入O2的电极的电极反应式是 。
③写出通入CH3OH的电极的电极反应式是 。
④乙池中反应的化学方程式为 。
⑤当电路中通过0.01mol电子时,丙池溶液的C(H+) = mol/L(忽略电解过程中溶液体积的变化)。
(3)合成甲醇的主要反应是:2H2(g)+ CO(g)
CH3OH(g) △H=—90.8 kJ·mol—1。
①在恒温恒容条件下,充入一定量的H2和CO,发生反应2H2(g)+ CO(g)
CH3OH(g)。则该反应达到平衡状态的标志有
a.混合气体的密度保持不变
b.混合气体的总压强保持不变
c.CO的质量分数保持不变
d.甲醇的浓度保持不变
e.v正(H2)= v逆(CH3OH)
f.v(CO)= v(CH3OH)
②要提高反应2H2(g)+ CO(g)
CH3OH(g)中CO的转化率,可以采取的措施是:
a.升温
b.加入催化剂
c.增加CO的浓度
d.加入H2
e.加入惰性气体
f.分离出甲醇
高二化学填空题极难题查看答案及解析
-
(14分)请回答下列问题:
(1)下表列出了一些化学键的键能E:
化学键
H—H
O===O
O—H
E/kJ·mol-1
436
x
463
反应H2(g)+
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,则x=__________。
(2)铅蓄电池是正极板上覆盖有PbO2,负极板上覆盖有Pb,电解质溶液是H2SO4溶液,电池放电时的总反应:Pb+PbO2+2H2SO4=2PbSO4+2H2O。
请写出充电时阴极的电极反应式:
(3)反应m A+n B
p C,在某温度下达到平衡。
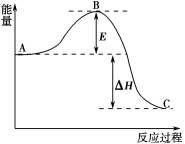
①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系是_______。
②若C为气体,且m + n = p,在加压时化学平衡发生移动,则平衡必定向_______方向移动。
③若再升高温度,平衡向逆向移动,则正反应为 反应(填“吸热”或“放热”)
(4)依据氧化还原反应Zn(s)+Cu2+(aq)===Zn2+(aq)+Cu(s)设计的原电池如图所示。
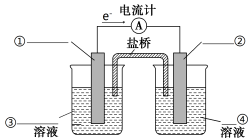
①请在图中标出电极材料及电解质溶液(写化学式)
②盐桥中的Cl-向________极移动(填“左”或“右”)。
高二化学填空题极难题查看答案及解析
-
(10分)有A、B、C、D、E、F六种元素,已知:它们位于三个不同短周期,核电荷数依次增大;A与E、B与F分别同主族;A与D按原子个数比1﹕1或2﹕l形成常温下为液态的化合物,E也能与D按原子个数比1﹕1或2﹕l形成化合物,B的外围电子数为内层电子数的两倍,B、C分别都能与D按原子个数比1﹕1或1﹕2形成化合物。请按要求回答以下问题:

(1)上图是A与D形成的一种化合物的晶体结构示意图,其中的虚线表示________, E与D按原子个数比1﹕1形成的化合物的电子式为________。
(2)人们通常把拆开l mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表列出了上述部分元素形成的化学键的键能:
化学键
F—D
F—F
B—B
F—B
C═D
D═D
键能/kJ·mol-1
460
176
347.7
347
745
497.3
①下列三种物质形成的晶体,熔点由高到低的顺序(用a、b、c表示):________
a.F与B形成的化合物 b.B与D形成的稳定化合物 c.F的单质
②F单质晶体中一个F原子与其紧邻的F原子形成的空间构型为_____________,
③已知加热下可发生如下转化:
F(s) + D2(g) 加热 FD2(s)
根据上表数据计算F单质晶体发生上述反应的反应热△H为:________。
高二化学填空题极难题查看答案及解析
-
HecK反应是偶联反应的一种,例如:
反应①:
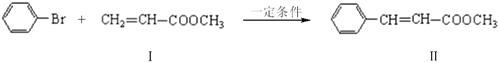
化合物Ⅰ可以由以下途径合成:

(1)化合物Ⅱ的分子式为____________,1mol该物质最多可与________molH2发生加成反应.
(2)卤代烃CH3CHBrCH3发生消去反应可以生成化合物Ⅲ,相应的化学方程为________________(注明条件)。
(3)化合物Ⅳ含有甲基且无支链的同系物Ⅵ的分子式为C4H6O,则化合物Ⅵ的结构简式为__________;
(4)化合物Ⅴ可与CH3CH2OH发生酯化反应生成化合物Ⅶ,化合物Ⅶ在一定条件下可以发生加聚,则其加聚产物的结构简式为_________________;
(5)化合物Ⅱ的一种同分异构体Ⅷ能发生银镜反应,且核磁共振氢谱只有三组峰,峰面积之比为1:2:2,Ⅷ的结构简式为_______________;
(6)一定条件下,
与
也可以发生类似反应①的反应,其有机产物的结构简式为________________。
高二化学填空题极难题查看答案及解析
-
I.(1)对反应N2O4(g)
2NO2(g) △H>0 ,在温度为T1、 T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。T1 T2(填“>”、“<”或“=”);A、C两点的速率VA VC(同上)。

(2)在100℃时,将0.400mol的NO2气体充入2L真空定容密闭容器中,
每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
时间(s)
0
20
40
60
80
n(NO2)/mol
0.40
n1
0.26
n3
n4
n(N2O4)/mol
0.00
0.05
n2
0.08
0.08
①该反应的平衡常数K的值为 ;
②若在相同情况下最初向该容器充入的是N2O4,要达到上述同样的平衡状态,N2O4的起始浓度是_____________mol/L。
③计算②中条件下达到平衡后混合气体的平均相对分子质量为 ;(结果保留小数点后一位)
II. 在0.5 L的密闭容器中,一定量的H2和N2进行如下化学反应:3H2(g)+N2(g)
2NH3(g) △H <0,其化学平衡常数K与温度t的关系如下表。请回答下列问题。
t/℃
200
300
400
K
K1
K2
0.5
④比较K1,K2的大小,K1_________K2(填写“ >”、“=”或“<”)。
⑤在400℃时,当测得NH3和N2、H2的物质的量分别为3mol和1 mol、2 mol时,则该反应的 V(H2)正_________ V (H2)逆(填写“>”、“=”或“<”)。
高二化学填空题极难题查看答案及解析