-
A、B、C、D、E五种微粒,它们可能是原子或离子,并且所含的元素都在短周期。A显负价时,不能被任何氧化剂氧化;金属B的原子核内质子数比前一周期的同族元素多8,其单质不能从CuSO4溶液中置换出Cu;C元素有三种同位素,Cl、C2、C3,C1的质量数分别为C2、C3的1/2和1/3;D的气态氢化物溶于水后显碱性;E是由两种不同元素组成的带负电荷的微粒,它共有10个电子,E极易与C+结合成中性微粒。回答:
(1)写出五种微粒的符号:A 、B 、C 、D 、E 。
(2)C的同位素名称:C2 。
(3)C和D形成分子的电子式为 ,空间结构为 。
高二化学填空题极难题查看答案及解析
-
能源和环境保护是世界各国关注的热点话题。请回答下列问题:
Ⅰ.收集和利用CO2是环境保护的热点课题。
500 ℃时,在容积为1 L的密闭容器中充入1 mol CO2和3 mol H2,发生如下反应:CO2(g)+3H2(g)
CH3OH(g)+H2O(g) ΔH<0,测得CO2和CH3OH的浓度与时间的关系如图所示。
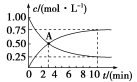
(1)A点含义是_____________;0~10 min内v(H2)=__________,平衡常数K1=__________(保留一位小数)。
(2)反应在500 ℃达到平衡之后,改变反应温度为T,CH3OH的浓度以0.030 mol·L-1·min-1的平均反应速率增大,经5 min又达到新平衡。
①T________500 ℃(填“大于”“小于”或“等于”),判断理由是_______________。
②列式计算温度为T时反应的平衡常数K2=_______________________。
(3)T时,反应达到平衡后,将反应容器的容积增大一倍。平衡向________(填“正反应”或“逆反应”)方向移动,判断的理由是___________________。
Ⅱ.含有Cr2O72-的废水毒性较大,某工厂排放的废水中含5.0×10-3 mol·L-1的Cr2O。为了使废水的排放达标,进行如下处理:
Cr2O72-
Cr3+、Fe3+
Cr(OH)3、Fe(OH)3
已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31。
若处理后的废水中残留的c(Fe3+)=2.0×10-13 mol·L-1,则残留的Cr3+的浓度为________。
高二化学填空题极难题查看答案及解析
-
按要求回答下列问题:
Ⅰ.(1)用系统命名法命名烃A:_________;
 烃A的一氯代物具有不同沸点的产物有________种。
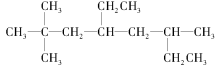
烃A的一氯代物具有不同沸点的产物有________种。(2)有机物
的系统名称是________,将其在催化剂存在下完全氢化,所得烷烃的系统名称是____________。
(3)3甲基1戊炔的结构简式为________;
(4)
的分子式为________;
名称为: 。
Ⅱ.某些有机化合物的模型如图所示。
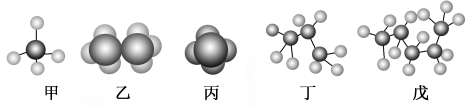
回答下列问题:
(1)属于比例模型的是________(填“甲”、“乙”、“丙”、“丁”或“戊”,下同)。
(2)表示同一种有机化合物的是____________。
(3)存在同分异构体的是________,写出其同分异构体的结构简式_____________________。
(4)含碳量最低的是________,含氢量最低的分子中氢元素的质量百分含量是________(保留一位小数)。
(5)C10H14 属于苯的同系物的所有同分异构体共有 种。
Ⅲ.用离子方程式解释下列过程:
①纯碱溶液显碱性:____________________。
②泡沫灭火器的反应原理(硫酸铝溶液与小苏打):_____________________。
③AgCl的浊液中加入K2S溶液,白色沉淀变为黑色:____________________。
高二化学填空题极难题查看答案及解析
-
工业上需要利用一批回收的含铜废料制造胆矾(CuSO4·5H2O)。该废料中各种成份含量如下:Cu和CuO约占87%,其它为Mg、Al、Fe、Si及其氧化物,还有少量的难溶物质。工艺流程为:
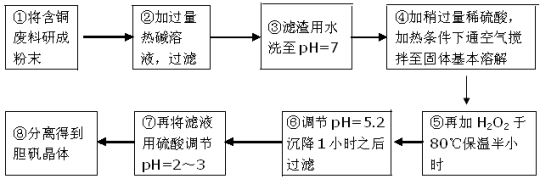
部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH如下表:
沉淀物
Al(OH)3
Fe(OH)3
Cu(OH)2
Mg(OH)2
Fe(OH)2
pH
5.2
3.1
6.7
9.4
9.7
请回答下列问题:
(1)步骤①中为什么要将含铜废料研磨成粉状? 。
(2)步骤②中的离子方程式(写出2个即可):
、
。
(3)步骤⑤中H2O2参加反应的离子方程式: 。
(4)步骤⑥中调节溶液pH时适宜的物质是 (填序号)。
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Cu(OH)2 E.MgCO3
(5)步骤⑦中用硫酸调节pH=2~3的原因是 。
(6)步骤⑧的分离方法步骤是 。
高二化学填空题极难题查看答案及解析
-
(12分)汽车尾气里含有的NO气体是由内燃机燃烧时产生的高温引起氮气和氧气反应所致: N2(g)+O2(g)
2NO(g) ΔH>0。已知该反应在2404℃时,平衡常数K=6.4×10-3。
请回答下列问题。
(1)该反应的平衡常数表达式为____________________________________。
(2)该温度下,向2 L密闭容器中充入N2和O2各1mol,平衡时,N2的转化率是________%(保留整数)。
(3)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1 mol/L、4.0×10-2 mol/L和3.0×10-3 mol/L,此时反应________(填“处于化学平衡状态”、“向正方向进行”或“向逆方向进行”),理由是_____________________。
(4)将N2、O2的混合气体充入恒温恒容密闭容器中,如图变化趋势正确的是________。
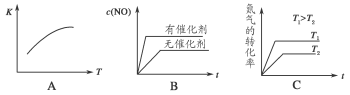
向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数_______(填“变大”、“变小”或“不变”)。
高二化学填空题极难题查看答案及解析
-
(14分)工业上以氨气为原料(铂铑合金网为催化剂)催化氧化法制硝酸的过程如下:
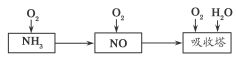
(1)已知反应一经发生,铂铑合金网就会处于红热状态。写出氨催化氧化的化学方程式:_____。当温度降低时,化学平衡常数K值________(填“增大”“减小”或“无影响”)。
(2)氨气是制取硝酸的重要原料,合成氨反应的化学方程式如下:N2+3H2
2NH3,该反应在固定容积的密闭容器中进行。
①下列各项标志着该反应达到化学平衡状态的是________(填字母)。
A.容器内N2、H2、NH3的浓度之比为1∶3∶2
B.v正(N2)=v逆(H2)
C.容器内压强保持不变
D.混合气体的密度保持不变
②若在恒温条件下,将N2与H2按一定比例混合通入一个容积为2 L固定容积的密闭容器中,5 min后反应达平衡时,n(N2)=1.0 mol,n(H2)=0.8 mol,n(NH3)=0.8 mol,则反应速率v(H2) =_____,平衡常数=________。
③若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将 (填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度 (填“大于”“小于”或“等于”)原来的2倍。
高二化学填空题极难题查看答案及解析
-
有X、Y、Z三种常见元素,已知:①X2-、Y-均与Y的气态氢化物分子具有相同的电子数;②Z与Y可组成化合物ZY3,ZY3溶液遇苯酚呈紫色。请回答:
⑴Y的最高价氧化物对应水化物的化学式是________ 。
⑵将ZY3溶液滴入沸水可得红褐色液体,
反应的离子方程式是________ ,
此液体具有的性质是________ (填写序号字母)。
a.光束通过该液体时形成光亮的“通路”
b.插入电极通直流电后,有一极附近液体颜色加深
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
⑶X单质在空气中燃烧生成一种无色有刺激性气味的气体。
①已知一定条件下,每1mol该气体被O2氧化放热98.0kJ。若2mol 该气体与1mol O2在此条件下发生反应,达到平衡时放出的热量是176.4kJ,则该气体的转化率为________。
②该无色有刺激性气味的气体与含1.5molY的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目
________
________ 。
高二化学填空题极难题查看答案及解析
-
药物阿莫西林能杀灭或抑制细菌繁殖,它的合成路线如下:
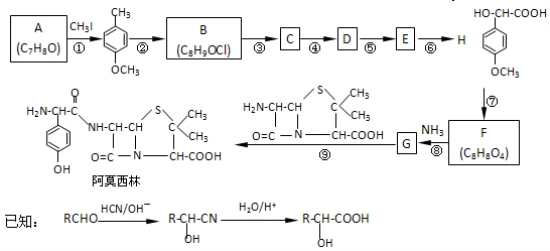
A能使三氯化铁溶液显色。
完成下列填空:
(1)写出A的结构简式:_____________;CH3I的作用___________________。
(2)反应④的化学方程式____________________________________。
H的一种同分异构体的一氯代物的结构为
,该物质在NaOH水溶液中加热反应时的化学方程式为 。
(3)试写出能同时满足以下条件H所有的同分异构体 。
a.能与氯化铁溶液发生显色反应 b.能与碳酸氢钠反应产生无色气泡
c.取0.1mol有机物能与足量Na反应能产生3.36L(标况下)气体
d.苯环上的一氯代物只有两种,但苯环上氢原子数不少3
e.分子中含有甲基
(4)试利用CH3CH=CH2为原料制备
的合成路线流程图(无机试剂任用)。
合成路线流程图例如下:
高二化学填空题极难题查看答案及解析
-
已知:①有机化学反应因反应条件不同,可生成不同的有机产品。例如:
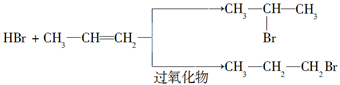
②苯的同系物与卤素单质混合,若在光照条件下,侧链烃基上的氢原子被卤素原子取代;若在催化剂作用下,苯环某些位置上的氢原子被卤素原子取代。
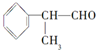
工业上利用上述信息,按下列路线合成结构简式为的物质,该物质是一种香料。
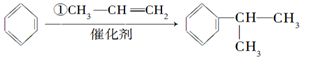
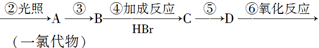
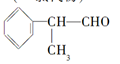
请根据上述路线,回答下列问题:
(1)A的结构简式可能为_____________、____________________。
(2)反应③的反应类型为_________________;反应⑤的条件是_______________
(3)反应④的化学方程式为(有机物写结构简式,并注明反应条件,下同):
__________________________________________________。
(4)工业生产中,中间产物A须经反应③④⑤得D,而不采取将A直接转化为D的方法,其原因是____________________________。
(5)检验产品中官能团的化学反应方程式为:_____________________________。
(6)这种香料具有多种同分异构体,其中某些物质有下列特征:①其水溶液遇FeCl3溶液呈紫色;② 苯环上的一溴代物有两种;③分子中没有甲基。写出一种符合上述条件的物质可能的结构简式:________。
高二化学填空题极难题查看答案及解析
-
最新研究发现,用隔膜电解法处理高浓度乙醛废水具有工艺流程简单、电耗较低等优点,其原理是使乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸,总反应为:2CH3CHO + H2O
CH3CH2OH + CH3COOH
实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置示意图如右图所示。
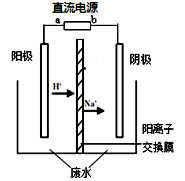
(1)若以甲烷燃料电池为直流电源,则燃料电池中b极应通入 (填化学式)气体。
(2)电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体。电极反应如下:
阳极:① 4OH--4e-=O2↑+2H2O
② 。
阴极:① 。
②CH3CHO+2e-+2H2O=CH3CH2OH+2OH-
(3)电解过程中,阴极区Na2SO4的物质的量 (填“增大”、“减小”或“不变”)。
(4)电解过程中,某时刻测定了阳极区溶液中各组分的物质的量,其中Na2SO4与CH3COOH的物质的量相同。下列关于阳极区溶液中各微粒浓度关系的说法正确的是 (填字母序号)。
a. c(Na+)不一定是c(SO42- )的2倍
b. c(Na+)=2c(CH3COOH)+2c(CH3COO-)
c. c(Na+)+c(H+)=c(SO42-)+c(CH3COO-)+c(OH-)
d. c(Na+)>c(CH3COOH)>c(CH3COO-)>c(OH-)
(5)已知:乙醛、乙醇的沸点分别为20.8℃、78.4℃。从电解后阴极区的溶液中分离出乙醇粗品的方法是 。
高二化学填空题极难题查看答案及解析