-
地壳中含量最多的金属元素,非金属元素和空气中含量最多的元素组成的化合物是
A. Al(NO3)3 B. CaCO3 C. Al2(SO4)3 D. Fe(NO3)3
难度: 中等查看答案及解析
-
在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下表
物 质
甲
乙
丙
丁
反应前质量(g)
5
2
42
12
反应后质量(g)
X
2
6
40
关于此反应,下列认识正确的是
A. 乙一定是催化剂 B. 参加反应的丙、丁的质量比为1: 2
C. X的值为13 D. 乙、丙中所含元素种类与甲、丁中所含元素种类相同
难度: 中等查看答案及解析
-
二氧化钛(TiO2)是一种用途广泛的化工原料,用四氯化钛(TiCl4)与某常见物质X反应可
制得二氧化钛,反应的化学方程式为:TiCl4 + □X = TiO2 + 4HCl 关于物质X,下列说法正确的
是( )
A.该物质由碳、氢、氧三种元素组成
B.该物质的化学式为H2O2
C.该物质中氢、氧元素的质量比为1:8
D.该物质中氧元素的质量分数是5%
难度: 中等查看答案及解析
-
生活中的下列现象,用分子的相关知识解释,不正确的是()
A. 水受热变成水蒸气,水分子分裂成了原子
B. 经过食堂附近,闻到饭菜香味,说明分子在不断地运动
C. 50mL水和50mL酒精混合后,总体积小于100mL,说明分子间有间隔
D. 燃烧的木条伸入集满氧气的集气瓶中燃烧更旺,伸入集满二氧化碳的集气瓶中熄灭,说明分子不同化学性质不同
难度: 中等查看答案及解析
-
芬太奴是强有力的麻醉剂,在军事上作为“非致命武器”曾被用作解救人质,其化学式为C20H24N2O,下列关于芬太奴的说法中不正确的是( )
A. 芬太奴的每一个分子中含有47个原子
B. 芬太奴是由碳、氢、氮、氧四种元素组成的物质
C. 一个芬太奴分子中含有一个氮气分子
D. 芬太奴中碳、氢、氮、氧元素的质量比为60:6:7:4
难度: 简单查看答案及解析
-
学以致用,请用所学知识判断下列做法安全可行的是 ( )
A. 在加油站拨打或接听移动电话 B. 遇火灾时打开所有门窗
C. 档案资料着火,可用液态二氧化碳扑火 D. 启用闲置的沼气池前先进行火把实验
难度: 简单查看答案及解析
-
物质世界充满了变化。下列变化属于物理变化的是
A. 光合作用 B. 钢铁生锈 C. 酸雨侵蚀 D. 冰山融化
难度: 简单查看答案及解析
-
下列物质中氮元素的化合价最低的是( )
A. NaNO3 B. NO2 C. NH4Cl D. N2
难度: 中等查看答案及解析
-
下列实验操作中,正确的是()
A.
 取用固体药品 B.
取用固体药品 B. 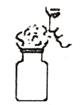 闻药品味道
闻药品味道C.
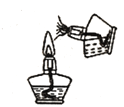 点燃酒精灯 D.
点燃酒精灯 D.  滴加液体
滴加液体难度: 简单查看答案及解析
-
下列物质按混合物、化合物,氧化物、单质的顺序排列的是( )
A. 石油 石灰水 干冰 石墨
B. 汽水 煤 二氧化碳 金刚石
C. 空气 碳酸钙 蒸馏水 液氧
D. 天然气 稀盐酸 氧化铜 锌
难度: 中等查看答案及解析
-
下列几种水硬度最小的是( )
A. 自来水 B. 矿泉水 C. 雨水 D. 蒸馏水
难度: 简单查看答案及解析
-
化学概念有交叉、并列和包含等关系,下列概念之间的关系,说法正确的是( )
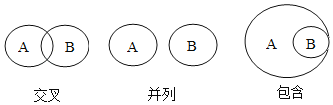
A. 单质和化合物属于包含关系
B. 化合物和纯净物属于并列关系
C. 纯净物和混合物属于交叉关系
D. 化合物和氧化物属于包含关系
难度: 中等查看答案及解析
-
我国人均水量居全世界八十几位,许多地区已出现因水资源短缺影响人民生活、制约经济发展的局面,因此节约用水,防止水源污染是我们每一位公民的义务。下列有关水的说法中正确的是( )
A. 为节约用水,可用工业废水直接浇灌农田
B. 水体“富营养化”能促进水生动植物生长
C. 工业上使用循环水,可节约水资源
D. 生活污水不会造成水体污染
难度: 简单查看答案及解析
-
李克强总理在2016年政府工作报告中提出“推动形成绿色生产生活方式,加快改善生态环境”.你认为日常生活中的下列做法不正确环保精神的是( )
A. 外出时乘坐公交车,少开私家车
B. 关闭所有工厂
C. 减少使用一次性筷子
D. 推广鼓励使用可降解塑料制品
难度: 中等查看答案及解析
-
如图是从元素周期表第Ⅶ主族截取的局部图,图中的四种元素影响着我们的生活.下面是根据图示信息的一些说法,其中错误的是( )
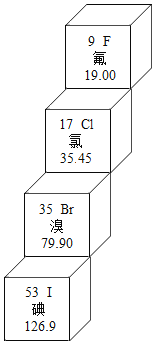
A. 这四种元素都属于非金属元素
B. 这四种元素具有相似的化学性质
C. 1个氯原子的质量约是35.45g
D. 氟原子核外电子数为9
难度: 中等查看答案及解析
-
某正二价金属的氧化物中,金属元素和氧元素的质量之比为5:2,该金属的相对原子质量为( )
A. 40 B. 56 C. 27 D. 24
难度: 中等查看答案及解析
-
一氧化碳和二氧化碳的共同点是( )
A. 都可用碳和氧气起反应来制取
B. 都是具有还原性的气体
C. 都有毒
D. 密度都比空气大
难度: 中等查看答案及解析
-
下列四种粒子的结构示意图中,表示金属元素原子的是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
推理是一种重要的化学思维方法,以下推理不合理的是( )
A. 因为H2O和H2O2的组成元素相同,所以他们的化学性质相同
B. 化合物一定由不同种元素组成,但由不同种元素组成的物质不一定是化合物
C. 分子、原子都是不带电的粒子,但是不带电的粒子不一定是分子、原子
D. 金刚石、石墨都是由碳元素组成的单质,所以它们的化学性质相同
难度: 中等查看答案及解析
-
在工业上,下列提高燃料利用率的措施中,与燃料充分燃烧无关的是:
A. 把煤炭磨成粉状进行燃烧
B. 把柴油喷成雾状进行燃烧
C. 给锅炉鼓风,增加空气供给量
D. 给锅炉外壳装隔热层,减少热量散失
难度: 中等查看答案及解析
-
自然界里丰富多彩的物质都是由极其微小的粒子构成的,化学就像一架“显微镜”,带领我们一步步地深入认识和研究物质,使我们学会了“用微观眼光看世界”。
(1)若“
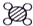 ”表示一个甲烷分子,则“
”表示一个甲烷分子,则“”表示 (填写化学符号),甲烷中各元素的质量比为 。
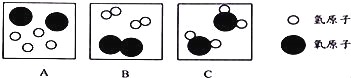
(2)水通入直流电后可分解,以下图片是水分解过程中微粒变化的部分示意图,请按它们在化学变化过程中出现的顺序排列 (用图中的字母表示),写出反应的化学方程式 。
难度: 中等查看答案及解析