-
第三能层含有的轨道数为
A. 3 B. 5 C. 7 D. 9
难度: 简单查看答案及解析
-
以下能级符号不正确的是
A. 3s B. 3p C. 3d D. 3f
难度: 简单查看答案及解析
-
下列原子或离子原子核外电子排布不属于基态排布的是
A. N:
B.
:
C. Na:
D. Si:
难度: 简单查看答案及解析
-
基态碳原子的最外能层的各能级中,电子排布的方式正确的是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
在d轨道中电子排布成
而不能排布成
其最直接的根据是
A. 能量最低原理 B. 泡利原理
C. 原子轨道构造原理 D. 洪特规则
难度: 简单查看答案及解析
-
多电子原子中,3s、3d、4p轨道能级次序为
A.
B.
C.
D. 无法确定
难度: 简单查看答案及解析
-
用稀的碱性溶液或清水浸泡,可使残留在蔬菜上的农药降低毒性
如用碱性溶液浸泡蔬菜,可在水中加入适量的
A. 白酒 B. 纯碱 C. 白糖 D. 食醋
难度: 简单查看答案及解析
-
有关中和滴定有如下操作:
洗涤;
往滴定管内注入标准溶液;
滴定;
检查滴定管是否漏水;
用标准溶液润洗滴定管
其正确的操作顺序是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
能使水的电离平衡右移,且水溶液显碱性的离子是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
物质的量浓度相同的三种盐NaX、NaY、NaZ的溶液,其pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是
A. HX、HY、HZ B. HX、HZ、HY C. HZ、HY、HX D. HY、HZ、HX
难度: 中等查看答案及解析
-
将足量的
分别添加到下述四种溶液中,所得溶液
最小的是
A.
的盐酸 B.
溶液
C.
溶液 D.
溶液
难度: 中等查看答案及解析
-
下列方程式属于水解反应方程式的是
A.
B.
C.
D.
难度: 简单查看答案及解析
-
在蒸发皿中加热蒸干下列物质的溶液并灼烧,可得原有物质的固体是
A. 氯化铝 B. 硫酸铁 C. 碳酸氢钠 D. 亚硫酸钠
难度: 中等查看答案及解析
-
下列物质的水溶液因水解而呈酸性的是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
有体积相同、相等pH的烧碱溶液和氨水,下列叙述中正确的是
A. 两溶液物质的量浓度相同
B. 用同浓度的盐酸中和时,消耗盐酸的体积相同
C. 两溶液中
离子浓度相同
D. 加入等体积的水稀释后,pH仍相等
难度: 中等查看答案及解析
-
下列溶液一定呈中性的是
A.
溶液
B.
的溶液
C. 使石蕊试液呈紫色的溶液
D. 酸与碱恰好完全反应生成正盐的溶液
难度: 中等查看答案及解析
-
在
时,将
的NaOH溶液与
的
溶液等体积混合后,下列关系式中正确的是
A.
B.
C.
D.
难度: 中等查看答案及解析
-
已知反应
能完全进行,则对下列推断中正确的是
A.
溶液的
,将其蒸干灼烧后,得到的残留物可能为BeO
B.
溶液的
,将其蒸干灼烧后,得到的残留物可能为BeO
C.
不具有两性
D.
水溶液的导电性强,因此
一定是离子化合物
难度: 中等查看答案及解析
-
下列溶液中,
离子的浓度最大的是
A.
的
溶液
B.
的
溶液
C.
的
溶液
D.
的
溶液
难度: 中等查看答案及解析
-
下列说法与盐类水解无关的是
A. 粗盐在空气中易潮解
B.
与
用于金属焊接中除锈
C. 用热纯碱溶液去油污
D. 蒸干并灼烧
溶液得到
难度: 中等查看答案及解析
-
在水中达到溶解平衡:
(aq),下列哪种情况可使
的量减少
A. 加入
溶液 B. 加入少量NaOH
C. 加入
溶液 D. 加入
溶液
难度: 中等查看答案及解析
-
常温下,浓度均为
的四种溶液pH如下表依据已有的知识和信息判断,下列说法正确的是
溶质
NaClO
pH
A. 常温下,
的水解能力强于其电离能力
B. 常温下,相同物质的量浓度的
、
、
依次升高
C.
溶液中存在以下关系:
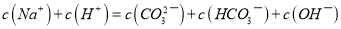
D. 向氯水中加入少量
固体,不能增大HClO的浓度
难度: 中等查看答案及解析
 .
.