-
下列各组离子在水溶液中一定能大量共存的是( )
A. 含有大量 Ba2+的溶液中:Cl-、K+、SO42-、CO32-
B. 含有大量H+的溶液中:Mg2+、Na+、SO42-、HCO3-
C. 含有大量OH-的溶液中:Mg2+、NO3-、SO42-、CO32-
D. 含有大量Na+的溶液中:H+、K+、NO3-、SO42-
难度: 中等查看答案及解析
-
镁、铝合金粉末10.2g溶于500mL 4mol·L-1盐酸中恰好完全反应。若加入2mol·L-1的氢氧化钠溶液,使得沉淀达到最大量,则需加入氢氧化钠溶液的体积为
A. 100mL B. 500mL C. 1000mL D. 1500mL
难度: 中等查看答案及解析
-
关于Na2CO3和NaHCO3性质的说法错误的是( )
A. 热稳定性:NaHCO3<Na2CO3
B. 与同浓度盐酸反应的剧烈程度:NaHCO3<Na2CO3
C. 相同温度时,在水中的溶解性:NaHCO3<Na2CO3
D. 等物质的量的Na2CO3、NaHCO3分别与足量盐酸反应产生的CO2质量相同
难度: 简单查看答案及解析
-
下列物质鉴别方法不正确的是( )
A. 用焰色反应鉴别NaCl、KCl溶液
B. 用氢氧化钠鉴别MgCl2溶液、AlCl3溶液
C. 利用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液
D. 用澄清石灰水鉴别SO2、CO2气体
难度: 简单查看答案及解析
-
对下列实验的评价,正确的是( )
A. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
B. 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32-
C. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
D. 验证烧碱溶液中是否含有Cl﹣,先加过量的稀硝酸除去OH﹣,再加入AgNO3溶液,如有白色沉淀,则证明有Cl﹣
难度: 中等查看答案及解析
-
某Na2CO3样品中含有K2CO3、NaNO3和Ba(NO3)2三种杂质中的一种或两种。现将11 g样品加入足量水中,样品全部溶解。再加入过量的CaCl2溶液,得到10 g沉淀。对样品所含杂质的正确判断是( )
A. 肯定有NaNO3
B. 肯定有NaNO3,可能还含有K2CO3
C. 肯定没有Ba(NO3)2,可能有NaNO3
D. 肯定没有K2CO3和Ba(NO3)2
难度: 中等查看答案及解析
-
设NA代表阿伏加德罗常数,下列说法正确的是( )
A. 1 mol硫单质在过量氧气中燃烧产生NA个SO3分子
B. 标准状况下,22.4 L SO3中含有氧原子数为3NA
C. 标准状况下,36 g H2O中含有氧原子数为1 mol
D. 5.4 g铝单质与足量NaOH溶液反应,转移电子数为0.6NA
难度: 简单查看答案及解析
-
下列关于化学反应的说法正确的是( )
A. 有单质生成的化学反应,一定是氧化还原反应
B. 金属单质在氧化还原反应中只能作还原剂
C. 有非金属单质参加的化合反应,非金属单质一定是氧化剂
D. 有气体生成的化学反应一定是氧化还原反应
难度: 中等查看答案及解析
-
2.3 g纯净的金属钠在干燥的空气中被氧化后得到3.5 g固体,由此判断其产物( )
A. 只有Na2O B. 只有Na2O2 C. 有Na2O和Na2O2 D. 无法确定
难度: 简单查看答案及解析
-
下列关于金属性质的叙述中正确的是( )
A. 钠与氧气反应时,产物是由O2的用量决定的
B. 打磨的铝箔加热至熔化时,铝会滴落
C. 点燃镁之前,应先用砂纸打磨
D. 铁只能与氧气反应,与氯气不反应
难度: 简单查看答案及解析
-
向紫色石蕊溶液中加入过量Na2O2粉末,振荡,正确的叙述是( )
A. 最后溶液变蓝色
B. 溶液先变蓝色最后褪色
C. 溶液仍为紫色
D. 因为Na2O2与石蕊发生氧化还原反应而无气泡产生
难度: 中等查看答案及解析
-
氧化铝的熔点很高,常用于制造耐火材料,例如制作耐火坩埚。下列操作不能在氧化铝坩埚中进行的是( )
A. 加热使CuSO4·5H2O失水 B. 加热使KMnO4分解
C. 加热熔化烧碱 D. 加热分解碱式碳酸铜
难度: 简单查看答案及解析
-
下列关于Al(OH)3的性质叙述错误的是( )
A. Al(OH)3受热易分解生成Al2O3和H2O
B. Al(OH)3是难溶于水的白色胶状物质
C. Al(OH)3能凝聚水中的悬浮物,也能吸附色素
D. Al(OH)3既能溶于NaOH溶液、氨水,又能溶于盐酸
难度: 简单查看答案及解析
-
用铝箔包裹0.1 mol金属钠,用钉扎出一些小孔,放入水中,完全反应后,用排水取气法收集产生的气体,则得到的气体为(标准状况)( )
A. 氧气和氢气的混合气体 B. 1.12升氢气
C. 大于1.12升氢气 D. 小于1.12升
难度: 中等查看答案及解析
-
等体积、等物质的量浓度的盐酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为3∶4,则甲、乙两烧杯中的反应情况可能是( )
A. 甲、乙中都是铝过量 B. 甲中铝过量,乙中碱过量
C. 甲中酸过量,乙中铝过量 D. 甲、乙中都是铝不足
难度: 中等查看答案及解析
-
除去氧化镁中的氧化铝可选用的试剂是 ( )
A. 氢氧化钾溶液 B. 硝酸 C. 浓硫酸 D. 稀盐酸
难度: 简单查看答案及解析
-
将质量均为m g的O2、X、Y气体分别充入相同容积的密闭容器中,压强(P)与温度(T)的关系如图所示,则X、Y气体可能分别是( )
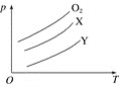
A. C2H4、CH4 B. CO2、Cl2
C. SO2、CO2 D. CH4、Cl2
难度: 简单查看答案及解析
-
已知在碱性溶液中可发生如下反应:2R(OH)3+3ClO﹣+4OH﹣=2RO4n-+3Cl﹣+5H2O,则RO4n-中R的化合价是( )
A. +3 B. +4 C. +5 D. +6
难度: 中等查看答案及解析
-
一定质量的镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图。下列关于反应的说法错误的是

A.镁和铝的物质的量之比为3∶2
B.镁和铝转移电子数之比为1∶1
C.镁和铝的摩尔质量之比为8∶9
D.镁和铝反应所用时间之比为3∶2
难度: 中等查看答案及解析
-
由Zn、Fe、Mg、Al四种金属中的两种组成的混合物10 g与足量的盐酸反应产生1.0 g H2,则混合物中一定含有的金属是( )
A. Zn B. Fe C. Al D. Mg
难度: 中等查看答案及解析
-
将钠、镁、铝各0.3 mol分别放入100 mL 1 mol·L-1的盐酸中,同温同压下产生的气体体积比是( )
A. 1∶2∶3 B. 6∶3∶2 C. 3∶1∶1 D. 1∶1∶1
难度: 困难查看答案及解析
-
将11.5 g钠、28 g铁分别放入20 mL 1 mol·L-1的盐酸中,结果正确的是( )
A. 铁与盐酸反应比钠剧烈 B. 钠与盐酸反应产生的气体多
C. 铁与盐酸反应产生的气体多 D. 反应结束时产生的气体一样多
难度: 简单查看答案及解析
-
将5.4 g Al投入200.0 mL 2.0 mol/L的某溶液中有氢气产生,充分反应后有金属剩余。该溶液可能为
A.NaOH溶液 B.Ba(OH)2溶液
C.H2SO4溶液 D.HCl溶液
难度: 中等查看答案及解析
-
有两份质量相同的碳酸氢钠固体,向第一份中加入盐酸使其充分反应;将第二份加热使其完全分解,冷却至原温度再加入相同浓度的盐酸,充分反应,则它们所耗用的盐酸的体积比为( )
A. 2∶1 B. 1∶1 C. 1∶2 D. 4∶1
难度: 简单查看答案及解析
-
使5.16 g 二氧化碳和水蒸气的混合气体通过足量的过氧化钠,固体增重1.96 g,则参加反应的过氧化钠质量为( )
A. 7.8 g B. 3.9 g C. 3.2 g D. 15.6 g
难度: 中等查看答案及解析
-
某溶液中可能含有大量的Mg2+、Al3+、H+、Cl-和少量OH-,向该溶液中逐滴加入0.5 mol·L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示,则可判断原溶液中( )

A. 有Mg2+,没有Al3+
B. 有Al3+,没有Mg2+
C. 有Mg2+和Al3+
D. 有大量的H+、Mg2+和Al3+
难度: 中等查看答案及解析
-
下列操作中最终可以得到Al(OH)3的是( )
A. Al2O3和水混合加热
B. 过量的稀HCl加入到NaAlO2溶液中
C. 过量的NaOH溶液加入到AlCl3溶液中
D. 过量的氨气通入到AlCl3溶液中
难度: 简单查看答案及解析
-
向MgCl2、AlCl3的混合溶液中,开始滴加试剂X,之后改滴试剂Y,所得沉淀的物质的量n(mol)与试剂体积V(mL)间的关系如图所示。以下结论错误的是( )

A. X是盐酸,Y是NaOH溶液,且c(Y)=2c(X)
B. 原混合液中,c(Al3+)∶c(Mg2+)∶c(Cl-)=1∶1∶5
C. X是NaOH溶液,Y是盐酸,且c(NaOH)∶c(HCl)=2∶1
D. 从7至9相应的离子方程式为H++OH-===H2O
难度: 困难查看答案及解析
-
用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断下列说法错误的是( )

A.实验中发生的反应都是氧化还原反应
B.铝是一种较活泼的金属
C.铝与氧气反应是放热反应
D.铝片上生成的白毛是氧化铝和氧化汞的混合物
难度: 简单查看答案及解析
-
把2.3g钠放入水中,要使每100个水分子中含有1个Na+离子,所需水的质量是( )
A. 184g B. 181.8g C. 180g D. 183.6g
难度: 中等查看答案及解析

