-
1 mol MgCl2中含有 ( )
A. 3.01×1023个Mg2+ B. 6.02×1023个Cl-
C. 1 mol Mg2+ D. 1 mol Cl2
难度: 简单查看答案及解析
-
下列物质不属于电解质的是( )
A.C2H5OH B.KOH C.HNO3 D.BaCl2
难度: 简单查看答案及解析
-
下列变化中,需加入氧化剂的是( )
A. 2Cl-→Cl2 B. Fe3+ →Fe2+
C. Cu2+ →Cu D. MnO4-→MnO2
难度: 简单查看答案及解析
-
实验室中需要配制2 mol·L-1的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )
A.950 mL,111.2 g B.500 mL,117 g
C.1 000 mL,117 g D.任意规格,111.2 g
难度: 简单查看答案及解析
-
某有机物苯酚,其试剂瓶上有如下标识,其含义是( )


A.自燃物品、易燃 B.腐蚀性、有毒
C.爆炸性、腐蚀性 D.氧化剂、有毒
难度: 简单查看答案及解析
-
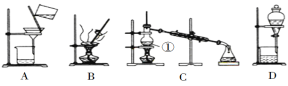
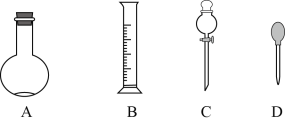
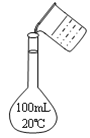
下列指定实验的装置图完全正确的是
A.称量氢氧化钠固体
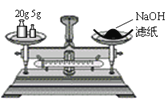
B.分离水和乙醇
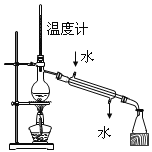
C.配制100mL0.10mol/L盐酸
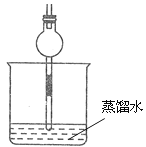
D.尾气处理吸收HCl气体
难度: 困难查看答案及解析
-
下列物质按酸、碱、盐分类依次排列正确的是( )
A.硫酸、纯碱、食盐
B.盐酸、生石灰、醋酸钠
C.醋酸、烧碱、硫酸铜
D.磷酸、石灰石、苛性钠
难度: 简单查看答案及解析
-
用NA表示阿伏德罗常数,下列叙述正确的是( )
A.标准状况下,22.4L H2O含有的分子数为NA
B.NA个CO2分子占有的体积为22.4L
C.物质的量浓度为1mol/L的MgCl2溶液中,含有Cl-个数为2NA
D.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA
难度: 中等查看答案及解析
-
下列溶液中Cl-的物质的量浓度最大的是( )
A.200mL2mol/L MgCl2溶液 B.1000mL 2.5mol/L MgCl2溶液
C.250mL 1.5mol/L AlCl3溶液 D.300mL 3mol/L KCl溶液
难度: 简单查看答案及解析
-
配制一定物质的量浓度的NaOH溶液时,造成所配制溶液浓度偏高的原因可能是( )
A.所用NaOH已潮解
B.定容时,俯视刻度线
C.用带游码的托盘天平称量NaOH固体质量时,误将砝码放在左盘,被称量物放在右盘
D.托盘天平的左右托盘上各放一张纸,调整天平至平衡后,将NaOH固体放在纸上称量
难度: 简单查看答案及解析
-
下列反应的离子方程式正确的是
A.Fe与稀H2SO4反应:2Fe + 6H+ = 2Fe3+ + 3H2↑
B.硫酸铜溶液与氢氧化钡溶液反应 :Ba2++ SO42― = BaSO4↓
C.氧化铜溶于硫酸:O2―+2H+= H2O
D.NaCl溶液与AgNO3溶液反应:Ag++Cl―= AgCl↓
难度: 中等查看答案及解析
-
在溶液中,能大量共存的离子组是
A.Na+、Mg2+、SO42、OH B.Na+、Ba2+、Cl、SO42
C.Cu2+、Ca2+、Cl、NO3 D.Ag+、K+、NO3、Cl
难度: 中等查看答案及解析