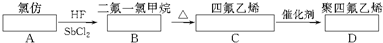
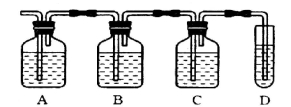
-
下列式子表示的物质一定为纯净物的是
A.C2H6 B.C4H10 C.C5H12 D.C7H16
难度: 中等查看答案及解析
-
关于原电池和电解池的叙述正确的是
A.原电池失去电子的电极称为阴极
B.电解池的阳极、原电池的负极都发生氧化反应
C.原电池的两极,一定要由活动性不同的两种金属组成
D.电解时电解池的阳极一定是阴离子放电
难度: 中等查看答案及解析
-
用惰性电极电解饱和Na2CO3溶液,若保持温度不变,则一段时间后
A.溶液的pH变大
B.c(Na+)与c (CO32-)的比值变大
C.溶液浓度变大,有晶体析出
D.溶液浓度不变,有晶体析出
难度: 中等查看答案及解析
-
若在铜片上镀银时,下列叙述正确的是
①将铜片接在电池的正极上,②将银片接在电源的正极上,③在铜片上发生的反应是:Ag++e-=Ag,④在银片上发生的反应是:4OH--4e-=O2+2H2O,⑤需用CuSO4溶液,⑥需用AgNO3溶液作电解液
A.①③⑥ B.②③⑥ C.①④⑤ D.②③④⑥
难度: 中等查看答案及解析
-
下列有机物的命名正确的是
A.3,3-二甲基丁烷
B.2,2-二甲基丁烷
C.2-乙基丁烷
D.2,3,3-三甲基丁烷
难度: 中等查看答案及解析
-
10 mL某烷烃,在50 mL O2中充分燃烧,得液态水和体积35 mL的混合气体(所有气体体积在同温、同压下测定),则该烃是
A.甲烷 B.乙烷 C.丙烷 D.丁烷
难度: 中等查看答案及解析
-
下列有关电化学原理的说法中,错误的是
A.在现实生活中,电化学腐蚀要比化学腐蚀严重的多,危害更大
B.在铜的精炼装置中,通常用粗铜作作阳极,精铜作阴极
C.氯碱工业,主要依托电解熔融的氯化钠来制取工业上重要的化工原料烧碱和氯气
D.可充电的电池称“二次电池”,在充电时,是将电能转变成化学能,在放电时,又将化学能转化成电能
难度: 中等查看答案及解析
-
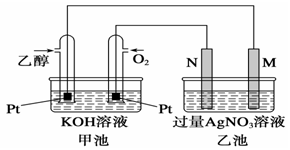
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:2CH3OH + 3O2 + 4OH—
2CO32— + 6H2O,则下列说法错误的是
A.放电时CH3OH参与反应的电极为正极
B.充电时电解质溶液的pH逐渐增大
C.放电时负极的电极反应为:CH3OH-6e-+8OH- = CO32— + 6H2O
D.充电时每生成1 mol CH3OH转移6 mol电子
难度: 中等查看答案及解析
-
下图
为直流电源,
为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为电镀槽.接通电路后发现
上的c点显红色,为实现铁上镀锌,接通
后,使c、d两点短路.下列叙述正确的是
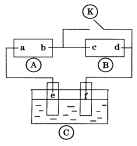
A.a为直流电源的负极
B.c极发生的反应为2H++2e-=H2↑
C.f电极为锌板
D.e极发生还原反应
难度: 中等查看答案及解析
-
已知正丁烷的二氯代物有6种同分异构体,则其八氯代物的同分异构体有
A.6种 B.8种 C.10种 D.12种
难度: 中等查看答案及解析
-
下列有关说法不正确的是
A.由乙烯分子组成和结构推测含一个碳碳双键的单烯烃通式为CnH2n
B.乙烯的电子式为:
C.从乙烯与溴发生加成反应生成1,2—二溴乙烷可知乙烯分子的碳碳双键中有一个键不稳定,易发生断裂
D.乙烯在空气中燃烧的现象与甲烷不同的原因是乙烯中含碳量高
难度: 中等查看答案及解析
-
既可用来除去甲烷中的丙烯,又可用来鉴别乙烷与丁烯的方法是
A.把气体通入足量液溴中
B.在导管口处点燃
C.一定条件下与H2发生加成反应
D.把气体通入足量溴水中
难度: 中等查看答案及解析
-
烷烃
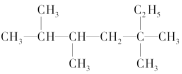 是单烯烃R和H2发生加成反应后的产物,则R可能的结构有
是单烯烃R和H2发生加成反应后的产物,则R可能的结构有A.4种 B.7种 C.6种 D.5种
难度: 中等查看答案及解析
-
某溶液中含有两种溶质NaCl和H2SO4,它们的物质的量之比为3:1。用石墨电极电解该混合溶液时,根据电极产物,可明显分为三个阶段。下列叙述不正确的是
A.阴极自始至终只析出H2
B.阳极先析出Cl2,后极出O2
C.电解最后阶段为电解水
D.溶液pH不断增大,最后为7
难度: 中等查看答案及解析
-
据报道,我国拥有完全自主产权的氢氧燃料电池车将在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解质溶液为KOH溶液。下列有关该电池的叙述不正确的是
A.正极反应式为:O2+2H2O+4e-=4OH-
B.工作一段时间后,电解质溶液中KOH的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2=2H2O
D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
难度: 中等查看答案及解析
-
下列关于烷烃与烯烃的性质及反应类型的对比中正确的是
A.烷烃只含有饱和键,烯烃只含有不饱和键
B.烷烃不能发生加成反应,烯烃只能发生加成反应
C.通式为CnH2n+2的一定是烷烃,通式为CnH2n的一定是烯烃
D.烷烃与烯烃相比,发生加成反应的一定是烯烃
难度: 中等查看答案及解析
-
一种有机物的化学式为C4H4,分子结构如图所示,将该有机物与适量氯气混合后光照,生成的卤代烃的种类共有
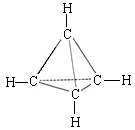
A.2 B.4 C.5 D.6
难度: 中等查看答案及解析
-
通以相等的电量,分别电解等浓度的硝酸银和硝酸亚汞(亚汞的化合价为+1)溶液,若被还原的硝酸银和硝酸亚汞的物质的量之比n硝酸银︰n硝酸亚汞=2︰1,则下列表述正确的是
A.在两个阴极上得到的银和汞的物质的量之比n银︰n汞=2︰1
B.在两个阳极上得到的产物的物质的量不相等
C.硝酸亚汞的化学式为HgNO3
D.硝酸亚汞的化学式为Hg2(NO3)2
难度: 中等查看答案及解析
-
下图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。下列有关描述错误的是
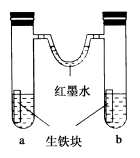
A.生铁块中的碳是原电池的正极
B.红墨水柱两边的液面变为左低右高
C.两试管中相同的电极反应式是:Fe-2e-=Fe2+
D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
难度: 中等查看答案及解析
-
下列实验不能获得成功的是
①用甲烷气体通入碘水制碘甲烷
②甲烷和溴蒸气混合光照制取纯净的一溴甲烷
③用洒精灯加热甲烷气体制取炭黑和氢气
A.只有① B.只有③ C.只有② D.①②③
难度: 中等查看答案及解析
-
按如图甲装置进行实验,若乙中横坐标x表示流入电极的电子的物质的量,下列叙述不正确的是
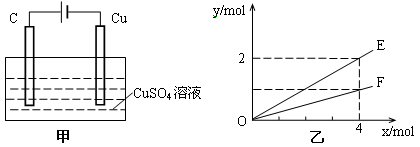
A.E表示生成铜的物质的量
B.E表示反应消耗水的物质的量
C.F表示生成硫酸的物质的量
D.F表示反应生成氧气的物质的量
难度: 中等查看答案及解析
-
下列各组物质之间的化学反应,反应产物一定为纯净物的是
A.
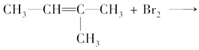
B.CH2===CH—CH2—CH3+HCl
C.CH3—CH===CH2+H2O
D.nCH2===CH2+nCH2===CH—CH3
难度: 中等查看答案及解析
-
下列有机物不是同一种物质的是
A.
和
B.CH2=CH—CH=CH2和
C.C(CH3)3C(CH3)3和CH3(CH2)3C(CH3)3
D.
和
难度: 中等查看答案及解析
-
某有机物在氧气里充分燃烧,生成CO2和H2O的质量比为22:9,由此可得出的正确的结论是
A.碳、氢、氧的原子个数比为1:2:3
B.碳、氢的原子个数比为1:1
C.该有机物中肯定不含氧元素
D.不能判断该有机物中是否含有氧元素
难度: 中等查看答案及解析
-
下列描述中,不符合生产实际的是
A.电解法精炼粗铜,用粗铜作阳极
B.电解熔融的氧化铝制取金属铝,用铁作阳极
C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极
D.在镀件上电镀锌,用锌作阳极
难度: 中等查看答案及解析