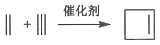
-
分类是化学学习与研究的常用方法,下列分类正确的是( )
A. 混合物:水玻璃、氯水、福尔马林、聚乙烯
B. CO2、NO2、P2O5均为酸性氧化物,Na2O、Na2O2均为碱性氧化物
C. 根据能否发生丁达尔效应,将分散系分为溶液、胶体和浊液
D. 根据溶液导电能力强弱,将电解质分为强电解质和弱电解质
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 用氨水可以鉴别Al3+、Mg2+和Ag+
B. 用水鉴别乙醇、乙酸乙酯和溴苯
C. 除去乙酸乙酯中的乙酸:用NaOH溶液,然后分液
D. 除去乙烷中少量的乙烯:光照下通入Cl2,生成液态CH2Cl-CH2Cl,气液分离
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列说法正确的是 ( )
A. 标准状况下11.2L的CHCl3中含有的分子数为0.5 NA
B. 78g Na2S和Na2O2的混合物中含有阴离子数大于6.02×1023
C. 常温下,42g乙烯和丙烯的混合气体中碳原子数目一定为3NA
D. 将100 mL0.1 mol·L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA
难度: 困难查看答案及解析
-
下列说法正确的是( )
A. 石油的裂化、煤的气化与液化都属于化学变化,而石油的分馏与煤的干馏都属于物理变化
B.
 的系统命名法为2,5-二甲基-4-乙基己烷
的系统命名法为2,5-二甲基-4-乙基己烷C. 总质量一定时,乙酸和甲醛无论以何种比例混合,完全燃烧消耗氧气的量相等
D. 油脂、淀粉、蛋白质等高分子化合物都属于混合物,一定条件下均可发生水解
难度: 中等查看答案及解析
-
常温下,下列各组离子可能大量共存的是( )
A. 加入铝粉能放出H2的溶液:K+、NH4+、SO42﹣、NO3﹣
B. 0.1mol/L FeCl3溶液中:Al3+、SO42﹣、I﹣、SCN-
C. 由水电离产生的c(H+)=1×10﹣13mol/L的溶液中:S2﹣、SO32﹣、Na+、K+
D. 使pH 试纸变红的溶液中:Fe2+、Mg2+、NO3﹣、Cl﹣
难度: 困难查看答案及解析
-
向含有c(FeCl3)=0.2mol·L-1、c(FeCl2)=0.1mol·L-1的混合溶液中滴加稀NaOH溶液,可得到一种黑色分散系,其中分散质粒子是直径约为9.3nm的金属氧化物,下列有关说法中正确的是( )
A. 该分散系的分散质为Fe2O3
B. 加入NaOH时发生的反应可能为:Fe2++2Fe3++8OH==Fe3O4+4H2O
C. 在电场作用下,阴极附近分散系黑色变深,则说明该分散系带正电荷
D. 可用过滤的方法将黑色金属氧化物与Na+分离开
难度: 中等查看答案及解析
-
已知:乙醇可被强氧化剂(如酸性高锰酸钾)氧化为乙酸。
 可经三步反应制取
可经三步反应制取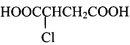 ,第二步的反应类型是( )
,第二步的反应类型是( )A. 水解反应 B. 消去反应 C. 氧化反应 D. 加成反应
难度: 困难查看答案及解析
-
根据下列实验操作和现象所得到的结论正确的是
选项
实验操作和现象
实验结论
A
将电石与水反应产生的气体通入溴水中,溶液褪色
说明有乙炔生成
B
将苯、液溴、铁粉混合物反应产生的气体通入到AgNO3溶液中有淡黄色沉淀产生
说明反应为取代反应
C
向20%蔗糖溶液中加入少量稀H2SO4,加热;再加入银氨溶液;未出现银镜
说明蔗糖未水解
D
将溴乙烷与NaOH的乙醇溶液共热产生的气体通入到酸性KMnO4溶液中,溶液褪色
不能说明有乙烯生成
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是( )
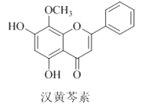
A. 汉黄芩素的分子式为C16H13O5
B. 该物质中所有原子一定共面
C. 1 mol该物质与溴水反应,最多消耗2 mol Br2
D. 与足量H2发生加成反应后,该分子中官能团的种类减少1种
难度: 困难查看答案及解析
-
把500 mL NH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含amol NaOH的溶液恰好完全反应;另取一份加入含b moI HC1的溶液恰好不再放出气体。则该混合溶液中c(Na+)为 ( )
A.
B.
C.
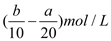 D.
D. 难度: 困难查看答案及解析
-
羟氨(NH2OH)是一种还原剂。将16.00mL 0.05mol/L的羟氨酸性溶液与足量硫酸铁在煮沸条件下反应,生成的Fe2+又恰好被24.00mL 0.02mol/L的酸性KMnO4溶液所氧化。在上述反应中,羟氨的氧化产物为( )
A. NO2 B. NO C. N2O D. N2
难度: 困难查看答案及解析
-
芳香族有机物的分子式为C11H14O2,能与NaOH溶液反应,苯环上只有两个取代基,其中有一个是-C4H9,满足条件的该有机物有( )
A. 12种 B. 24种 C. 18种 D. 6种
难度: 困难查看答案及解析
-
下列离子方程式书写正确的是( )
A. Ca(HCO3)2 溶液中滴入过量NaOH溶液:HCO3- +Ca2++ OH- =CaCO3↓+H2O
B. 向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全 Ba2++OH-+H++SO42-=BaSO4↓+H2O
C. 向NaAlO2 溶液中通入过量的 CO2:CO2 +2H2O+ A1O2- =Al(OH)3↓+ HCO3-
D. 向Ca(ClO)2 溶液中通入过量的 SO2 :C1O- +SO2+H2O = HClO + HSO3-
难度: 困难查看答案及解析
-
卤代烃与金属镁在无水乙醚中反应,可得格氏试剂 R—MgX,它可与醛、酮等羰基化合物加成,所得产物经水解可以得到醇,这是某些复杂醇的合成方法之一。现欲合成(CH3)3C—OH,下列所选用的卤代烃和羰基化合物的组合正确的是 ( )

A. 丙酮和一氯甲烷 B. 甲醛和 1-溴丙烷
C. 乙醛和氯乙烷 D. 甲醛和2-溴丙烷
难度: 困难查看答案及解析
-
已知Br2+2Fe2+===2Fe3++2Br-。向100mLFeBr2溶液中通入标况下氯气6.72L,氯气全部被还原,测得溶液c(Br-)=c(Cl-),原溶液中FeBr2溶液的浓度(mol·L-1)为( )
A. 2 B. 4 C. 2.5 D. 6
难度: 困难查看答案及解析
-
关于下列三种化合物的说法正确的是( )
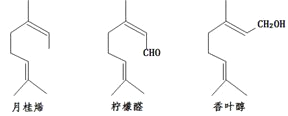
A. 都可以发生加成反应、酯化反应、氧化反应 B. 均不存在顺反异构体
C. 可以用金属钠和银氨溶液进行鉴别 D. 不同化学环境的氢原子均为7 种
难度: 中等查看答案及解析
-
化合物A相对分子质量为136,分子式为C8H8O2。A的核磁共振氢谱有4个峰且面积之比为1∶2∶2∶3,A分子中只含一个苯环且苯环上只有一个取代基,其红外光谱与核磁共振氢谱如下图。关于A的下列说法中,正确的是( )
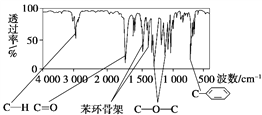
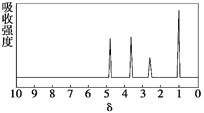
A. 符合题中A分子结构特征的有机物只有1种
B. A属于酯类化合物,在酸性条件下水解产物遇FeCl3溶液显紫色
C. A在一定条件下可与4 mol H2发生加成反应
D. 与A属于同类化合物的同分异构体只有2种
难度: 困难查看答案及解析