-
下列有关物质结构的表述正确的是
A.次氯酸的电子式
B.硫原子的最外层电子数为6
C.二氧化硅的分子式 SiO2 D.钠离子的结构示意图
难度: 简单查看答案及解析
-
下列表示对应化学反应的离子方程式正确的是
A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I 2+6OH-
B.向NH4HCO3溶液中加少量NaOH溶液并加热:NH4++OH-
NH3↑+H2O
C.将少量二氧化硫气体通入冷氨水中:SO2+NH3·H2O=HSO3-+NH4+
D.用稀硝酸洗涤试管内壁的银镜:3Ag+4H++NO3-=3Ag++NO↑+2H2O
难度: 简单查看答案及解析
-
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.2NA
B.常温常压下,18g H2O含有的电子总数为10NA
C.标准状况下,11.2LSO3中含有分子的数目为0.5NA
D.常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA
难度: 简单查看答案及解析
-
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用相同的是
A. 2H2O=2H2+O2↑ B.4Fe(OH)2+O2+2H2O=4Fe(OH)3
C.2F2+2H2O=4HF+O2 D.2Al+2NaOH+2H2O=2NaAlO2+3H2↑
难度: 简单查看答案及解析
-
下列说法中正确的是 ( )
A.次外层电子数是2或8的原子一定不是副族元素
B.离子化合物中不存在共价键
C.质量数就是原子的相对原子质量
D.核外电子排布相同的微粒,一定具有相同的化学性质
难度: 简单查看答案及解析
-
已知X、Y、Z、T四种金属元素,X、Y在反应时各放出一个电子形成稳定结构所吸收的能量是Y>X; 对应最高价氧化物的水化物的碱性是T>X; 原子序数T>Z, 其稳定结构的离子核外电子数相等,而其离子半径是Z>T。四种元素的金属性从强到弱排列顺序正确的是 ( )
A. Z、T、X、Y、 B. Y、X、Z、T C. X、Y、T、Z D. Y、X、T、Z
难度: 简单查看答案及解析
-
下列有关物质性质的比较正确的是 ( )
①同主族元素的单质从上到下,非金属性减弱,熔点增高
②元素的最高正化合价在数值上等于它所在的族序数
③同周期主族元素的原子半径越小,越难失去电子
④元素的非金属性越强,它的气态氢化物水溶液的酸性越强.
⑤还原性:S2->Se2->Br->Cl-⑥酸性:HClO4>H2SO4>H3PO4>H2SiO3
A.①③ B.②④ C.③⑥ D.⑤⑥
难度: 简单查看答案及解析
-
SF6是一种优良的绝缘气体,分子结构中只存在S-F键。已知:1molS(s)转化为气态硫原子吸收能量280kJ,断裂1molF-F 、S-F键需吸收的能量分别为160kJ、330kJ。则S(s)+3F2(g)=SF6(g)的反应热△H为
A. -1780kJ/mol B. +1220 kJ/mol C. -1220 kJ/mol D. +1780 kJ/mol
难度: 简单查看答案及解析
-
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水” 电池在海水中放电时的有关说法正确的是:
A.正极反应式:Ag+Cl--e-=AgCl
B.每生成1 mol Na2Mn5O10转移1 mol电子
C.Na+不断向“水”电池的正极移动
D. AgCl是还原产物
难度: 简单查看答案及解析
-
100mL6mol/L硫酸跟过量锌粒反应,在一定温度下,为了减慢反应进行的速率,但又不影响生成氢气的总量。可向反应物中加入适量的
A.醋酸钠(固体) B.3mol/L硫酸 C.碳酸钾溶液 D.硫酸铵(固体)
难度: 简单查看答案及解析
-
用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积)。下列分析正确的是
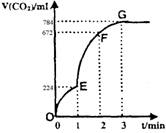
A.OE段表示的平均速率最快
B.EF段,用盐酸表示该反应的平均反应速率为0.04mol/(L·min)
C.OE、EF、FG三段中,该反应用二氧化碳表示的平均反应速率之比为2:6:7
D.G点表示收集的CO2的量最多
难度: 简单查看答案及解析
-
将A与B的混合气体1 mol放入容积为2 L的密闭容器内,在一定条件下发生反应:2A(g)+3B(g)
C(g)+ 2D(g) ,经过4min达到平衡,此时容器内的压强是反应前的3/5,以各气体的浓度变化表示的反应速率正确的是( )
A.vA=0.025 mol·(L·min)-1 B.vB=0.150mol·(L·min)-1
C.vC=0.0125mol·(L·min)-1 D.vD=0.050mol·(L·min)-1
难度: 简单查看答案及解析
-
在一定温度体积不变的容器中,对可逆反应
的下列叙述中不能说明反应已达到平衡的是( )
A C生成的速率与C分解的速率相等
B单位时间内生成amolA,同时生成3amolC
C容器内各气体的百分含量不再变化
D混合气体的平均相对分子质量不再变化
难度: 简单查看答案及解析
-
分子式为C10H14的单取代芳香烃,其可能的结构有
A.2种 B.4种 C.6种 D.8种
难度: 简单查看答案及解析
-
下列说法正确的是
A.蔗糖及其水解产物均能发生银镜反应
B.用溴水不能鉴别苯和甲苯
C.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
D.用甘氨酸(
)和丙氨酸(
)缩合最多可形成3种二肽
难度: 简单查看答案及解析
-
向27.2Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO 和Cu(NO3)2。在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法正确的是
A.Cu与Cu2O 的物质的量之比为1:1
B.硝酸的物质的量浓度为2.6mol/L
C.产生的NO的体积为4.48L
D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol
难度: 简单查看答案及解析