-
现有失去标签的CaCl2、AgNO3、HCl和Na2CO3四瓶溶液.为了确定这四种溶液成分,将他们编号为A、B、C、D后进行化学实验.实验记录如下:
根据上述实验填空:实验顺序 实验内容 实验现象 ① A+B 无现象 ② B+D 有气体放出 ③ C+B 有沉淀生成 ④ A+D 有沉淀生成
(1)A、B、C三瓶溶液分别是(用化学式表示):______、______、______.
(2)写出B和D反应的离子方程式:______.
(3)说明A和B不发生反应的理由:______.难度: 中等查看答案及解析
-
氯化钠溶液在生产、生活中都有广泛的用途.现配置1L 0.2mol•L-1NaCl溶液.请回答问题.
实验步骤 有关问题 (1)计算并称量 需要NaCl的质量为______ g (2)溶解 为加速溶解,可进行的操作是______ (3)转移 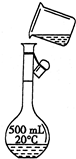
指出示意图中的两处错误:
错误1:______
错误2:______(4)定容 若俯视容量瓶刻度线,定容后会造成所配溶液的物质的量浓度______(填“偏高”“偏低”或“无影响”) 难度: 中等查看答案及解析
-
有一种褐铁矿主要成分是Fe2O3,所含杂质不溶于水和酸.某研究性学习小组的同学们利用一小块样品,进行了以下实验.
(1)检验矿物样品中是否有Fe3+
实验用品:锤子、研钵、烧杯、玻璃棒、漏斗、铁架台、滤纸、试管、胶头滴管
实验步骤:
①取样:将样品用锤子敲碎,再在研钵中研细备用.
②溶【解析】
将样品粉末倒入烧杯,加入______,用玻璃棒充分搅拌.
③______(填操作名称).
④检验:取少许溶液,______.
实验现象:______.
实验结论:矿物样品中含有Fe3+.
(2)制备氢氧化亚铁
①为了得到亚铁盐的溶液,同学们在剩余的溶液中加入过量的某种固体试剂,该试剂是(填化学式)______,反应的离子方程式是______.
②对于①中过量的固体试剂是否需要除去,同学们产生了两种观点.
甲组:认为需要过滤. 乙组:认为不需要过滤.
你支持的是组______(填“甲”或“乙”),理由是______
③同学们在新制得的亚铁盐溶液中加入适量新制的氢氧化钠溶液,制出的氢氧化亚铁呈______色.为使试管中的氢氧化亚铁保存的时间更长,请在右图中画出你的设计(可以加必要的文字说明).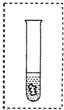
难度: 中等查看答案及解析
-
金属及其化合物的种类很多,我们可以按照“金属单质、金属氧化物、金属氢氧化物、盐”的类别进行研究.以下是某种金属及其化合物之间的转化关系(“→”所指的转化都是一步完成)

(1)写出以下物质的化学式:A______,C______.
(2)A与水反应的离子方程式:______.
(3)若B为呼吸面具中的供养剂,其供养时主要反应的化学方程式:______.
(4)写出一种“C→D”转化的化学方程式:______.难度: 中等查看答案及解析
-
储氢纳米碳管的研制成功体现了科技的进步.用电弧法合成的纳米管伴有大量的杂质--碳纳米颗粒.这种碳纳米颗粒可用氧化气化法提纯.其反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、K2SO4、Cr2(SO4)3和H2O七种.
(1)已知K2Cr2O7在反应中得到电子,则配平后的该氧化还原反应的方程式为:______.
(2)H2SO4在上述反应中表现出的性质是(填选项序号)______.
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(3)上述反应中的还原剂是(填化学式)______,还原产物是(填化学式)______.
(4)若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为______.难度: 中等查看答案及解析
-
某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出),其中E为白色沉淀,I为红褐色沉淀.(此转化关系中所用的试剂都是足量的)
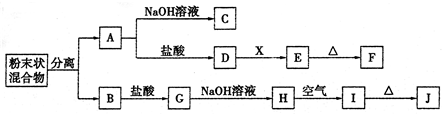
(1)写出下列物质的化学式:F______,G______.
(2)将混合物中两种金属分离开的最简单的方法是______.
(3)D→E的转化中,加入过量的X可能是______.
A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液
(4)写出下列转化的化学方程式:
A→C:______;
H→I:______.难度: 中等查看答案及解析
-
将3.84g Fe和Fe2O3的混合物溶于120mL的盐酸,刚好完全反应,生成0.03mol H2,若反应后的溶液中无Fe3+,且溶液体积不变,试求:
(1)原混合物中Fe2O3和Fe的质量分别为多少?
(2)原盐酸的物质的量浓度.难度: 中等查看答案及解析
-
某研究型学习小组为测定镁和铝的混合物中铝的质量分数,称取该混合物a g,溶于200mL 5mol/L HCl溶液中,共收集到标准状况下的氢气3.36L.
(1)a 的取值范围是______.
(2)向反应后所得溶液中逐渐加入4mol/L的NaOH溶液,当沉淀质量达到最大值时,加入的NaOH溶液的体积是______mL,沉淀的最大质量是______g.(用含a 的代数式表示)
(3)继续加入NaOH溶液至沉淀不再发生变化时,过滤、洗涤并灼烧沉淀至恒重,所得残余固体的质量仍为a g,计算原混合物中铝的质量分数(写出计算过程).难度: 中等查看答案及解析