-
将下列各组物质按酸、碱、盐分类顺序排列正确的是
A.硫酸,纯碱,石灰石 B.硝酸,烧碱,胆矾
C.醋酸,碱式碳酸铜,醋酸钠 D.盐酸,熟石灰,苛性钠
难度: 中等查看答案及解析
-
下列各组混合物中,按照溶解、过滤、蒸发的操作顺序能将它们分离开的是( )
A.氧化铜和炭粉 B.硝酸钾和氯化钠
C.水和酒精 D.碳酸钠和硫酸钡
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A.氢氧化钠的摩尔质量是40 g
B.1 mol NaOH的质量是40 g/mol
C.1 g H2和1 g N2所含分子数相等
D.等质量的N2 . CH4 . CO. H2O中,CH4所含分子数最多
难度: 中等查看答案及解析
-
下列实验操作中错误的是( )
A.称氢氧化钠时,不能直接称量,要放在称量纸上
B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D.过滤时,玻璃棒的末端应轻轻靠在三层的滤纸上
难度: 中等查看答案及解析
-
下列实验装置与实验操作正确的是
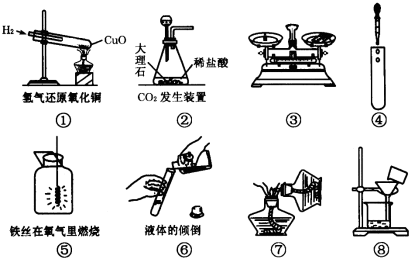
A.①④⑤ B.②③⑧ C.④⑥ D.⑤⑦
难度: 中等查看答案及解析
-
下列离子方程式正确的是( )
A.澄清的石灰水与盐酸反应 Ca(OH) 2 + 2H+ = Ca2+ + 2H2 O
B.钠与水的反应 Na + 2H2 O = Na+ + 2O
H- + H2↑
C.铜片插入硝酸银溶液 Cu + Ag+ = Cu2+ + Ag
D.大理石溶于醋酸 CaCO3 + 2 CH3COOH = Ca2+ + 2 CH3COO- + H2O + CO2↑
难度: 中等查看答案及解析
-
据中央电视台报道,近年我国的一些沿江城市多次出现大雾天气,致使高速公路关闭,航班停飞,雾属于下列哪种分散系( )
A.乳浊液 B.溶液 C.胶体 D.悬浊液
难度: 简单查看答案及解析
-
在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺
序是( )
A.p(Ne)>p(H2)>p(O2) B.p(O2)>p(Ne)>p(H2)
C.p(H2)>p(O2)>p(Ne) D.p(H2)>p(Ne)>p(O2)
难度: 中等查看答案及解析
-
某混合物的水溶液,只可能含有以下离子中的若干:NH4+ 、Cl-、Mg2+、Ba2+、K+、CO32 -、SO42 -,现取三份100 mL溶液进行如下实验:① 第一份加入AgNO3溶液有沉淀产生;② 第二份加足量NaOH溶液加热后,收集到气体0.04 mol;③ 第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥,沉淀质量2.33 g。根据上述实验,以下推测正确的是
A.K+一定不存在
B.该溶液中含CO32 -离子的浓度为0.1 mol/L
C.Cl-可能存在
D.Ba2+一定不存在,Mg2+可能存在
难度: 困难查看答案及解析
-
用1kg溶剂中所含溶质的物质的量表示的溶液的浓度叫质量物质的量浓度,其单位是mol/kg。某物质的溶液的质量分数为20%,质量物质的量浓度为2.358mol/kg,则该物质可能为
A.NaHCO3 B.CaCO3 C.KHCO3 D.Na2CO3
难度: 中等查看答案及解析
-
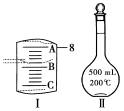
如图所示为“铁链环”结构,图中两环相交部分A、B、C、D表示物质间的反应。下列对应部分反应的离子方程式书写不正确的是( )

A.Cl2+2OH-===Cl-+ClO-+H2O
B.Cu2++2OH-===Cu(OH)2↓
C.Cu2++SO42-+Ba2++2OH-===BaSO4↓+Cu(OH)2↓
D.OH-+HCO===H2O+CO
难度: 中等查看答案及解析
-
水溶液中能大量共存的一组离子是
A.Na+、Ag+、Cl-、CO32- B.H+、Na+、Fe2+、MnO4-
C.K+、Ca2+、Cl-、NO3- D.K+、NH4+、OH-、SO42-
难度: 中等查看答案及解析
-
某金属的硝酸盐受热分解生成NO2、O2和该金属的氧
化物。已知NO2和O2的分子个数比为4:1,则在分解过程中该金属的化合价将( )。
A.无法确定 B.升高 C.不变 D.降低
难度: 中等查看答案及解析
-
在热的稀硫酸溶液中溶解了11.4g FeSO4,当加入50mL 0.5mol·L-1KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3溶液也完全反应,并有NxOy气体逸出,则该NxOy是( )
A.N2O B.NO C.N2O3 D.NO2
难度: 中等查看答案及解析
-
已知Q与R的摩尔质量之比为9:22,在反应X+2Y=2Q+R中,当1.6g X与Y完全反应后,生成4.4g R,则参与反应的Y和生成物Q的质量之比为( )
A.46 : 9 B.32 : 9 C.23 : 9 D.16 : 9
难度: 中等查看答案及解析
-
向0.1mol·L-1NaOH溶液中通入过量CO2后,溶液中存在的主要离子是( )
A.Na+、CO32- B.Na+、HCO3- C. HCO3- CO32- D.Na+、OH-
难度: 中等查看答案及解析