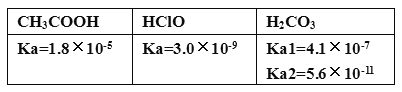-
下表是25 ℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是
A. 相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B. 碳酸钠溶液中滴加少量氯水的离子方程式H2O+2CO32-+Cl2===2HCO3-+Cl-+ClO-
C. 向0.1 mol·L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=9:5,此时溶液pH=5
D. 向浓度均为1×10-3mol·L-1的KCl和K2CrO4混合液中滴加1×10-3mol· L-1的AgNO3溶液,CrO42-先形成沉淀
-
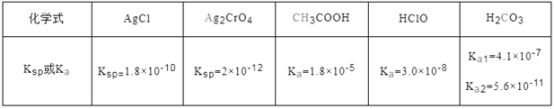
下表是25℃ 时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是( )

A.相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B.碳酸钠溶液中滴加少量氯水,反应的离子方程式为 +Cl2+H2O=
+Cl2+H2O= +Cl-+ClO-
+Cl-+ClO-
C.向0.1mol·L-1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液pH=5
D.向浓度均为1×10-3mol·L-1的KCl和K2CrO4混合液中滴加1×10-3mol·L-1的AgNO3溶液, 先形成沉淀
先形成沉淀
-
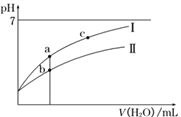
已知:25℃时某些弱酸的电离平衡常数。下面图像表示常温下稀释CH3COOH,HClO两种酸的稀溶液时,溶液pH随加水量的变化,下列说法正确的是( )
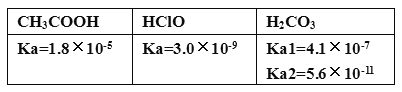
A. 相同浓度CH3COONa和NaClO的混合液中,各离子浓度大小关系为:c(Na+) > c(ClO-) > c(CH3COO-)> c(OH-) > c(H+)
B. 向NaClO溶液中通少量CO2的离子方程式为:2ClO- + CO2 + H2O = 2HClO + CO32-
C. 图像中a、c两点处的溶液中 相等(HR代表CH3COOH或HClO)
相等(HR代表CH3COOH或HClO)
D. 图像中a点对应酸的总浓度大于b点酸的总浓度
-
化学平衡常数(K)、弱酸的电离平衡常数(Ka)、难溶物的溶度积常数(KSP)是判断物质性质或变化的重要的平衡常数.下列关于这些常数的说法中,正确的是( )
A. 平衡常数的大小与温度、浓度、压强、催化剂等有关
B. KSP(AgCl)>KSP(AgI),由此可以判断AgCl(s)+I-=AgI(s)+Cl-(aq)能够发生
C. 当温度升高时,弱酸的电离常数Ka变小
D. Ka(HCN)<Ka(CH3COOH),说明相同物质的量浓度时,氢氰酸的酸性比醋酸强
-
化学平衡常数 、电离常数(Ka、Kb)、溶度积常数
、电离常数(Ka、Kb)、溶度积常数 等常数是表示、判断物质性质的重要常数,下列关于这些常数的说法中,正确的是
等常数是表示、判断物质性质的重要常数,下列关于这些常数的说法中,正确的是
A. 当温度升高时,弱酸、弱碱的电离常数(Ka、Kb)和溶度积常数 一定均变大
一定均变大
B.  说明相同物质的量浓度时,氢氰酸的酸性比醋酸的强
说明相同物质的量浓度时,氢氰酸的酸性比醋酸的强
C. 向氯化钡溶液中加入等体积同浓度的碳酸钠和硫酸钠溶液,先产生 沉淀,则
沉淀,则
D. 化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关
-
化学平衡常数(K)、电离常数(Ka、Kb)、溶度积常数(Ksp)等常数是表示、判断物质性质的重要常数,下列关于这些常数的说法中,正确的是
A.当温度升高时,弱酸、弱碱的电离常数(Ka、Kb)均变大
B.Ka(HCN)<Ka(CH3COOH)说明相同物质的量浓度时,氢氰酸的酸性比醋酸的强
C.向氯化钡溶液中加入等体积同浓度的碳酸钠和硫酸钠溶液,先产生BaSO4沉淀,则Ksp(BaSO4)>Ksp(BaCO3)
D.化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关
-
已知,25℃时有关弱酸的电离平衡常数如下:

则下列有关说法正确的是( )
A.等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3 )>pH(CH3COONa)
B.a mol·L-1 HCN溶液与b mol·L-1 NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则b一定大于a
C.向冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度、pH均先增大后减小
D.等物质的量NaHCO3和Na2CO3的混合溶液中,一定存在: c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
-
化学平衡常数(K)电离常数(Ka、Kb)、溶度积常数(Ksp)等常数是表示、判断物质性质的重要常数,下列关于这些常数的说法中,正确的是
A.当温度升高时,弱酸、弱碱的电离常数(Ka、Kb)均变大
B.Ka(HCN)<Ka(CH3COOH)说明相同物质的量浓度时,氢氰酸的酸性比醋酸的强
C.向氯化钡溶液中加入等体积同浓度的碳酸钠和硫酸钠溶液,先产生BaSO4沉淀,则Ksp(BaSO4)>Ksp(BaCO3)
D.化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关
-
化学平衡常数(K)电离常数(Ka、Kb)、溶度积常数(Ksp)等常数是表示、判断物质性质的重要常数,下列关于这些常数的说法中,正确的是
A.当温度升高时,弱酸、弱碱的电离常数(Ka、Kb)均变大
B.Ka(HCN)<Ka(CH3COOH)说明相同物质的量浓度时,氢氰酸的酸性比醋酸的强
C.向氯化钡溶液中加入等体积同浓度的碳酸钠和硫酸钠溶液,先产生BaSO4沉淀,则Ksp(BaSO4)>Ksp(BaCO3)
D.化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关
-
已知K、Ka、Kw、Ksp分别表示化学平衡常数、弱酸的电离平衡常数、水的离子积常数、难溶电解质的溶度积常数。
(1)有关上述常数的说法正确的是___。
 它们都能反映一定条件下对应变化进行的程度
它们都能反映一定条件下对应变化进行的程度
 它们的大小都随温度的升高而增大
它们的大小都随温度的升高而增大
 常温下,CH3COOH在水中的Ka大于在饱和CH3COONa溶液中的Ka
常温下,CH3COOH在水中的Ka大于在饱和CH3COONa溶液中的Ka
(2)已知25℃时CH3COOH和NH3·H2O电离常数相等,则该温度下CH3COONH4溶液中水电离的H+浓度为___,溶液中离子浓度大小关系为___。
(3)氯化铝溶液蒸干、灼烧后得到的固体物质是___。
(4)泡沫灭火器的反应原理(硫酸铝溶液与小苏打)___。(写离子方程式)
(5)已知在25℃时Ksp[Mg(OH)2]=3.2×10-11,Ksp[Cu(OH)2]=2.2×10-20。25℃时,向浓度均为0.02mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入NaOH溶液,先生成沉淀___(填化学式);当两种沉淀共存时, =___。
=___。