常温下,用0.100 0 mol·L-1的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是
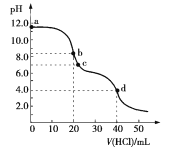
A.a点溶液呈碱性的原因用离子方程式表示为C+2H2O
H2CO3+2OH-
B.c点处的溶液中:c(Na+)-c(Cl-)=c(HC)+2c(C
)
C.滴定过程中使用甲基橙作为指示剂比酚酞更准确
D.d点处溶液中水电离出的c(H+)大于b点处
高三化学多选题中等难度题
常温下,用0.100 0 mol·L-1的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是

A.a点溶液呈碱性的原因用离子方程式表示为C+2H2O
H2CO3+2OH-
B.c点处的溶液中:c(Na+)-c(Cl-)=c(HC)+2c(C
)
C.滴定过程中使用甲基橙作为指示剂比酚酞更准确
D.d点处溶液中水电离出的c(H+)大于b点处
高三化学多选题中等难度题
常温下,用0.100 0 mol·L-1的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是

A.a点溶液呈碱性的原因用离子方程式表示为C+2H2O
H2CO3+2OH-
B.c点处的溶液中:c(Na+)-c(Cl-)=c(HC)+2c(C
)
C.滴定过程中使用甲基橙作为指示剂比酚酞更准确
D.d点处溶液中水电离出的c(H+)大于b点处
高三化学多选题中等难度题查看答案及解析
常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是
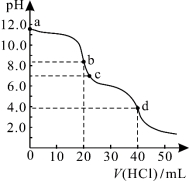
A.a点溶液呈碱性的原因用离子方程式表示为:CO+2H2O
H2CO3+2OH-
B.c点处的溶液中c(Na+)-c(Cl-)=c(HCO)+2c(CO
)
C.滴定过程中使用甲基橙作为指示剂比酚酞更准确
D.d点处溶液中水电离出的c(H+)大于b点处
高三化学选择题简单题查看答案及解析
常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是
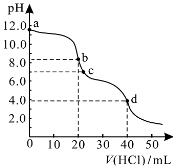
A. a点溶液呈碱性的原因用离子方程式表示为:CO+2H2O
H2CO3+2OH-
B. c点处的溶液中c(Na+)-c(Cl-)=c(HCO)+2c(CO
)
C. 滴定过程中使用甲基橙作为指示剂比酚酞更准确
D. d点处溶液中水电离出的c(H+)大于b点处
高三化学选择题困难题查看答案及解析
常温下,用0.1000mol/L的盐酸滴定20.00mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是( )
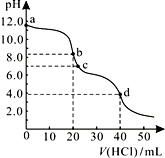
A. c点处的溶液中c(Na+)-c(Cl-)=c(HCO)+2c(CO
)
B. a点溶液呈碱性的原因用离子方程式表示为: CO+2H2O
H2CO3+2OH-
C. b点溶液中c(Na+)> c(HCO)> c(Cl-)
D. d点处溶液中水的电离程度大于b点处
高三化学选择题中等难度题查看答案及解析
常温下,用0.1000mol/L的盐酸滴定20.00mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是( )
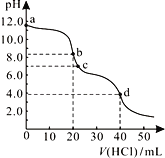
A. c点处的溶液中c(Na+)-c(Cl-)=c(HCO)+2c(CO
)
B. a点溶液呈碱性的原因用离子方程式表示为: CO+2H2O
H2CO3+2OH-
C. b点溶液中c(Na+)> c(HCO)> c(Cl-)
D. d点处溶液中水的电离程度大于b点处
高三化学选择题中等难度题查看答案及解析
常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸体积关系如右图所示。下列有关叙述错误的是
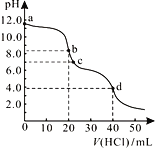
A. a点溶液呈碱性的原因用离子方程式表示为:CO32-+H2OHCO3-+OH-
B. b点处的溶液中c(Na+)-2c(CO32-)=c(HCO3-)+c(Cl-)
C. 滴定过程中使用酚酞作为指示剂比石蕊更准确
D. d点处溶液中水电离出的c(H+)小于c点处
高三化学单选题困难题查看答案及解析
常温下,用0. 1000 mol·L-1的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示(饱和H2CO3溶液pH=5.6)。下列有关叙述正确的是
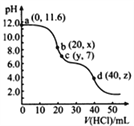
A. 若c(Na2CO3)=0.1000 mol·L-1,则H2CO3的Ka2数量级约为10-6
B. c点处溶液中一定有:c(Na+)=2c(CO32-)+c(HCO3-)
C. a、c两点水的c(OH-)之比为10-11.6 :10-7
D. 若z=5.6,则d点有c(Na+)=c(Cl-)>c(H2CO3)>c(OH-)
高三化学单选题中等难度题查看答案及解析
常温下,用0. 1000 mol·L-1的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示(饱和H2CO3溶液pH=5.6)。下列有关叙述正确的是

A. 若c(Na2CO3)=0.1000 mol·L-1,则H2CO3的Ka2数量级约为10-6
B. c点处溶液中一定有:c(Na+)=2c(CO32-)+c(HCO3-)
C. a、c两点水的c(OH-)之比为10-11.6 :10-7
D. 若z=5.6,则d点有c(Na+)=c(Cl-)>c(H2CO3)>c(OH-)
高三化学单选题中等难度题查看答案及解析
常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸体积关系如右图所示。下列有关叙述错误的是
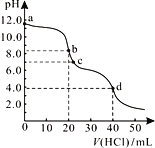
A. a点溶液呈碱性的原因用离子方程式表示为:CO32-+H2OHCO3-+OH-
B. b点处的溶液中c(Na+)-2c(CO32-)=c(HCO3-)+c(Cl-)
C. 滴定过程中使用酚酞作为指示剂比石蕊更准确
D. d点处溶液中水电离出的c(H+)小于c点处
高三化学单选题困难题查看答案及解析
常温下,用0. 1000 mol·L-1的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示(饱和H2CO3溶液pH=5.6)。下列有关叙述正确的是
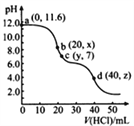
A. 若c(Na2CO3)=0.1000 mol·L-1,则H2CO3的Ka2数量级约为10-6
B. c点处溶液中一定有:c(Na+)=2c(CO32-)+c(HCO3-)
C. a、c两点水的c(OH-)之比为10-11.6 :10-7
D. 若z=5.6,则d点有c(Na+)=c(Cl-)>c(H2CO3)>c(OH-)
高三化学单选题中等难度题查看答案及解析