已知常温下,向溶液中,滴入
NaOH溶液,所得曲线如图所示,下列说法正确的是(已知电离度为已电离粒子的浓度与初始浓度的比值)()

A.若A点的,则此温度下醋酸的电离度计算式为
B.B点存在等式关系:
C.若C点加入氢氧化钠溶液amL,则常温下醋酸的电离平衡常数计算式为
D.若D点,则由水电离出的
高三化学单选题中等难度题
已知常温下,向溶液中,滴入
NaOH溶液,所得曲线如图所示,下列说法正确的是(已知电离度为已电离粒子的浓度与初始浓度的比值)()

A.若A点的,则此温度下醋酸的电离度计算式为
B.B点存在等式关系:
C.若C点加入氢氧化钠溶液amL,则常温下醋酸的电离平衡常数计算式为
D.若D点,则由水电离出的
高三化学单选题中等难度题
已知常温下,向溶液中,滴入
NaOH溶液,所得曲线如图所示,下列说法正确的是(已知电离度为已电离粒子的浓度与初始浓度的比值)()

A.若A点的,则此温度下醋酸的电离度计算式为
B.B点存在等式关系:
C.若C点加入氢氧化钠溶液amL,则常温下醋酸的电离平衡常数计算式为
D.若D点,则由水电离出的
高三化学单选题中等难度题查看答案及解析
常温下,用0.1000mol/L的NaOH溶液滴定某浓度的二元弱酸()溶液,所得溶液中各种含X的微粒的物质的量分数(
)与pH的变化曲线如图所示。下列说法正确的是
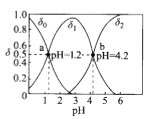
A.的电离常数
,
的水解常数
B.由水电离出的c():a>b
C.曲线分别表示
(
)和
(HX-)的变化
D.b点所示溶液中:c(>3c(
)
高三化学单选题困难题查看答案及解析
常温下,用0.1000mol/L的NaOH溶液滴定某浓度的二元弱酸()溶液,所得溶液中各种含X的微粒的物质的量分数(
)与pH的变化曲线如图所示。下列说法正确的是
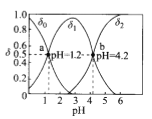
A. 的电离常数
,
的水解常数
B. 由水电离出的c():a>b
C. 曲线分别表示
(
)和
(HX-)的变化
D. b点所示溶液中:c(>3c(
)
高三化学单选题困难题查看答案及解析
常温下,用某浓度的NaOH溶液滴定20.00 mL 等浓度的CH3COOH溶液,所得滴定曲线如下图。下列说法正确的是
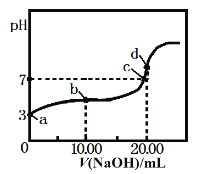
A. a点醋酸的浓度为1.0×10-3mol·L-1
B. a、b 两点对应的醋酸电离平衡常数:a<b
C. c点c(Na+):c(CH3COO-)=1:1
D. d点溶液升高温度,溶液pH不变
高三化学单选题中等难度题查看答案及解析
已知:,
。常温下,向某浓度的盐酸溶液中滴加氢氧化钠溶液,所得溶液的
和
变化如图所示。下列说法正确的是( )
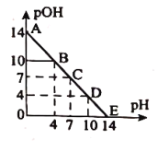
A.盐酸与溶液的浓度相等
B.点和
点水的电离程度相同
C.滴加溶液改为加水稀释,该图曲线不变
D.升高温度,滴定过程中pH+pOH>14
高三化学单选题中等难度题查看答案及解析
下列说法正确的是( )
A.常温下将pH=2的醋酸和pH=12的NaOH溶液等体积混合,所得溶液显碱性
B.已知同温时氢氟酸的电离常数大于亚硝酸的电离常数,则相同温度相同浓度的NaF溶液和NaNO2溶液的碱性:NaF溶液较强
C.将等体积的盐酸和氨水混合,充分反应后所得溶液呈中性,则两溶液的物质的量浓度关系为:c(HCl)<c(NH3·H2O)
D.已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)= c(CO32-),且c(Mg2+)·c(CO32-)=6.82×10-6
高三化学选择题中等难度题查看答案及解析
常温下,0.2mol·L-1NaHA与等浓度等体积的NaOH溶液混合,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
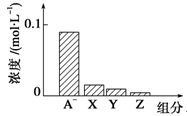
A.NaHA溶液显酸性
B.混合溶液中水电离出的C(OH-)、C(H+)相等
C.图中X、Y、Z分别代表OH-、HA-、H+
D.混合溶液中:C(Na+)= C(H2A)+ C(HA-)+ C(A2-)
高三化学选择题困难题查看答案及解析
常温下,向溶液中滴加
的NaOH溶液,所得溶液pH与加入的NaOH溶液体积的关系曲线如图所示,下列说法正确的是
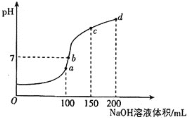
A.a、b、c、d四个点中,水的电离程度最大的是d
B.a点溶液中:
C.b点溶液中:
D.c点溶液中: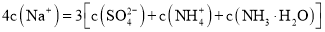
高三化学单选题中等难度题查看答案及解析
常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
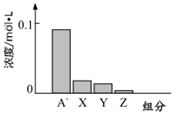
A.将HA加水稀释,溶液中所有粒子的浓度均减小
B.等浓度的HA和NaOH溶液中水的电离程度相同
C.图中X表示HA,Y表示H+,Z表示OH-
D.该混合溶液中: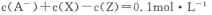
高三化学选择题困难题查看答案及解析
常温下,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/L的NaOH溶液,所得溶液PH与NaOH溶液体积的关系曲线如图所示,下列说法正确的是
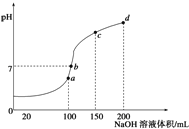
A. a、b、c、d四个点中,水的电离程度最大的是d
B. a点溶液中:c(NH3·H2O)+c(H+)=c(OH—)
C. b点溶液中:c(Na+)+c(NH4+)=c(SO42—)
D. c点溶液中:4c(Na+)= 3[c(SO42—) +c(NH4+)+ c(NH3·H2O)]
高三化学null困难题查看答案及解析