-
一定温度下,在某2 L恒容密闭容器中加入纳米级氧化亚铜并通入0.1 mol 水(g),发生如下反应:2H2O(g) 2H2(g)+O2(g) ΔH=+484 kJ·mol-1。不同时间产生O2的物质的量见下表:
2H2(g)+O2(g) ΔH=+484 kJ·mol-1。不同时间产生O2的物质的量见下表:
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
下列说法不正确的是( )
A.前20 min内的平均反应速率v(H2O)=5×10-5mol·L-1·min-1
B.达到平衡时,需要从外界吸收的能量为0.968 kJ
C.增大水的浓度,可以改变待反应的限度
D.使用纳米级的氧化亚铜,可以增大平衡时氧气的体积分数
-
一定温度下,在某2 L恒容密闭容器中加入纳米级氧化亚铜并通入0.1 mol 水(g),发生如下反应:2H2O(g) 2H2(g)+O2(g) ΔH=+484 kJ·mol-1。不同时间产生O2的物质的量见下表:
2H2(g)+O2(g) ΔH=+484 kJ·mol-1。不同时间产生O2的物质的量见下表:
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
下列说法不正确的是( )
A.前20 min内的平均反应速率v(H2O)=5×10-5mol·L-1·min-1
B.达到平衡时,需要从外界吸收的能量为0.968 kJ
C.增大水的浓度,可以改变待反应的限度
D.使用纳米级的氧化亚铜,可以增大平衡时氧气的体积分数
-
在一定温度下,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g) 2Z(g),此反应达到平衡的标志是( )
2Z(g),此反应达到平衡的标志是( )
A. 单位时间内消耗0.1 mol X的同时生成0.2 mol Z
B. v正(X) =v逆(Z)
C. 容器内X、Y、Z的浓度之比为1∶2∶2
D. 容器内压强不随时间变化
-
在一定温度下,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g) 2Z(g),此反应达到平衡的标志是( )
2Z(g),此反应达到平衡的标志是( )
A. 单位时间内消耗0.1 mol X的同时生成0.2 mol Z
B. v正(X) =v逆(Z)
C. 容器内X、Y、Z的浓度之比为1∶2∶2
D. 容器内压强不随时间变化
-
在相同的密闭容器中,用高纯度纳米级Cu2O分别进行催化分解水的实验:2H2O(g) 2H2(g) + O2(g) ∆H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
2H2(g) + O2(g) ∆H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
| 序号 | 时间/min | 0 | 10 | 20 | 30 | 40 | 60 |
| ① | 温度T1 / 1号Cu2O | 0.0500 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | 温度T1 / 2号Cu2O | 0.0500 | 0.0490 | 0.0483 | 0.0480 | 0.0480 | 0.0480 |
| ③ | 温度T2 / 2号Cu2O | 0.0500 | 0.0480 | 0.0470 | 0.0470 | 0.0470 | 0.0470 |
下列说法不正确的是( )
A.实验时的温度T2高于T1
B.2号Cu2O的催化效率比1号Cu2O的催化效率高
C.实验①前20 min的平均反应速率v(O2) = 7×10ˉ5 mol·Lˉ1·minˉ1
D.等质量纳米级Cu2O比微米级Cu2O催化效率高,这与Cu2O的粒径大小有关
-
在相同的密闭容器中,用高纯度纳米级Cu2O分别进行催化分解水的实验:2H2O(g) 2H2(g) + O2(g) ∆H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
2H2(g) + O2(g) ∆H>0,实验测得反应体系中水蒸气浓度(mol·L-1)的变化结果如下:
| 序号 | 时间/min | 0 | 10 | 20 | 30 | 40 | 60 |
| ① | 温度T1 / 1号Cu2O | 0.0500 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | 温度T1 / 2号Cu2O | 0.0500 | 0.0490 | 0.0483 | 0.0480 | 0.0480 | 0.0480 |
| ③ | 温度T2 / 2号Cu2O | 0.0500 | 0.0480 | 0.0470 | 0.0470 | 0.0470 | 0.0470 |
下列说法不正确的是( )
A.实验时的温度T2高于T1
B.2号Cu2O的催化效率比1号Cu2O的催化效率高
C.实验①前20 min的平均反应速率v(O2) = 7×10ˉ5 mol·Lˉ1·minˉ1
D.等质量纳米级Cu2O比微米级Cu2O催化效率高,这与Cu2O的粒径大小有关
-
向某密闭容器中加入0.3 mol A、0.1 mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示。附图中乙图为 t2时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件,所用条件均不同。已知, t3 ~t4阶段为使用催化剂[已知t0~t1阶段c(B)未画出]。
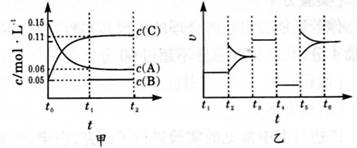
(1)若 t1=15s,则t0~ t1阶段以C浓度变化表示的反应速率为v(C)= 。
(2)t4~t5阶段改变的条件为 ,B的起始物质的量为 。
(3)t5~t6阶段容器内A的物质的量共减少0.03 mol,而此过程中容器与外界的热交换总量为akJ,写出该反应的热化学方程式 。
-
在一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应2HI(g)  H2(g)+I2(g),2s 时生成0.1 mol H2,则以HI表示该时段的化学反应速率是
H2(g)+I2(g),2s 时生成0.1 mol H2,则以HI表示该时段的化学反应速率是 ( )
( )
A.0.05 mol·Lˉ1·sˉ1
B.0.1 mol·Lˉ1·sˉ1
C.0.2 mol·Lˉ1·sˉ1
D.0.8 mol·Lˉ1·sˉ1
-
工业上用CO生产燃料甲醇。一定温度和容积条件下发生反应:CO(g)+2H2(g) CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
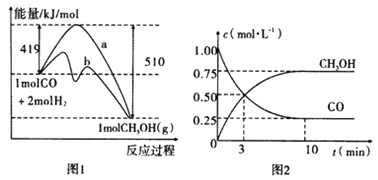
请回答下列问题:
(1)在“图1”中,曲线_________(填“a”或“b”)表示使用了催化剂;没有使用催化剂时,在该温度和压强条件下反应CO(g)+2H2(g) CH3OH(g)的△H=_____________。
CH3OH(g)的△H=_____________。
(2)下列说法正确的是__________。
A.起始充入的CO的物质的量为1mol
B.增加CO的浓度,H2的转化率会增大
C.容器中压强恒定时,反应达到平衡状态
(3)从反应开始到建立平衡,v(CO)=____________;达到平衡时,c(H2)=_________,该温度下CO(g)+2H2(g)  CH3OH(g)的化学平衡常数为______________。达到平衡后若保持其它条件不变,将容器体积压缩为0.5L,则平衡___________移动 (填“正向”、“逆向”或“不”)(4)已知CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g);ΔH=-193kJ/mol。又知H2O(l)= H2O(g)ΔH=+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式___________________________________________________。
CH3OH(g)的化学平衡常数为______________。达到平衡后若保持其它条件不变,将容器体积压缩为0.5L,则平衡___________移动 (填“正向”、“逆向”或“不”)(4)已知CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g);ΔH=-193kJ/mol。又知H2O(l)= H2O(g)ΔH=+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式___________________________________________________。
(5)已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P—P:198,Cl—Cl :243,P—Cl:331。
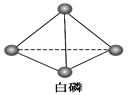
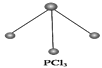
则反应P4(白磷,s)+6Cl2(g) 4PCl3(s)的反应热ΔH=____________________。
4PCl3(s)的反应热ΔH=____________________。
-
工业上用CO生产燃料甲醇。一定温度和容积条件下发生反应:CO(g)+2H2(g) CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
CH3OH(g)。图1表示反应中的能量变化;图2表示一定温度下,在体积为1L的密闭容器中加入2mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。

请回答下列问题:
(1)在“图1”中,曲线_______(填“a”或“b”)表示使用了催化剂;没有使用催化剂时,在该温度和压强条件下反应CO(g)+2H2(g) CH3OH(g)的△H=_________。
CH3OH(g)的△H=_________。
(2)从反应开始到建立平衡,v(CO)=________;达到平衡时,该温度下CO(g)+2H2(g)  CH3OH(g)的化学平衡常数为______________。达到平衡后若保持其它条件不变,将容器体积压 缩为0.5L,则平衡___________移动 (填“正向”、“逆向”或“不”)。
CH3OH(g)的化学平衡常数为______________。达到平衡后若保持其它条件不变,将容器体积压 缩为0.5L,则平衡___________移动 (填“正向”、“逆向”或“不”)。
(3)已知CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g);ΔH=-193kJ/mol。又知H2O(l)= H2O(g);ΔH=+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式____________。
2H2(g)+O2(g) ΔH=+484 kJ·mol-1。不同时间产生O2的物质的量见下表:




