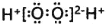-
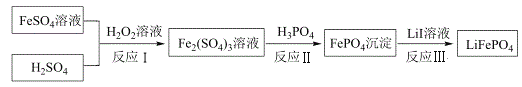
2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂(LiFePO4)。LiFePO4的一种制备方法如图。

下列说法正确的是( )
A.过氧化氢的电子式为: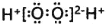
B.反应Ⅰ的离子方程式为:2Fe2++H2O2=2Fe3++2OH-
C.反应Ⅱ的离子方程式为:Fe3++PO =FePO4↓
=FePO4↓
D.反应Ⅲ的化学方程可能为:2FePO4+2LiI=2LiFePO4+I2
-
2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂(LiFePO4)。LiFePO4的一种制备方法如图。
已知:H3PO4能电离出PO 。
。
(1)LiFePO4中,铁元素的化合价为_____。
(2)反应I中H2O2的作用是_____。
(3)检测反应II中铁离子是否完全反应的操作是_____。(离子检验常用的表达方式为:取xx试剂,向其中滴加xx,若出现xx现象,则说明xx结论。)
(4)反应Ⅲ的化学方程式是_____。
-
2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂(LiFePO4)。LiFePO4的一种制备方法如下。

已知:H3PO4能电离出PO43-。
(1)Li在元素周期表中的位置是________。
(2)LiFePO4中,铁元素的化合价为________价。
(3)将反应Ⅰ补充完整:____Fe2+ + 2H+ + ____H2O2 =____Fe3+ + 2H2O 。____
(4)反应Ⅲ的化学方程式是_________。
-
2019年诺贝尔化学奖授予古迪纳夫(John Goodenough)等三位化学家,以表彰其在锂电池发展上所做的杰出贡献。古迪纳夫开发了钴酸锂、锰酸锂和磷酸亚铁锂等电极材料,其中磷酸亚铁锂(LiFePO4)可通过如下反应制备:Li2CO3+2FePO4+H2C2O4 3CO2↑+2LiFePO4+H2O。
3CO2↑+2LiFePO4+H2O。
(1)配平上述化学方程式,并在方程式上面用“双线桥”标明电子转移的方向和数目_______。
(2)该反应的还原产物为_________。若反应中转移0.1 mol电子,则生成标准状况下的CO2________L。
-
2019年诺贝尔化学奖授予美国科学家约翰•古迪纳夫、斯坦利•惠廷厄姆和日本科学家吉野彰,以表彰他们在锂离子电池研发领域作出的贡献。近日,有化学家描绘出了一种使用DMSO(二甲基亚砜)作为电解液,并用多孔的黄金作为电极的锂—空气电池的实验模型,该电池放电时在多孔的黄金上氧分子与锂离子反应,形成过氧化锂(Li2O2),其装置图如图所示。下列有关叙述正确的是
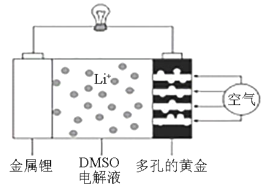
A.DMSO电解液能传递Li+和电子,不能换成水溶液
B.该电池放电时每消耗2molO2,转移4mol电子
C.该池放电时,外电路中电流的方向为从金属锂电极流出
D.多孔的黄金为电池正极,电极反应式可能为O2+4e-=2O2-
-
2019年诺贝尔化学奖颁给几位在锂离子电池研发领域做出贡献的科学家,锂单质化学性质与钠类似,活泼性比钠略差。它的密度为0.534g/cm3,锂元素的焰色为紫红色,将绿豆大的锂投入水中,下列实验现象合理的有( )
①锂沉入水中 ②锂浮在水面上 ③水中有大量气泡 ④反应后在水中加入几滴石蕊试液,溶液变红 ⑤反应剧烈,发出紫红色火焰 ⑥锂四处游动
A.②⑥ B.①③ C.②③⑤ D.②④⑤⑥
-
2019年诺贝尔化学奖颁给几位在锂离子电池研发领域做出贡献的科学家,锂单质化学性质与钠类似,活泼性比钠略弱。它的密度为0.534g/cm3,锂元素的焰色为紫红色,将绿豆大的锂投入水中,下列实验现象合理的有( )
①锂沉入水中
②锂浮在水面上
③水中有大量气泡
④反应后在水中加入几滴石蕊试液,溶液变红
⑤反应剧烈,发出紫红色火焰
⑥锂四处游动
A.②③ B.①③ C.②③⑤ D.②④⑤⑥
-
为分离废磷酸亚铁锂电池的正极材料(主要含LiFePO4和铝箔)中的金属,将正极材料粉碎后进行如下流程所示的转化:
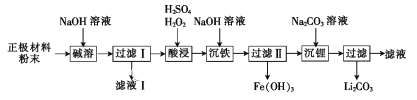
已知LiFePO4不溶于水和碱,能溶于强酸。
(1)“碱溶”时的离子方程式为___。
(2)向滤液Ⅰ中通入过量CO2会析出Al(OH)3沉淀,写出该反应的离子方程式:____。
(3)“酸浸”时溶液中Fe2+发生反应的离子方程式为_____。
(4)检验“沉铁”后所得溶液中是否存在Fe3+的方法是____。
(5)以Fe(OH)3为原料可以制取FeSO4晶体,还需的试剂有____。
(6)“沉锂”时,检验Li+是否沉淀完全的方法是____。
-
2019年诺贝尔化学奖授予三位对锂电池研究作出杰出贡献的科学家。一种锂-空气电池如图所示。当电池工作时, 与
与 在多孔碳材料电极处生成
在多孔碳材料电极处生成 (
( 或1)。下列说法正确的是
或1)。下列说法正确的是

A.锂电极发生氧化反应
B.多孔碳材料电极为负极
C.电池工作时外电路电子由多孔碳材料电极流向锂电极
D.正极的电极反应式为:
-
磷酸铁锂动力电池的正极与负极中间是聚合物的隔膜隔开的,锂离子可以通过。该电池的总反应式为:Li1﹣xFePO4+LixC6═C6+LiFePO4 (注:LixC6是单质Li附在碳电极上的一种形式)
(1)磷酸铁锂电池放电时,负极反应式为 。
(2)若用该电池电解精炼铜,阴极质量增重19.2g时,则电池中通过聚合物隔膜的Li+数目为 。
(3)以该电池为电源,用Fe2O3为阳极,石墨为阴极,NaOH溶液为电解质溶液制备高铁酸钠(Na2FeO4),写出阳极的电极反应式 。
(4)以该电池为电源,用惰性电极电解2L硫酸铜和氯化钠的混合溶液, 若两极均产生0.14mol气体,电路中共有0.4mol的电子转移,则电解后溶液的c(OH-)为 。
若两极均产生0.14mol气体,电路中共有0.4mol的电子转移,则电解后溶液的c(OH-)为 。