-
Zn、Fe及其化合物在生产生活中应用比较广泛。工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO和CuO等杂质)制取金属锌的工艺流程如下:
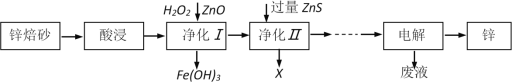
(1)为了提高酸浸效率,可采用的措施有___________________________________(任答两条);
写出ZnFe2O4溶于酸的离子方程式____________________________________
(2)向净化Ⅰ操作中加入ZnO的目的___________________________________
(3)若净化后的溶液中Cu2+浓度为1×10-12mol/L,则净化后溶液中Zn2+浓度为__________(已知:室温下Ksp(ZnS)=1.6×10-24, Ksp(CuS)=6.4×10-36)
(4)“电解”工艺制锌时Zn2+利用率较低,废液中有大 量的Zn2+ 残留。某化工厂拟采用改变酸锌比净化废液的方式来提高原料的利用率,降低成本。如图是工业生产中不同酸锌比时净化液利用率对电解时直流电耗能影响关系图。根据图分析,该工厂净化废液时的最佳酸锌比为______。
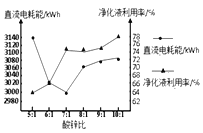
A. 5:1 B.6:1 C.7:1 D.10:1
(5)ZnFe2O4是一种性能优良的软磁材料,工业上常利用ZnFe2(C2O4)3·6H2O隔绝空气加热分解制备,该晶体的热分解化学方程式为_______________________________________。测热分解后产品中ZnFe2O4的质量分数方法如下:取a克产品用H2SO4溶解后加入足量KI溶液充分反应,调溶液至弱酸性,再加入淀粉指示剂,用c mol/L Na2S2O3标准溶液滴定,用去此标准溶液v mL时,刚好到达滴定终点,则此产品中ZnFe2O4的质量分数为____________(用a、c、v表示)。(已知:I2+2S2O32-=2I-+S4O62-)
-
Zn、Fe及其化合物在生产生活中应用比较广泛。工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO和CuO等杂质)制取金属锌的工艺流程如下:
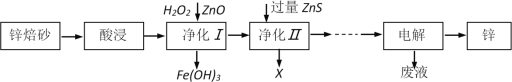
(1)为了提高酸浸效率,可采用的措施有___________________________________(任答两条);
写出ZnFe2O4溶于酸的离子方程式____________________________________
(2)向净化Ⅰ操作中加入ZnO的目的___________________________________
(3)若净化后的溶液中Cu2+浓度为1×10-12mol/L,则净化后溶液中Zn2+浓度为__________(已知:室温下Ksp(ZnS)=1.6×10-24, Ksp(CuS)=6.4×10-36)
(4)“电解”工艺制锌时Zn2+利用率较低,废液中有大 量的Zn2+ 残留。某化工厂拟采用改变酸锌比净化废液的方式来提高原料的利用率,降低成本。如图是工业生产中不同酸锌比时净化液利用率对电解时直流电耗能影响关系图。根据图分析,该工厂净化废液时的最佳酸锌比为______。
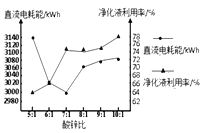
A. 5:1 B.6:1 C.7:1 D.10:1
(5)ZnFe2O4是一种性能优良的软磁材料,工业上常利用ZnFe2(C2O4)3·6H2O隔绝空气加热分解制备,该晶体的热分解化学方程式为_______________________________________。测热分解后产品中ZnFe2O4的质量分数方法如下:取a克产品用H2SO4溶解后加入足量KI溶液充分反应,调溶液至弱酸性,再加入淀粉指示剂,用c mol/L Na2S2O3标准溶液滴定,用去此标准溶液v mL时,刚好到达滴定终点,则此产品中ZnFe2O4的质量分数为____________(用a、c、v表示)。(已知:I2+2S2O32-=2I-+S4O62-)
-
Zn、Fe及其化合物在生产生活中应用比较广泛。工业上利用锌焙砂 主要含ZnO、
主要含ZnO、 ,还含有少量FeO和CuO等杂质
,还含有少量FeO和CuO等杂质 制取金属锌的工艺流程如下:
制取金属锌的工艺流程如下:
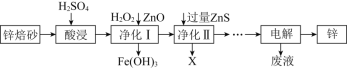
回答下列问题:
 “酸浸”时
“酸浸”时 溶于酸的化学反应方式________。
溶于酸的化学反应方式________。
 向“净化I”中加入ZnO的目的____________。
向“净化I”中加入ZnO的目的____________。
 “净化Ⅱ”中反应的离子方程式为__________。
“净化Ⅱ”中反应的离子方程式为__________。
 “电解”工艺制锌时
“电解”工艺制锌时 利用率较低,废液中有大量的
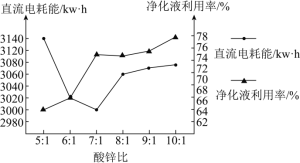
利用率较低,废液中有大量的 残留。某化工厂拟采用改变酸锌比净化废液的方式来提高原料的利用率,降低成本。下图是工业生产中不同酸锌比时净化液利用率对电解时直流电耗能影响关系图。根据下图分析,该工厂净化废液时的最佳酸锌比为_______
残留。某化工厂拟采用改变酸锌比净化废液的方式来提高原料的利用率,降低成本。下图是工业生产中不同酸锌比时净化液利用率对电解时直流电耗能影响关系图。根据下图分析,该工厂净化废液时的最佳酸锌比为_______ 填写序号
填写序号 。
。
A 



 是一种性能优良的软磁材料,工业上常利用
是一种性能优良的软磁材料,工业上常利用 隔绝空气加热分解制备,同时生成CO、
隔绝空气加热分解制备,同时生成CO、 等,该晶体的受热分解化学方程式为________。测定产品中
等,该晶体的受热分解化学方程式为________。测定产品中 的质量分数,其方法是取a克产品用
的质量分数,其方法是取a克产品用 溶解后加入足量KI溶液充分反应,调溶液至弱酸性,再加入淀粉指示剂,用
溶解后加入足量KI溶液充分反应,调溶液至弱酸性,再加入淀粉指示剂,用 标准溶液滴定,用去此标准溶液
标准溶液滴定,用去此标准溶液 时,刚好到达滴定终点,则此产品中
时,刚好到达滴定终点,则此产品中 的质量分数为_______________
的质量分数为_______________ 用a、c、v表示
用a、c、v表示 。
。 已知:
已知:
-
锌是一种常用金属,工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO 等)湿法制取金属锌的流程如图所示,回答下列问题。
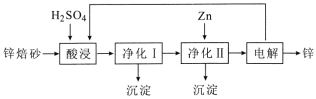
已知:Fe的活泼性强于Ni。
(1)ZnFe2O4可写成ZnO•Fe2O3,则ZnFe2O4与H2SO4反应的化学方程式___。
(2)“净化Ⅰ”操作分为两步:
①将溶液中少量的 Fe2+氧化,下列试剂中可选用的是_____(填字母标号)。
A.新制氯水 B.30 % H2O2溶液 C.FeC13溶液 D.KMnO4溶液
②加入ZnO,调节溶液pH为3.3~6.7;加热到60℃左右并不断搅拌,加热搅拌主要目的是___。
(3)“净化Ⅰ”生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是____。
(4)“净化Ⅱ”中加入过量Zn的目的是______。
-
工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO、CuO等杂质)制取金属锌的工艺流程如下:
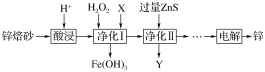
(1)酸浸时要将锌焙砂粉碎,其目的是提高酸浸效率,为达到这一目的,还可采用的措施是_____(任答一条)。写出ZnFe2O4溶于酸的离子方程式____________________________
(2)净化Ⅰ中H2O2 参与反应的离子方程式为_________________________
(3)净化Ⅱ中Y 的主要成分是________(填化学式)。
-
工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO等氧化物)制取金属锌的流程如图所示。回答下列问题:
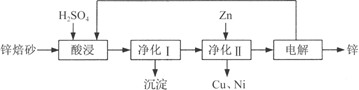
(1)酸浸时ZnFe2O4会生成两种盐,该反应的化学方程式为___________。
(2)净化Ⅰ操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,使Fe3+转化为Fe(OH)3沉淀。
①写出酸性条件下H2O2与Fe2+反应的离子方程式:___________。
②25 ℃时,pH=3的溶液中,c(Fe3+)=________mol·L-1(已知25 ℃,Ksp[Fe( OH)3]=4.0×10-38)。
③净化Ⅰ生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是____________________。
(3)若没有净化Ⅱ操作,则对锌的制备带来的影响是_________________。
⑷本流程中可以循环利用的物质除锌外还有________________。
-
工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO等氧化物)制取金属锌的流程如图所示。回答下列问题:
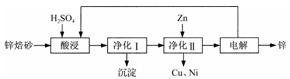
(1)酸浸时ZnFe2O4会生成两种盐,该反应的化学方程式为___________。
(2)净化Ⅰ操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,使Fe3+转化为Fe(OH)3沉淀。
①写出酸性条件下H2O2与Fe2+反应的离子方程式:___________。
②25 ℃时,pH=3的溶液中,c(Fe3+)=___________mol·L-1(已知25 ℃,Ksp[Fe( OH)3]=4.0×10-38)。
③净化Ⅰ生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是_______________。
(3)若没有净化Ⅱ操作,则对锌的制备带来的影响是_________________。
(4)本流程中可以循环利用的物质除锌外还有________________。
-
工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO等氧化物)制取金属锌的流程如图所示。回答下列问题:
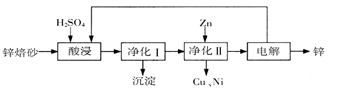
(1)酸浸时ZnFe2O4会生成两种盐,该反应的化学方程式为________
(2)净化I操作分为两步:第一步是将溶液中少量的Fe2+氧化;第二步是控制溶液pH,使Fe3+转为Fe(OH)3沉淀。
①写出酸性条件下H2O2与Fe2+反应的离子方程式________
②250C时,pH=3的溶液中,c (Fe3+)=________mol/L(已知25℃, 。
。
③净化I生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是________。
(3)若没有净化II操作,则对锌的制备带来的影响是________。
(4)本流程中可以循环利用的物质除锌外还有________。
-
工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO、CuO等氧化物杂质)制取金属锌的流程如图所示。
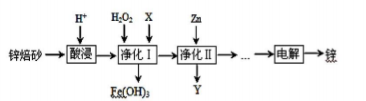
(1)提高酸浸效率的措施为____________(任答一条即可);酸浸时H +与难溶固体ZnFe2O4反应的离子方程式为____________________________。
+与难溶固体ZnFe2O4反应的离子方程式为____________________________。
(2)净化I中H2O2参与反应的离子方程式为_____________________;X可选择的试剂为___________(写化学式),净化II中Y为__________(写化学式);
(3)电解法制备锌的装置如图甲所示:
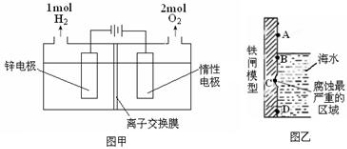
则电解槽中盛有的电解质溶液为__________(填字母);
a.ZnCl2溶液 b.Zn(NO3)2溶液 c.ZnSO4溶液
(4)使用含有[Zn(OH)4]2-的强碱性电镀液进行镀锌防腐蚀,可得到细致的光滑镀层,电镀时阴极电极反应式_______________。以锌为负极,采用牺牲阳极法防止铁闸的腐蚀,图乙中锌块的固定位置最好应在_________处(填字母)。
-
工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO、CuO等杂质)制取金属锌的工艺流程如下:回答下列问题:
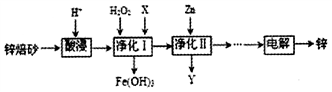
(1)ZnFe2O4是一种性能优良的软磁材料,也是一种催化剂,能催化烯类有机物氧化脱氢等反应。
①ZnFe2O4中Fe的化合价是__________,从物质分类角度说,ZnFe2O4属于_________ (填“酸”、“碱”或“盐”)。
②工业上利用反应ZnFe2(C2O4)3·6H2O ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中氧化产物是_______ (填化学式),每生成1mol ZnFe2O4,转移电子的物质的量是_____。
ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中氧化产物是_______ (填化学式),每生成1mol ZnFe2O4,转移电子的物质的量是_____。
(2)酸浸时要将锌焙砂粉碎,其目的是提高酸浸效率。为达到这一目的,还可采用的措施是______________________(任答一条);已知ZnFe2O4能溶于酸,则酸浸后溶液中存在的金属离子有__________________。
(3)净化I中H2O2参与反应的离子方程式为_______________________;试剂X的作用是_________________________。
(4)钢铁镀锌是钢铁防护的一种有效方法。按图甲装置进行模拟铁上镀锌的实验,实验结果如图乙所示。乙中横坐标x表示电路中通过电子的物质的量,纵坐标y表示反应物或生成物的物质的量。
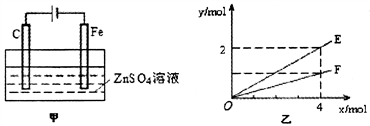
①C电极的电极反应式为___________________________。
②E可以表示的量是__________________________(任写一种)。
主要含ZnO、
,还含有少量FeO和CuO等杂质
制取金属锌的工艺流程如下:
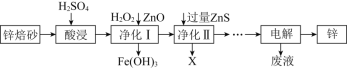
“酸浸”时
溶于酸的化学反应方式________。
向“净化I”中加入ZnO的目的____________。
“净化Ⅱ”中反应的离子方程式为__________。
“电解”工艺制锌时
利用率较低,废液中有大量的
残留。某化工厂拟采用改变酸锌比净化废液的方式来提高原料的利用率,降低成本。下图是工业生产中不同酸锌比时净化液利用率对电解时直流电耗能影响关系图。根据下图分析,该工厂净化废液时的最佳酸锌比为_______
填写序号
。

是一种性能优良的软磁材料,工业上常利用
隔绝空气加热分解制备,同时生成CO、
等,该晶体的受热分解化学方程式为________。测定产品中
的质量分数,其方法是取a克产品用
溶解后加入足量KI溶液充分反应,调溶液至弱酸性,再加入淀粉指示剂,用
标准溶液滴定,用去此标准溶液
时,刚好到达滴定终点,则此产品中
的质量分数为_______________
用a、c、v表示
。
已知:












