-
氨是重要的工业原料,其可以用来合成氮肥,某氮肥厂氨氮废水中氮元素多以NH4+和NH3·H2O的形式存在,该废水的处理流程如下:
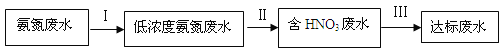
请回答下列问题:
(1)过程1中加入氢氧化钠,写出其中发生的离子方程式____________________
(2)写出氨分子的结构式______;指出分子中化学键是_____(填‘离子键’或‘共价键’)。
(3)过程Ⅱ:在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。其中第一步反应的能量变化示意图如图:
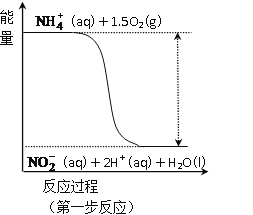
第一步反应是_______反应(选填“放热”或“吸热”),判断依据是_______________。
-
(8分)某氮肥厂氨氮废水中氮元素多以 和NH3·H2O的形式存在,该废水的处理流程如下:
和NH3·H2O的形式存在,该废水的处理流程如下:
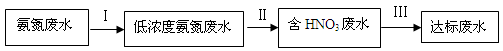
(1)过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30 ℃,通空气将氨赶出并回收。用离子方程式表示加NaOH溶液的作用: 。
(2)过程Ⅱ:在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。其中第一步反应的能量变化示意图如下:
。其中第一步反应的能量变化示意图如下:
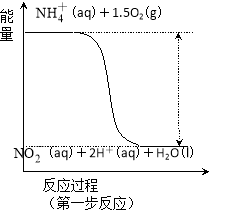
第一步反应是 反应(选填“放热”或“吸热”),判断依据是
(3)过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比是 。
-
氨气(NH3)是一种重要的化工原料,广泛应用于制氮肥、制药、合成纤维等。请回答下列问题:
(1)2molNH3在标准状况下的体积是___。
(2)2molNH3的质量是___,其中所含氢元素的质量是___。
(3)2molNH3所含的氨分子数为___,电子数为___。
(4)工业上用反应N2+3H2  2NH3来合成氨气,则若制得2molNH3,标准状况下参与反应的H2的体积为___;14克N2参与反应可得NH3物质的量为___。
2NH3来合成氨气,则若制得2molNH3,标准状况下参与反应的H2的体积为___;14克N2参与反应可得NH3物质的量为___。
-
氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、铵盐和纯碱等的原料。
(1)以氨为燃料,氧气为氧化剂可以设计制造氨燃料电池,因产物无污染,在很多领域得到广泛应用。若电极材料均为惰性电极,KOH溶液作电解质溶液,则该电池负极电极反应式为________________;正极反应式为_________________________。
(2)下列措施可以加快合成氨反应速率的是_________。
A.通过缩小容器的容积增大压强
B.及时将氨液化分离出去
C.适当升温
D.添加合适的催化剂
E.恒温恒容时,再充入一定体积的氮气
(3)某化学研究性学习小组模拟工业合成氨的反应。在容积固定为2L的密闭容器内充入1mol N2和3mol H2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
则从反应开始到25 min时,①以N2表示的平均反应速率为________;②H2的平衡转化率为____________;
(4) 以CO2与NH3为原料合成尿素[化学式为CO(NH2)2]的主要反应如下,已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);ΔH=-159.47 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g);ΔH=+116kJ·mol-1
③H2O(l)=H2O(g);ΔH=+44kJ·mol-1
写出CO2与NH3合成尿素和液态水的热化学反应方程式_______________。
-
氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、按盐和纯碱等的原料。
(1)以氨为燃料,氧气为氧化剂可以设计制造氨燃料电池,因产物无污染,在很多领域得到广泛应用。若电极材料均为惰性电极,KOH 溶液作电解质溶液,则该电池负极电极反应式为_______________;正极反应式为______________。
(2)下列措施可以加快合成氨反应速率的是______________。
A.通过缩小容器的容积增大压强 B.及时将氨液化分离出去
C.适当升温 D.添加合适的催化剂
E.恒温恒容时,再充入一定体积的氮气
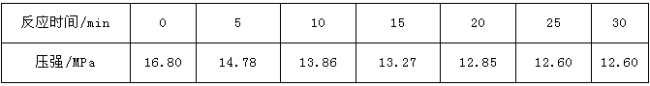
(3)某化学研究性学习小组模拟工业合成氨的反应。在容积固定为2L的密闭容器内充入lmolN2 和3molH2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
则①从反应开始到25min时,以N2表示的平均反应速率为________;
②H2的平衡转化率为_______________;
(4)以CO2与NH3为原料合成尿素[化学式为CO(NH2)2]的主要反应如下,已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);△H=-159.47kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g);△H=+116kJ·mol-1
③ H2O(l)=H2O(g);△H=+44kJ·mol-1
写出CO2 与NH3 合成尿素和液态水的热化学反应方程式_____________。
-
NH3及其盐都是重要的化工原料。
(1)合成氨工业对化学的国防工业具有重要意义,写出氨的两种重要用途 。
(2)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为 。
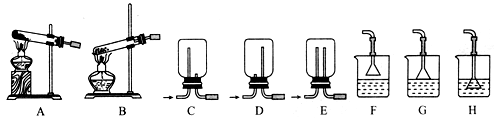
实验室制备氨气,下列方法中适宜选用的是 。
①固态氯化铵加热分解 ②固体氢氧化钠中滴加浓氨水
③氯化铵溶液与氢氧化钠溶液共热 ④加热农氨水
(3)按下图装置进行NH3性质实验。(已知AB两瓶容积相同)
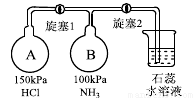
①先打开旋塞1,B瓶中的现象是 ,原因是 ,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是 。
(4)某兴趣小组在实验室探究工业合成硝酸的化学原理。
①氨的催化氧化:图a是探究氨的催化氧化的简易装置,实验中观察到锥形瓶中铂丝保持红热,有红棕色气体生成或白烟产生。白烟的成分是 (填化学式)。
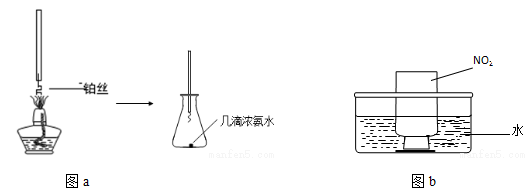
②NO2的吸收:如图b所示,将一瓶NO2倒置于水槽中,在水下移开玻璃片,可观察到的现象是 。
-
下列说法不正确的是( )
A. 光催化还原水制氢比电解水制氢更节能环保、更经济
B. 氨氮废水(含NH4+及NH3)可用化学氧化法或电化学氧化法处理
C. 某种光学检测技术具有极高的灵敏度,可检测到单个细胞(V≈10-12L)内的数个目标分子,据此可推算该检测技术能测量到细胞内浓度约为10-12~10-11mol/L的目标分子
D. 向汽油中添加甲醇后,该混合燃料的热值不变
-
(1)人类可以主动参与氮循环,合成氨工业就是参与的手段之一。以天然气为原料合成氨是新的生产氮肥的方法,它具有污染小、成本低等诸多优点。其过程大体如图1所示:
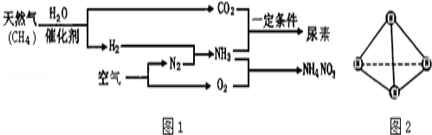
①请写出用天然气制备氢气的化学方程式:_________________________________;
②写出合成尿素[CO (NH2) 2]反应的化学方程式:__________________________;
③写出O2与NH3在有催化剂的条件下反应生成NH4NO3和H2O的化学方程式:______;
④每生产1mol NH4NO3最少需要NH3______mol,而要生产这些NH3又最少需要CH4____mol;
(2)科学家已获得极具理论研究意义的N4分子,其结构为正四面体(如图2).已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则1molN4气体转化为N2时要释放______kJ能量。
-
为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
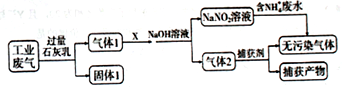
己知:NO+NO2+NaOH=NaNO2+H2O
2NO2+2NaOH=NaNO3+NaNO2+H2O
请回答下列问题:
(1)固体1中主要含有_________________________ (用化学式表示);
(2)X可以是________(填物质名称),且该物质需要________(填“少量”或“过量”);
(3)捕获剂所捕获的气体主要是________(用化学式表示);
(4)处理含NH4+废水时,发生反应的离子方程式为_________________________。
-
某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
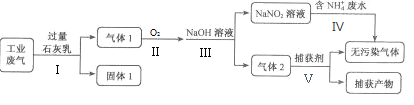
已知::2NO2+2NaOH=NaNO3+NaNO2+H2O;NO+NO2+2NaOH=2NaNO2+H2O。
(1)固体1的主要成分除Ca(OH)2外,还有__________ 、________ (填化学式);
(2)步骤Ⅱ中需要的O2量应是_____(填“少量”或“过量”);步骤Ⅴ最终捕获剂捕获的气体产物是________;
(3)步骤Ⅳ处理含NH4+废水时,发生反应的离子方程式为__________________;
(4)为确保步骤Ⅲ无NaNO3生成,理论上应控制NO与O2的物质的量之比为_____,若n(NO) :n(O2)=5:2且NaOH溶液足量,则步骤Ⅲ所得溶液中NaNO3与NaNO2的物质的量之比为______________。










