-
下列说法或表示方法正确的是( )
A.HI(g) 
 H2(g)+
H2(g)+  I2(s) △H = - 26.5kJ/mol,可知通入 1mol HI 在密闭容器中分解后可放出 26.5kJ 的能量
I2(s) △H = - 26.5kJ/mol,可知通入 1mol HI 在密闭容器中分解后可放出 26.5kJ 的能量
B.由 C(石墨)→C(金刚石)△H=+1.9kJ/mol 可知,金刚石比石墨稳定
C.在 101kPa 时,2gH2 完全燃烧生成液态水,放出 285.8kJ 热量,则 H2 燃烧热的化学方程式表示为:2H2(g)+ O2(g)=2H2O(l)△H=﹣285.8kJ/mol
D.在稀溶液中,H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJ/mol ,若将含 0.5mol H2SO4 的浓硫酸与含 1mol NaOH的溶液混合,放出的热量大于 57.3kJ
-
下列有关热化学方程式的叙述正确的是( )
A.已知HI(g)
 H2(g)+
H2(g)+ I2(s) ΔH=+26.5kJ·mol-1,则将1molHI气体置于密闭容器中充分分解,吸收26.5kJ的热量
I2(s) ΔH=+26.5kJ·mol-1,则将1molHI气体置于密闭容器中充分分解,吸收26.5kJ的热量
B.已知2H2(g)+O2(g)=2H2O(g) ΔH=-571.6kJ·mol-1,则氢气的燃烧热为ΔH=-285.8kJ·mol-1
C.已知H2(g)+F2(g)=2HF(g) △H=-270kJ·mol-1,则2 L HF气体分解成1LH2和1LF2吸收270kJ热量
D.已知OH-(aq)+H+(aq)=H2O(l) ΔH=-57.3kJ·mol-1,则含40.0gNaOH的稀溶液与稀醋酸完全中和,放出的热量小于57.3kJ
-
下列说法或表示方法正确的是
A.HI(g)  1/2H2(g)+ 1/2I2(s);△H = —26.5kJ/mol,由此可知1mol HI在密闭容器中分解后可以放出26.5kJ的能量
1/2H2(g)+ 1/2I2(s);△H = —26.5kJ/mol,由此可知1mol HI在密闭容器中分解后可以放出26.5kJ的能量
B.在稀溶液中,H+(aq)+OH-(aq)==H2O(l) ΔH=-57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3 kJ
C.由C(石墨)==C(金刚石) ΔH=1.90 kJ·mol-1可知,金刚石比石墨稳定
D.在100 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,则H2 燃烧的热化学方程式为2H2(g)+O2(g)==2H2O(l) ΔH=-285.8 kJ·mol-1
燃烧的热化学方程式为2H2(g)+O2(g)==2H2O(l) ΔH=-285.8 kJ·mol-1
-
(10分).698 K时,向某V L的密闭容器中充入2 mol H2(g)和2 mol I2(g),发生反应:H2(g)+I2(g)  2HI(g) ΔH=-26.5 kJ·mol-1,测得各物质的物质的量浓度与时间变化的关系如图所示。
2HI(g) ΔH=-26.5 kJ·mol-1,测得各物质的物质的量浓度与时间变化的关系如图所示。
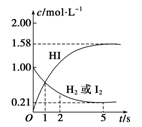
请回答下列问题:
(1)V=__________。
(2)该反应达到最大限度的时间是________,该时间内平均反应速率v(HI)=________。
(3)该反应达到平衡状态时,________(填“吸收”或“放出”)的热量为__________。
-
698 K时,向V L的密闭容器中充入2 mol H2(g)和2 mol I2(g),发生反应:H2(g)+I2(g)⇌2HI(g) ΔH=-26.5 kJ·mol-1,测得各物质的物质的量浓度与时间变化的关系如图所示。
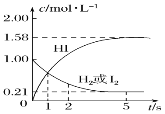
请回答下列问题:
(1)V=________;反应从开始到平衡时,这段时间内平均反应速率v(HI)=_______。
(2)下列说法中可以说明反应2HI(g) ⇌H2(g)+I2(g)已达到平衡状态的是___。
A.单位时间内生成n mol H2的同时生成2n mol HI
B.温度和体积一定时,容器内压强不再变化
C.条件一定,混合气体的平均相对分子质量不再变化
D.温度和压强一定时,混合气体的密度不再变化
(3)当反应H2(g)+I2(g) ⇌2HI(g)达到平衡状态时,_____(填“吸收”或“放出”)的热量为___。
(4)恒容下,某时刻加入HI(g),HI(g)的转化率_______(填“增大”、“减小”、“不变”)。
(5)压缩体积,平衡向________移动(填“正反应”、“逆反应”、“不”),气体颜色_______(填“变深”、“变浅”、不变”)
-
425℃时,向某V L的密闭容器中充入2molH2(g)和2mol I2(g)发生反应: H2(g)+I2(g) 2HI(g)
2HI(g) =-26.5kJ/mol,测得各物质的物质的量浓度与时间变化的关系如图所示。
=-26.5kJ/mol,测得各物质的物质的量浓度与时间变化的关系如图所示。
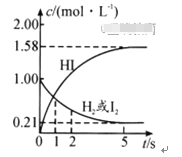
请回答下列问题:
(1)V=__________.
(2)该反应达到最大限度了的时间是____________,该时间内平均反应速率v(HI)=________________。
(3)该反应达到平衡状态时,__________(填“吸收”或“放出”)的热量为__________。
-
425℃时,向某V L的密闭容器中充入2molH2(g)和2mol I2(g)发生反应: H2(g)+I2(g) 2HI(g)
2HI(g) =-26.5kJ/mol,测得各物质的物质的量浓度与时间变化的关系如图所示。
=-26.5kJ/mol,测得各物质的物质的量浓度与时间变化的关系如图所示。
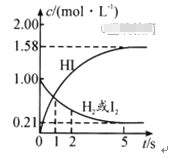
请回答下列问题:
(1)V=__________.
(2)该反应达到最大限度了的时间是____________,该时间内平均反应速率v(HI)=________________。
(3)该反应达到平衡状态时,__________(填“吸收”或“放出”)的热量为__________。
-
425℃时,向某V L的密闭容器中充入2molH2(g)和2mol I2(g)发生反应: H2(g)+I2(g) 2HI(g)
2HI(g) =-26.5kJ/mol,测得各物质的物质的量浓度与时间变化的关系如图所示。
=-26.5kJ/mol,测得各物质的物质的量浓度与时间变化的关系如图所示。

请回答下列问题:
(1)V=__________.
(2)该反应达到最大限度了的时间是____________,该时间内平均反应速率v(HI)=________________。
(3)该反应达到平衡状态时,__________(填“吸收”或“放出”)的热量为__________。
-
碘与氢气反应的热化学方程式是
①I2(g) + H2(g) 2HI(g) △H=-9.48 kJ·mol-1
2HI(g) △H=-9.48 kJ·mol-1
②I2(s) + H2(g) 2HI(g) △H= +26.48 kJ·mol-1
2HI(g) △H= +26.48 kJ·mol-1
下列说法正确的是
A.②的反应物总能量比①的反应物总能量低
B.I2(s) = I2(g) △H= +17.00 kJ·mol-1
C.①的产物比②的产物稳定
D.1mol I2(g)中通入1 mol H2(g),发生反应时放热9.48 kJ
-
碘与氢气反应的热化学方程式是
① I2(g) + H2(g) 2HI(g) △H=-9.48 kJ·mol-1
2HI(g) △H=-9.48 kJ·mol-1
② I2(s) + H2(g) 2HI(g) △H=+26.48 kJ·mol-1
2HI(g) △H=+26.48 kJ·mol-1
下列说法正确的是
A.①的产物比②的产物稳定
B.I2(s)= I2(g) △H= +17.00kJ·mol-1
C.②的反应物总能量比①的反应物总能量低
D.1 mol I2(g)中通入1 mol H2(g),发生反应时放热9.48 kJ
H2(g)+
I2(s) △H = - 26.5kJ/mol,可知通入 1mol HI 在密闭容器中分解后可放出 26.5kJ 的能量




