-
乙烯是合成食品外包装材料聚乙烯的单体,可以由丁烷裂解制备。
主反应:C4H10(g,正丁烷) C2H4(g)+C2H6(g) ΔH1
C2H4(g)+C2H6(g) ΔH1
副反应:C4H10(g,正丁烷) CH4(g)+C3H6(g) ΔH2 回答下列问题:
CH4(g)+C3H6(g) ΔH2 回答下列问题:
(1)化学上,将稳定单质的能量定为0,生成稳定化合物时的释放或吸收能量叫生成热,生成热可表示该物质相对能量。下表为25℃、101 kPa下几种有机物的生成热:
| 物质 | 甲烷 | 乙烷 | 乙烯 | 丙烯 | 正丁烷 | 异丁烷 |
| 生成热/kJ·mol1 | −75 | −85 | 52 | 20 | −125 | −132 |
①表格中的物质,最稳定的是________________(填结构简式)。
②上述反应中,ΔH1=____________kJ·mol1。
(2)一定温度下,在恒容密闭容器中投入一定量正丁烷发生反应生成乙烯。下列情况表明该反应达到平衡状态的是_________________(填代号)。
A.气体密度保持不变 B. 保持不变
保持不变
C.反应热不变 D.正丁烷分解速率和乙烷消耗速率相等
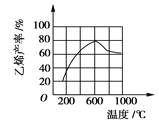
(3)向密闭容器中充入丁烷,在一定条件(浓度、催化剂及压强等)下发生反应,测得乙烯产率与温度关系如图所示。温度高于600℃时,
随着温度升高,乙烯产率降低,可能的原因是____________(填代号)。
A.平衡常数降低 B.活化能降低
C.催化剂活性降低 D.副产物增多
(4)在一定温度下向1 L恒容密闭容器中充入2 mol正丁烷,反应生成乙烯和乙烷,经过10 min 达到平衡状态,测得平衡时气体压强是原来的1.75倍。
①0~10 min内乙烷的生成速率v(C2H6)为___________mol·L1·min1。
②上述条件下,正丁烷的平衡转化率为_____________;该反应的平衡常数K为____。
(5)丁烷−空气燃料电池以熔融的K2CO3(其中不含O2和HCO3-)为电解质,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池的正极反应式为26CO2+13O2+52e=6CO32-,负极反应式为____________________。
-
乙烯是合成食品外包装材料聚乙烯的单体,可以由丁烷裂解制备。裂解的副反应为C4H10(g,正丁烷) CH4(g)+C3H6(g),请回答下列问题:
CH4(g)+C3H6(g),请回答下列问题:
(1)化学上,将稳定单质的能量定为0,由元素的单质化合成单一化合物时的反应热叫该化合物的生成热,生成热可表示该物质相对能量。25 ℃、101 kPa几种有机物的生成热如下表所示:
| 物质 | 甲烷 | 乙烷 | 乙烯 | 丙烯 | 正丁烷 | 异丁烷 |
| 生成热/kJ· mol-1 | -75 | -85 | 52 | 20 | -125 | -132 |
由正丁烷裂解生成乙烯的热化学方程式为_____________________________。
(2)一定温度下,在恒容密闭容器中投入一定量正丁烷发生反应生成乙烯。
下列情况能说明该反应达到平衡状态的是________(填标号)。
A.气体密度保持不变 B.c(C2H4)·c(C2H6)/c(C4H10)保持不变
C.反应热保持不变 D.正丁烷分解速率和乙烷消耗速率相等
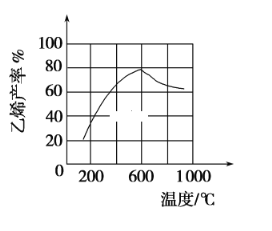
(3)向密闭容器中充入正丁烷,在一定条件(浓度、催化剂及压强等)下发生反应,测得乙烯产率与温度关系如图所示。温度高于600℃时,随着温度升高,乙烯产率降低,可能的原因是____________。
(4)在一定温度下向10 L恒容密闭容器中充入2 mol正丁烷,反应生成乙烯和乙烷,经过10 min达到平衡状态,测得平衡时气体压强是原来的1.75倍。
①0~10 min内乙烷的生成速率v(C2H6)=________ mol·L-1·min-1。
②上述条件下,正丁烷的平衡转化率为_______,该反应的平衡常数K为_____。
(5)丁烷空气燃料电池以熔融的K2CO3(其中不含O2-和HCO3-)为电解质,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池的正极反应式为26CO2+13O2+52e-===26CO32-,则负极反应式为_________________________。
-
乙烯的产量是衡量一个国家石油化工水平的重要标志。工业上常用丁烷裂解制备乙烯。
主反应:C4H10(g,正丁烷) C2H4(g)+C2H6(g) ΔH1
C2H4(g)+C2H6(g) ΔH1
副反应:C4H10(g,正丁烷) CH4(g)+C3H6(g) ΔH2
CH4(g)+C3H6(g) ΔH2
回答下列问题:
(1)化学上,将稳定单质的能量定为0,由元素的单质化合成单一化合物时的反应热叫该化合物的生成热,生成热可表示该物质相对能量。下表为25℃、101kPa下儿种有机物的生成热:
| 物质 | 甲烷 | 乙烷 | 乙烯 | 丙烯 | 正丁烷 | 异丁烷 |
| 生成热/kJ·mol-1 | -75 | -85 | 52 | 20 | -125 | -132 |
①上述反应中,ΔH1=___kJ·mol-1。
②若忽略副反应,相同条件下采用异丁烷裂解制取一定量的乙烯,其能耗比采用正丁烷__(填“高”或“低”)。
(2)一定温度下,在恒压密闭容器中投入一定量正丁烷发生反应生成乙烯。
①下列情况表明该反应达到平衡状态的是___(填代号)。
a.气体密度保持不变
b. 保持不变
保持不变
c.ΔH不变
d.正丁烷分解速率和乙烷消耗速率相等
②为了同时提高反应速率和转化率,可采用的措施是__。
(3)向密闭容器中充入丁烷,在一定条件(浓度、催化剂及压强等)下发生反应,测得乙烯产率与温度关系如图所示。
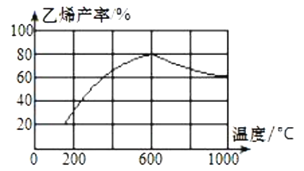
温度高于600℃时,随着温度升高,乙烯产率降低,可能的原因是__。
(4)在一定温度下向1L恒容密闭容器中充入2mol正丁烷,容器内压强为P0,反应生成乙烯和乙烷,经过10min达到平衡状态,此温度下用各组分的分压表示的平衡常数K(p)=0.5P0用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),则0~10min内乙烯的生成速率v(C2H4)为__mol·L-1。
-
PVDC是聚偏二氯乙烯的英文缩写,可作为保鲜食品的包装材料,它的结构简式为 。下列说法中错误的是
。下列说法中错误的是
A.PVDC由单体CCl2=CH2发生加聚反应合成
B.PVDC由单体CCl3CH3发生缩聚反应合成
C.PVDC有很大缺点,如在空气中熔融可分解出HCl等,会污染空气
D.PVDC的单体可发生加成、取代、氧化、消去等反应
-
聚偏二氯乙烯(PVDC)的结构简式为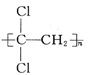 ,它可以承受高温蒸煮,也可作为保鲜食品的包装材料,下列有关PVDC的叙述错误的是
,它可以承受高温蒸煮,也可作为保鲜食品的包装材料,下列有关PVDC的叙述错误的是
A. 没有固定的熔点,沸点 B. 聚合度为n,属于混合物
C. 单体可由乙烯与氯气加成制得 D. 单体可发生加成、取代、氧化、消去等反应
-
材料是人类赖以生存和发展的重要物质基础,它为人们的生活增添了色彩。
(1)三大合成材料是指合成橡胶、____________和________________。包装食品的聚乙烯塑料袋可以进行热封口,该塑料具有____________(填“热塑”或“热固”)性。
(2)下列三种材料中,灼烧时会产生烧焦羽毛臭味的是____________。(填字母代号,下同)
A.尼龙 B.羊毛 C.棉花
(3)陶瓷的发明是人类早期科学技术发展史上的重要里程碑,陶瓷属于____________
A.金属材料 B.无机非金属材料 C.有机高分子材料
(4)下列有关金属防护的方法不正确的是____________
A.户外健身器材上刷油漆 B.铁制衣架外面包上一层塑料层
C.机械轴承上涂润滑油 D.地下埋设的铁管上连接铜块
-
下列关于有机化合物的说法正确的是( )
A.2-甲基丁烷也称为异丁烷
B.聚氯乙烯的单体属于不饱和烃
C.用Na2CO3溶液一种试剂能区分乙酸、乙醇、苯、四氯化碳四种物质
D.由CH2=CH2制备(合成)草酸二乙酯,所发生的化学反应类型有加成反应、取代反应、氧化反应、消去反应
-
下列说法不正确的是( )
A.高吸水性树脂属于功能高分子材料
B.食品包装袋、食物保鲜膜等材料的主要成份是聚乙烯
C.人造纤维、合成纤维和光导纤维都是有机高分子化合物
D.高分子化合物的结构大致可以分为线型结构、支链型结构和网状结构三类
-
在下列有关说法中正确的是 ( )
①相同质量的CH4、C2H4、C2H2完全燃烧时耗O2量的关系为CH4 > C2H4 >C2H2
②对于任意比混合的乙烯、丙烯和环丁烷混合气体在足量氧气中燃烧,只要混合气体的 质量不变,完全燃烧后产生的CO2和H2O的量也不改变
③对于任意比混合的C2H4、C2H6、C2H2混合气体,只要混合气体物质的量不变,完全燃烧后产生的CO2物质的量也不改变
④某有机物在足量氧气中燃烧后产生CO2与H2O的物质的量之比为2:3,则该有机物的类型肯定为烷烃
A. ①②③ B. ①②③④ C. ②③ D. 以上组合均不正确
-
在下列有关说法中正确的是
①相同质量的CH4、C2H4、C2H2完全燃烧时耗O2量的关系为CH4 > C2H4 >C2H2
②对于任意比混合的乙烯、丙烯和环丁烷混合气体在足量氧气中燃烧,只要混合气体的质量不变,完全燃烧后产生的CO2和H2O的量也不改变
③对于任意比混合的C2H4、C2H6、C2H2混合气体,只要混合气体物质的量不变,完全燃烧后产生的CO2物质的量也不改变
④某有机物在足量氧气中燃烧后产生CO2与H2O的物质的量之比为2:3,则该有机物的类型肯定为烷烃
A.①②③ B.①②③④ C. ②③ D.以上组合均不正确
C2H4(g)+C2H6(g) ΔH1
CH4(g)+C3H6(g) ΔH2 回答下列问题:
保持不变



 ,它可以承受高温蒸煮,也可作为保鲜食品的包装材料,下列有关PVDC的叙述错误的是
,它可以承受高温蒸煮,也可作为保鲜食品的包装材料,下列有关PVDC的叙述错误的是