现有如下两个装置,其中锌片和铜片均为足量,请回答相关问题。
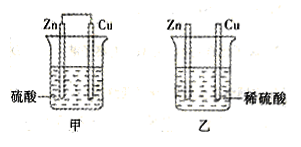
(1)装置乙中可观察到的现象是_______。
(2)若甲中所用硫酸为80%的浓硫酸,开始阶段可观察到的现象是_____,锌电极上发生的反应类型是_____(填“氧化反应”或“还原反应”),此时的总反映化学方程式为_______。一段时间后装置中发生了另一个反应,原因是_______,与开始阶段相比锌片上的反应是否发生了变化______(填“是”或“否”)
高一化学简答题中等难度题
现有如下两个装置,其中锌片和铜片均为足量,请回答相关问题。

(1)装置乙中可观察到的现象是_______。
(2)若甲中所用硫酸为80%的浓硫酸,开始阶段可观察到的现象是_____,锌电极上发生的反应类型是_____(填“氧化反应”或“还原反应”),此时的总反映化学方程式为_______。一段时间后装置中发生了另一个反应,原因是_______,与开始阶段相比锌片上的反应是否发生了变化______(填“是”或“否”)
高一化学简答题中等难度题
现有如下两个装置,其中锌片和铜片均为足量,请回答相关问题。

(1)装置乙中可观察到的现象是_______。
(2)若甲中所用硫酸为80%的浓硫酸,开始阶段可观察到的现象是_____,锌电极上发生的反应类型是_____(填“氧化反应”或“还原反应”),此时的总反映化学方程式为_______。一段时间后装置中发生了另一个反应,原因是_______,与开始阶段相比锌片上的反应是否发生了变化______(填“是”或“否”)
高一化学简答题中等难度题查看答案及解析
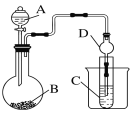
为检验炭粉与浓硫酸反应的产物设计如下装置,回答相关问题:
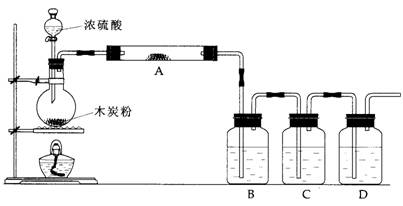
(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气________
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:
________
(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用
A中加入的试剂和作用是______ _____
B中加入的试剂和作用是____ ____________
D中加入的试剂和作用是__ ___________
(4)实验时,C中应观察到的现象是______________________
高一化学实验题简单题查看答案及解析
(8分)以下甲、乙、丙为探究原电池原理的有关装置,试回答下列问题:
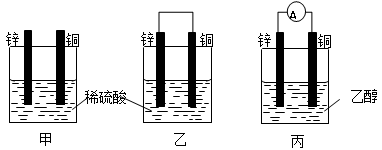
(1)甲中预计可以观察到得现象是:铜片上 (填“有”或“没有”)气泡产生,锌片上 (填“有”或“没有”)气泡产生。
(2)乙中锌为原电池的 极,电极反应是 ;铜为原电池的 极,电极反应是 。原电池总反应为
(3)丙中电流计A的指针是否发生偏转: (填“是”或“否”)
高一化学填空题中等难度题查看答案及解析
(8分)科学探究的基本程序包括形成问题、建立假设、设计研究方案、检验假设、表达或交流结果等。请根据课本中的《活动与探究》相关知识回答问题。
某同学应用如下所示装置研究气体的性质。现有某气体,其主要成分是氯气,还含有少量空气和水蒸气。
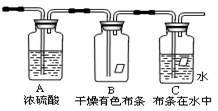
请回答:该项研究的主要目的是__ _。浓硫酸的作用是_ __。B、C中能观察到的实验现象是_________。从物质性质方面来看,这样的实验设计方案不符合绿色化学的理念,你认为该如何改进?_____。
高一化学实验题中等难度题查看答案及解析
用铜片、锌片和稀硫酸及若干其他器材组合成一个原电池,画出装置图并回答 (1)画出装置图。
(2)从理论上讲,预期看到的现象是
(3)实验过程中,观察到锌片上有少量气泡冒出,铜片上有大量气泡冒出。试解释:。
(4)此电池的负极是,正极的电极反应式是。
(5)该电池工作一段时间,将两个电极小心取出洗涤并晾干,经称量发现锌片比原来减少3.25 g。请计算理论上导线中共通过了________mol电子
高一化学实验题简单题查看答案及解析
观察图中 A、B、C 三个装置,回答下列问题:
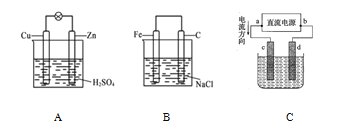
(1)把一块纯净的锌片插入装有稀硫酸的烧杯中,可观察到锌片上有气泡,再平行插入一铜片,可观察到铜片上_________(填“有”或“没有”)气泡产生。用导线把锌片和碳棒连接起来组成一个原电池(图A),正极的反应式为_______。
(2) 如果烧杯中最初装入的是 500 mL 2 mol·L-1 硫酸溶液,构成铜锌原电池,当收集到 11.2 L(标准状况下)H2 时,溶液体积变化忽略不计,则烧杯内溶液中硫酸的物质的量的浓度为_______mol/L。
(3) 如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(图 B),放置数天后,铁片生锈。负极反应式为_______。
(4) 图 C 是电解 CuCl2 溶液的装置,其中 c、d 为石墨电极。
①正极为_______(填“a”或“b”)。
②阳极电极反应式为_______,检验该阳极产物的方法是将_______试纸靠近电极。
③电解一段时间后发现阴极增重 6.4 g,若该电解反应所需的电子全部由氢氧燃料电池提供,则至少需要消耗_______L 氢气(标准状况下)才能满足需要。
高一化学填空题中等难度题查看答案及解析
下面这个实验为“套管实验”,实验装置如下图,请观察实验装置。分析实验原理,并回答下列问题:
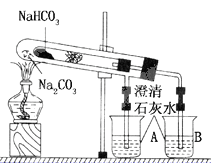
(1)整个实验过程中,能观察到①烧杯A中的现象:②烧杯B中的现象______________;
(2)实验结束时的操作是______________
(3)写出实验过程中发生反应的化学方程式______________;
(4)该实验可证明稳定性:NaHCO3 Na2CO3(填大于,小于或等于),证明稳定性比较时,能否将NaHCO3、Na2CO3的位置互换 (填能或不能)。
高一化学实验题困难题查看答案及解析
化学是一门实验为基础的科学。请回答下列问题:
(1)利用如图装置可验证浓、稀硝酸氧化性强弱,请完成 实验操作,回答相关问题:

①实验操作过程:固定铜片,打开分液漏斗活塞及止水夹2,从不对称U形管1、2长管口处分别注入稀硝酸、浓硝酸,液面与双孔橡皮塞接触,然后,关闭分液漏斗玻璃活塞、止水夹1、2。此后可观察到现象______;然后打开止水夹1,会发现不对称U形管2中长导管口无色气泡变红棕色,浓硝酸逐渐变黄(说明稀硝酸不能氧化这种无色气体而浓硝酸可以)。
②请用一个化学方程式体现该实验验证浓、稀硝酸氧化性强弱的原理_________。
(2)利用如图装置可以验证非金属性的变化规律。
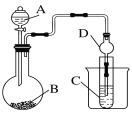
①干燥管D的作用是__________。
②实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B中所装药品分别为________、________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为______________________。
③若要证明非金属性:Cl > C >Si,则A中加入试剂____________、B中加Na2CO3、C中加入试剂______________。
高一化学实验题困难题查看答案及解析
化学是一门实验为基础的科学。请回答下列问题:
(1)利用如图装置可验证浓、稀硝酸氧化性强弱,请完成 实验操作,回答相关问题:
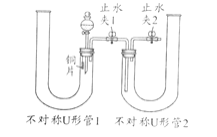
①实验操作过程:固定铜片,打开分液漏斗活塞及止水夹2,从不对称U形管1、2长管口处分别注入稀硝酸、浓硝酸,液面与双孔橡皮塞接触,然后,关闭分液漏斗玻璃活塞、止水夹1、2。此后可观察到现象______;然后打开止水夹1,会发现不对称U形管2中长导管口无色气泡变红棕色,浓硝酸逐渐变黄(说明稀硝酸不能氧化这种无色气体而浓硝酸可以)。
②请用一个化学方程式体现该实验验证浓、稀硝酸氧化性强弱的原理_________。
(2)利用如图装置可以验证非金属性的变化规律。
①干燥管D的作用是__________。
②实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B中所装药品分别为________、________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为______________________。
③若要证明非金属性:Cl > C >Si,则A中加入试剂____________、B中加Na2CO3、C中加入试剂______________。
高一化学实验题困难题查看答案及解析
I.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学们分别设计了如下图甲、乙所示的实验装置。请回答相关问题:
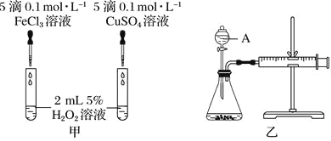
(1)定性甲所示装置可通过观察_________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_________。
(2)定量如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为_______,实验中需要测量的数据是________。
II.以下是某研究小组探究影响反应速率部分因素的相关实验数据。
| 实验 序号 | H2O2溶液浓度/% | H2O2溶液体积/mL | 温度/℃ | MnO2用量/g | 收集O2的体积/mL | 反应所需时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | 2 | 49.21 | |
| ④ | 30 | 5 | 55 | 2 | 10.76 |
(3)通过实验①和②对比可知,化学反应速率与_____有关;从实验③和④对比可知,化学反应速率与温度的关系是_____。
高一化学实验题中等难度题查看答案及解析