-
在某温度T℃时,将N2O4、NO2分别充入两个各为1L的密闭容器中,反应过程中浓度变化如下[2NO2(g) N2O4(g) △H<0]:
N2O4(g) △H<0]:
| 容器 | 物质 | 起始浓度/(mol L-1) L-1) | 平衡浓度/(mol L-1) L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 |
| Ⅱ | N2O4 | 0 | 0.0142 |
| NO2 | 0.100 | 0.0716 |
下列说法不正确的是( )
A. 平衡时,Ⅰ、Ⅱ中反应的转化率a(N2O4)>a(NO2)
B. 平衡后,升高相同温度,以N2O4表示的反应速率v(Ⅰ)<v(Ⅱ)
C. 平衡时,Ⅰ、Ⅱ中正反应的平衡常数K(I)=
D. 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深
-
在某温度T℃时,将N2O4、NO2分别充入两个各为1L的密闭容器中,反应过程中浓度变化如下[2NO2(g) N2O4(g) △H<0]:
N2O4(g) △H<0]:
| 容器 | 物质 | 起始浓度/(mol L-1) L-1) | 平衡浓度/(mol L-1) L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 |
| Ⅱ | N2O4 | 0 | 0.0142 |
| NO2 | 0.100 | 0.0716 |
下列说法不正确的是( )
A. 平衡时,Ⅰ、Ⅱ中反应的转化率 (N2O4)>(NO2)
(N2O4)>(NO2)
B. 平衡后,升高相同温度,以N2O4表示的反应速率 (Ⅰ)<
(Ⅰ)< (Ⅱ)
(Ⅱ)
C. 平衡时,Ⅰ、Ⅱ中正反应的平衡常数K(Ⅰ)=
D. 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深
-
在某温度T℃时,将N2O4、NO2分别充入两个各为1L的密闭容器中,反应过程中浓度变化如下[2NO2(g) N2O4(g) △H<0]:
N2O4(g) △H<0]:
| 容器 | 物质 | 起始浓度/(mol L-1) L-1) | 平衡浓度/(mol L-1) L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 |
| Ⅱ | N2O4 | 0 | 0.0142 |
| NO2 | 0.100 | 0.0716 |
下列说法不正确的是( )
A. 平衡时,Ⅰ、Ⅱ中反应的转化率a(N2O4)>a(NO2)
B. 平衡后,升高相同温度,以N2O4表示的反应速率v(Ⅰ)<v(Ⅱ)
C. 平衡时,Ⅰ、Ⅱ中正反应的平衡常数K(I)=
D. 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深
-
在100℃时,将N2O4、NO2分别充入两个各为1 L的密闭容器中,反应过程中浓度变化如下:2NO2(g)  N2O4(g) ΔH <0
N2O4(g) ΔH <0
| 容器 | 物质 | 起始浓度/(mol•L-1) | 平衡浓度/(mol•L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 |
| Ⅱ | N2O4 | 0 | 0.014 |
| NO2 | 0.100 | 0.072 |
下列说法正确的是
A. 平衡时,Ⅰ、Ⅱ中反应物的转化率α(N2O4)<α(NO2)
B. 平衡时,Ⅰ、Ⅱ中上述正反应的平衡常数K(Ⅰ) = 2K(Ⅱ)
C. 平衡后,升高相同温度,以N2O4表示的反应速率ν(Ⅰ)<ν(Ⅱ)
D. 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深
-
8分)一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8 mol NO2,发生如下反应:2NO2(红棕色) N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答:
N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如下图,按下列要求作答:
(1)在该温度下,反应的化学平衡常数表达式为:________
(2)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率: ________mol·L-1·s-1
(3)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?答:
(4)t1时,正反应速率 ________ (填“>”、“<”或“=”)逆反应速率
(5)维持容器的温度不变,若缩小容器的体积,则平衡向 移动
(填“正反应方向”、“逆反应方向”或“不移动”)
(6)维持容器的体积不变,升高温度,达到新平衡时体系的颜色 ________ ________
(填“变深”、“变浅”或“不变”)
-
在一定温度下,容积固定的密闭容器中,通入一定量的N2O4,发生反应N2O4(g)  2NO2(g),体系中各物质浓度随时间变化如图所示,则下列叙述错误的是
2NO2(g),体系中各物质浓度随时间变化如图所示,则下列叙述错误的是

A. 若温度升高,混合气体的颜色变深
B. 在该温度下反应2NO2(g)  N2O4(g)的平衡常K为25/9
N2O4(g)的平衡常K为25/9
C. 反应达平衡后,将反应容器的容积减少一半,平衡向正反应方向移动
D. 反应达平衡后,向此容器中通入NO2气体,则c(NO2)增大
-
在容积为1.00 L的密闭容器中,充入一定量的N2O4,发生反应N2O4(g) 2NO2(g),随着温度升高,混合气体的颜色变深。体系中各物质的浓度变化与时间关系如图所示。下列说法正确的是
2NO2(g),随着温度升高,混合气体的颜色变深。体系中各物质的浓度变化与时间关系如图所示。下列说法正确的是
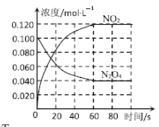
A.反应的△H <0
B.在 0〜60s 时段,反应速率v(N2O4)=0.001mol·L-1·s-1
C.平衡时,反应的平衡常数K=0.240
D.T1℃时平衡后将温度变为T2℃,测得c(N2O4)降低,则T1>T2
-
往恒容密闭容器中通入一定量N2O4,发生反应N2O4(g) 2NO2(g),随温度升高,气体颜色变深。如图表示该反应平衡时有关物理量Y随某条件X(其他条件不变)变化的 规律。X、Y分别是( )
2NO2(g),随温度升高,气体颜色变深。如图表示该反应平衡时有关物理量Y随某条件X(其他条件不变)变化的 规律。X、Y分别是( )
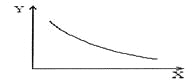
A. 温度T,逆反应速率v B. 温度T,气体的密度
C. 压强P,平衡常数K D. 压强P,N2O4转化率
-
一定温度下,2L密闭容器中充入0.40 mol N2O4,发生反应:N2O4(g) 2NO2(g),一段时间后达到平衡,测得数据如下:
2NO2(g),一段时间后达到平衡,测得数据如下:
| 时间/s | 20 | 40 | 60 | 80 | 100 |
| c(NO2 )/(mol/L) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
请回答:
(1)20 s内,v(NO2)=____________mol·L-1·s-1。
(2)升高温度时,气体颜色加深,则正反应是____________(填“放热”或“吸热”)反应。
(3)该温度下反应的化学平衡常数数值为_____________。
(4)相同温度下,若开始时向该容器中充入的是0.20 molN2O4和0.40molNO2,则达到平衡后,c(NO2)=_____________。
-
已知N2O4(g) 2NO2(g) ΔH=+57.20 kJ/mol,t℃时,将一定量的NO2、N2O4充入一个容积为2 L的恒容密闭容器中,浓度随时间变化关系如下表所示:
2NO2(g) ΔH=+57.20 kJ/mol,t℃时,将一定量的NO2、N2O4充入一个容积为2 L的恒容密闭容器中,浓度随时间变化关系如下表所示:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| c(X)/(mol/L) | 0.2 | c | 0.6 | 0.6 | 1.0 | c1 | c1 |
| c(Y)/(mol/L) | 0.6 | c | 0.4 | 0.4 | 0.4 | c2 | c2 |
下列推断不正确的是
A. c(X)代表NO2的浓度
B. 20min时改变的条件是向容器中加入0.8molNO2
C. 该反应的平衡常数K=0.9 mol/L
D. 25min后混合气体的平均摩尔质量为64.4g·mol-1
N2O4(g) △H<0]:
(N2O4)>(NO2)
(Ⅰ)<
(Ⅱ)


