-
已知:25℃时,下列4种溶液.请回答下列问题.
A.0.01mol•L﹣1氨水 B.0.01mol•L﹣1 NaOH溶液
C.pH=2的CH3COOH溶液 D.pH=2的HCl溶液
(1)①4种溶液中,水的电离程度最大的是 (填序号).
②若将C、D溶液分别稀释10倍,pH变化如图,曲线I对应的溶液为 (填序号).图中a、b、c三点对应溶液的导电能力由强到弱的顺序是 (用a、b、c表示)
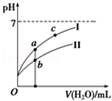
③若将VmL的D溶液滴入到45mL的B溶液中充分反应后,溶液PH=3,则V= mL(溶液体积变化忽略不计).
(2)请设计实验证明CH3COOH为弱酸 .
(3)相同体积的C溶液①和D溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是 .(请填序号)
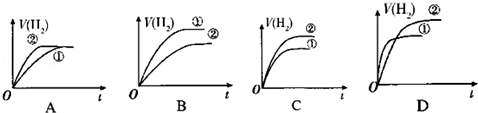
-
完成下列问题:
(1)25℃时有下列4种溶液:
A.0.01mol/L氨水 B.0.01mol/LNaOH溶液
C.pH=2的CH3COOH溶液 D.pH=2的HCl溶液
请回答下列问题:
①上述4种溶液中,水的电离程度最大的是________(填序号)。
②若将B、C溶液等体积混合,所得溶液pH_______7(填“>”、“<”或“=”)
(2)已知25℃时
| 物质 | H3PO2 | H2S | 一元酸HA |
| Ka | Ka=5.9×10-2 | Ka1=9.1×10-8 Ka2=1.1×10-12 | Ka=1.1×10-10 |
①一元酸H3PO2的电离方程式为_________________________。
②H2S溶液与NaA溶液反应的化学方程式为________________。
③经测定,25℃时0.01mol/LNa2S溶液的pH为11,则c(H+)+c(HS-)+2c(H2S)=______。
④0.1mol/L的NaHS溶液,测得溶液显_______。则该溶液中c(H2S)____c(S2-)(填“>”、“<”或“=”),作出上述判断的依据是__________(用计算和文字解释)。
(3)①25℃时,亚硝酸的电离常数为Ka=1.0×10-5,0.2mol/L的HNO2溶液与0.1mol/L的NaOH溶液等体积混合后,恢复到25℃,混合溶液中各离子和HNO2分子浓度由大到小的顺序为_____________。
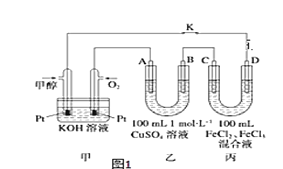
(4)如图是甲醇燃料电池工作示意图,其中A,B,D均为石墨电极,C为铜电极。
①甲中负极的电极反应式____________________。
②乙中B极的电极反应式____________________。
③丙中C极的电极反应式___________________。
-
现有浓度均为0.01mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水。请回答下列问题:
(1)①、②、③、④四种溶液中,水电离出的c(H+)由大到小的顺序是_________(填序号)。
(2)④、⑤、⑥、⑦四种溶液中,c(NH4+)由大到小的顺序是_______(填序号)。
(3)将③和④按体积比1:2混合后,混合液中各离子浓度由大到小的顺序是_______。
(4)已知T℃时,③溶液的pH=11,该温度下,水的离子积Kw=______________;该温度下,将pH之和为13的NaOH溶液和醋酸溶液等体积混合后,所得溶液呈____(填“酸”“碱”或“中”)性。T℃时,将aL pH=11的NaOH溶液与bL pH=1的H2SO4溶液混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a:b=________。
-
现有室温下浓度均为0.01mol/L的几种溶液:①盐酸 ②醋酸③氨水④ NaOH溶液。回答下列问题:
(1)②的电离方程式为________ ; ③,④中水的电离程度较大的是______
(2)室温下,溶液①中由水电离产生c(H+)=______;当温度升高到100摄氏度时,(Kw=1×10-12)溶液④的pH= ______
(3)将①、③等体积混合,所得溶液呈______ (填酸,碱或中)性。
(4)将②、④等体积混合后,若溶液呈中性,则消耗两溶液的体积为②_____ ④(填“>”、“<”或“=”)
(5)室温时,若用标准溶液①滴定④,滴定过程中,需要加入_______作指示剂,滴定终点的判断方法是_________。
-
溶液的酸碱性可用酸度(AG)表示,已知AG =lg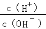 ,室温下将0.01mol•L﹣l盐酸逐滴滴入20.00mL 0
,室温下将0.01mol•L﹣l盐酸逐滴滴入20.00mL 0 .01 mol•L﹣l氨水中,溶液的AG变化如图所示,下列说法正确的是
.01 mol•L﹣l氨水中,溶液的AG变化如图所示,下列说法正确的是
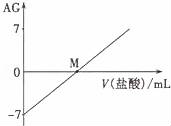
A.室温下,0.01 mol•L﹣l盐酸的AG=12
B.M点时溶液中:c(NH4+)=c(Cl﹣)
C.M点加入盐酸的体积大于20.00 mL
D.M点以后NH4+的水解程度逐渐增大
-
已知t ℃时,0.01 mol/L NaOH溶液的pH=11,0.1 mol/L的HA溶液中c(H+)/c(OH-)=109
请回答下列问题:
(1)该温度下,水的离子积Kw=_____,0.1 mol/L的HA溶液中水电离出的c(OH-)=_____。
(2)在室温下,将pH之和为14的NaOH溶液和HA溶液等体积混合后,所得溶液呈_____(填“酸”“碱”或“中”)性。
(3)在室温下,蒸馏水稀释0.01 mol/L HA溶液时,下列呈减小趋势的是_____。
A.水的电离程度 B.c(HA)/c(A-)
C.溶液中c(H+)和c(OH-)的乘积 D.溶液中c(A-)·c(HA)的值
(4)室温下,取pH=2的盐酸和HA溶液各100 mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示:
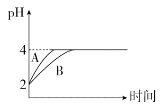
①图中表示HA溶液pH变化曲线的是____(填“A”或“B”)。
②设盐酸中加入Zn的质量为m1,HA溶液中加入Zn的质量为m2,则m1_____m2(填“>”“<”或“=”)。
(5)室温下,取0.01 mol/L的盐酸和HA溶液各100 mL,分别滴加0.01 mol/LNaOH溶液至恰好完全反应,所需NaOH溶液的体积前者____后者(填“>”“<”或“=”)。
-
已知t ℃时,0.01 mol/L NaOH溶液的pH=11,0.1 mol/L的HA溶液中c(H+)/c(OH-)=109
请回答下列问题:
(1)该温度下,水的离子积Kw=_____,0.1 mol/L的HA溶液中水电离出的c(OH-)=_____。
(2)在室温下,将pH之和为14的NaOH溶液和HA溶液等体积混合后,所得溶液呈_____(填“酸”“碱”或“中”)性。
(3)在室温下,蒸馏水稀释0.01 mol/L HA溶液时,下列呈减小趋势的是_____。
A.水的电离程度 B.c(HA)/c(A-)
C.溶液中c(H+)和c(OH-)的乘积 D.溶液中c(A-)·c(HA)的值
(4)室温下,取pH=2的盐酸和HA溶液各100 mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示:
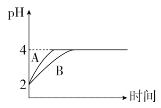
①图中表示HA溶液pH变化曲线的是____(填“A”或“B”)。
②设盐酸中加入Zn的质量为m1,HA溶液中加入Zn的质量为m2,则m1_____m2(填“>”“<”或“=”)。
(5)室温下,取0.01 mol/L的盐酸和HA溶液各100 mL,分别滴加0.01 mol/LNaOH溶液至恰好完全反应,所需NaOH溶液的体积前者____后者(填“>”“<”或“=”)。
-
下列说法中,正确的是
A. 已知25℃时NH4CN水溶液显碱性,则25℃时的电离平衡常数K(NH3·H2O)>K(HCN)
B. 25℃时,Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL0.01 mol·L-1NH4Cl溶液中的Ksp小
C. pH试纸测得新制氯水的pH为4.5
D. FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3
-
常温下,下列混合溶液的pH一定大于7的是
A.0.01mol/L的盐酸和0.01mol/L的NaOH溶液等体积混合
B.pH=3的盐酸和pH=11的氨水溶液等体积混合
C.0.01mol/L的盐酸和0.01mol/L的氨水溶液等体积混合
D.pH=3的醋酸和pH=11的NaOH溶液等体积混合
-
已知硫酸、氨水的密度与所加水量的关系如下图所示:
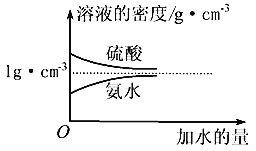
现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
| 溶液 | 溶质的物质的量浓度 | 溶液的密度/g·cm-3 |
| 硫酸 | 4 mol·L-1 | ρ1 |
| 2 mol·L-1 | ρ2 |
| 氨水 | 4 mol·L-1 | ρ3 |
| 2 mol·L-1 | ρ4 |
(1)ρ1、ρ2、ρ3、ρ4由大到小的顺序为:________。
(2)表中2 mol·L-1氨水的质量分数为:________。
(3)将4 mol·L-1的氨水与2 mol·L-1的硫酸等体积混合,所得溶液呈______性(填“酸”、“碱”、“中”);溶液中离子浓度从大到小的顺序是:__________________________。
(4)将20%的硫酸与10%的硫酸等体积混合,所得硫酸溶液的质量分数是______。
A.>15% B.=15% C.<15% D.无法判断
(5)100g浓度为4 mol·L-1的硫酸溶液与_____mL水混合,可以使硫酸的物质的量浓度减小到2 mol·L-1。



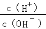 ,室温下将0.01mol•L﹣l盐酸逐滴滴入20.00mL 0
,室温下将0.01mol•L﹣l盐酸逐滴滴入20.00mL 0


