-
乙醛酸(OHC-COOH)是合成名贵香料的原料之一。
I.由乙二醛催化氧化制乙醛酸的反应如下:2OHC-CHO(g)+O2(g)  2OHC-COOH(g)△H
2OHC-COOH(g)△H
(1)已知反应中相关的化学键键能数据如表1:
| 化学键 | O=O | C-O | O-H | C-H |
| 键能(KJ/mol) | 498 | 351 | 465 | 413 |
计算上述反应的△H=____________kJ·mol-1。
(2)一定条件下,按照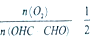 投料比进行上述反应,乙二醛的平衡转化率(a)和催化剂催化效率随温度变化如图1所示。
投料比进行上述反应,乙二醛的平衡转化率(a)和催化剂催化效率随温度变化如图1所示。
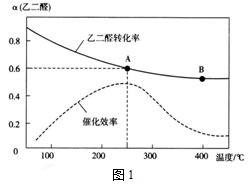
①该反应在A点放出的热量________ B点放出的热量(填“>”、“=”或“<”)
②某同学据图推知,生成乙醛酸的速率:v(A)>v(B),你认为此结论是否正确,简述理由__________。
③图中A点时,乙醛酸的体积分数为_____________。
④为提高乙二醛的平衡转化率,除改变投料比、温度外,还可以采取的措施有__________ (列举一条)。
Ⅱ.利用惰性电极电解饱和乙二酸和稀硫酸溶液也可以制备乙醛酸,原理如右图所示。
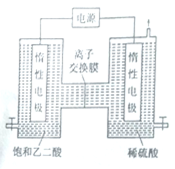
(1)图中的离子交换膜为___________ (填“阳”或“阴”)膜。
(2)稀硫酸的作用为____________。
(3)生成乙醛酸的电极反应式为_______________。
-
已知:乙二醛可被催化氧化为乙醛酸,其反应为2OHC-CHO(g)+O2(g) 2OHC-COOH(g) △H。一定条件下,按照
2OHC-COOH(g) △H。一定条件下,按照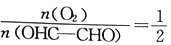 的投料比进行上述反应,乙二醛的平衡转化率(α)和催化剂的催化效率随温度的变化如图所示。下列叙述正确的是
的投料比进行上述反应,乙二醛的平衡转化率(α)和催化剂的催化效率随温度的变化如图所示。下列叙述正确的是
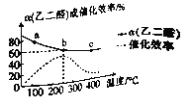
A. △H>0
B. b点时,乙二醛的体积分数为33.33%
C. 生成乙醛酸的速率:v(a)>v(b)>v(c)
D. a、b、c三点中,a点乙醛酸的体积分数最小
-
乙二醇是工业常见的有机原料,常用来制取纺织工业的乙二醛和化妆品行业的乙醛酸。
①乙二醇(HOCH2CH2OH)气相催化氧化法制取乙二醛(OHC-CHO),主要反应为:HOCH2CH2OH(g)+O2(g) OHC—CHO(g)+2H2O(g) ∆H
OHC—CHO(g)+2H2O(g) ∆H
| 化学键 | O—H | C—H | C—O | C=O | O=O | C—C |
| 键能(kJ·mol-1) | 436 | 413 | 356 | 745 | 493 | 346 |
则∆H=_____kJ·mol-1。
②当原料气中氧醇比(氧气和乙二醇的物质的量之比)一定时,乙二醛和副产物CO2的产率与反应温度的关系如图所示,则反应中应控制的适宜温度是___(填字母)。
a.低于450℃
b.450℃~490℃
c.高于495℃
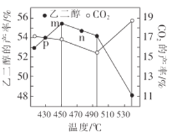
p、m、n三点中____是平衡点,__是逆反应速率最快的点。
③温度超过495℃时,乙二醛的产率直线下降的原因是___。
(2)将乙二醇氧化为乙二酸,再利用乙二酸(HOOCCOOH)通过电解制备乙醛酸,阴极的电极反应式为____。
(3)液相氧化制备乙醛酸是近年研究的热点。向25L某浓度的乙二醛溶液中,加入适量的催化剂V2O5/C,以0.1mol·L-1的流速通入氧气,测得溶液中乙二醛的浓度、溶液的pH随时间变化的关系如图所示:
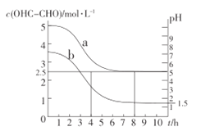
①图中曲线___(填“a”或“b”)表示溶液的pH值随时间变化的曲线。
②V2O5/C表示将催化剂覆盖在纳米碳纤维上,其目的是___。
③写出制备乙醛酸(HOC—COOH)的化学反应方程式:____,根据图中数据算出8h内乙醛酸的平均生成速率v(HOC—COOH)=____;该实验条件下乙醛酸的电离常数Ka=___。
-
乙醛酸(OHCCOOH)是合成名贵高档香料乙基香兰素 的原料之一,可用草酸(HOOCCOOH)电解制备,装置如图所示。下列说法不正确的是( )
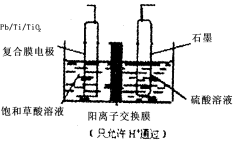
A.电解时石墨电极应与直流电的正极相连
B.阴极反应式为:HOOCCOOH+2H++2e- =OHCCOOH+H2O
C.电解时石墨电极上有O2放出
D.电解一段时间后,硫酸溶液的pH不变化
-
乙醛酸(OHCCOOH)是合成名贵高档香料乙基香兰素的原料之一,可用草酸(HOOCCOOH)电解制备,装置如图所示。下列说法不正确的是
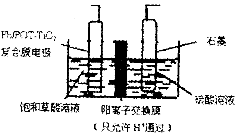
A.电解时石墨电极应与直流电源的正极相连
B.阴极反应式为:HOOCCOOH+2H++2e- =OHCCOOH+H2O
C.电解时石墨电极上有O2放出
D.电解一段时间后,硫酸溶液的pH不变化
-
乙二醛(OHC-CHO)是一种重要的精细化工产品。
Ⅰ.工业生产乙二醛
(1)乙醛(CH3CHO)液相硝酸氧化法
在Cu(NO3)2催化下,用稀硝酸氧化乙醛制取乙二醛,反应的化学方程式为 。该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点是 。
(2)乙二醇(HOCH2CH2OH)气相氧化法
① 已知:OHC-CHO(g)+2H2(g) HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K1
HOCH2CH2OH(g) ΔH=-78 kJ·mol-1 K1
2H2(g)+O2(g) 2H2O(g) ΔH=-484 kJ·mol-1 K2
2H2O(g) ΔH=-484 kJ·mol-1 K2
乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g) OHC—CHO(g)+2H2O(g)的ΔH= kJ·mol-1。相同温度下,该反应的化学平衡常数K= (用含K1、K2的代数式表示)。
OHC—CHO(g)+2H2O(g)的ΔH= kJ·mol-1。相同温度下,该反应的化学平衡常数K= (用含K1、K2的代数式表示)。
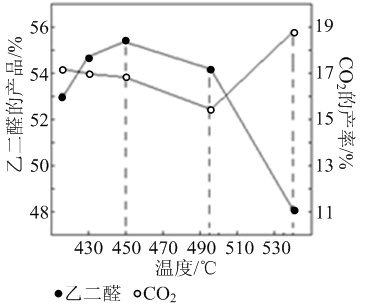
② 当原料气中氧醇比为1.35时,乙二醛和副产物CO2的产率与反应温度的关系如下图所示。反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是 、
Ⅱ.乙二醛电解氧化制备乙醛酸(OHC—COOH)的生产装置如下图所示,通电后,阳极产生的Cl2 与乙二醛溶液反应生成乙醛酸。
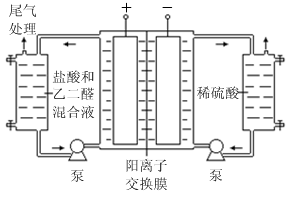
(3)阴极电极式为
(4)阳极液中盐酸的作用,除了产生氯气外,还有
(5)保持电流强度为a A,电解t min,制得乙醛酸m g,列式表示该装置在本次电解中的电流效率η=
(设:法拉第常数为f C·mol-1;η= )
)
-
乙二醛(OHC—CHO)是一种重要的精细化工产品。
Ⅰ. 工业生产乙二醛
(1)乙醛(CH3CHO)液相硝酸氧化法
在Cu(NO3)2催化下,用稀硝酸氧化乙醛制取乙二醛,反应的化学方程式为 。该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点是 。
(2)乙二醇(HOCH2CH2OH)气相氧化法
①已知:OHC—CHO(g) +2H2(g) HOCH2CH2OH(g) △H=−78kJ·mol−1 K1
HOCH2CH2OH(g) △H=−78kJ·mol−1 K1
2H2(g) + O2(g) 2H2O(g) △H=−484kJ·mol−1 K2
2H2O(g) △H=−484kJ·mol−1 K2
乙二醇气相氧化反应HOCH2CH2OH(g) +O2(g) OHC—CHO(g) + 2H2O(g)的△H= kJ·mol−1。相同温度下,该反应的化学平衡常数K= (用含K1、K2的代数式表示)。
OHC—CHO(g) + 2H2O(g)的△H= kJ·mol−1。相同温度下,该反应的化学平衡常数K= (用含K1、K2的代数式表示)。
②当原料气中氧醇比为1.35时,乙二醛和副产物CO2的产率与反应温度的关系如下图所示。反应温度在450~495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是 、 。
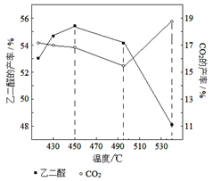
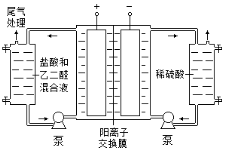
Ⅱ. 乙二醛电解氧化制备乙醛酸(OHC—COOH)的生产装置如下图所示,通电后,阳极产生的Cl2与乙二醛溶液反应生成乙醛酸。
(3)阴极反应式为 。
(4)阳极液中盐酸的作用,除了产生氯气外,还有 。
(5)保持电流强度为a A,电解t min,制得乙醛酸m g,列式表示该装置在本次电解中的电流效率η= 。(设:法拉第常数为f C•mol−1;η= )
)
-
乙醛酸(OHC-COOH)是一种重要的精细化工产品。以高硅铸铁为惰性电极材料,用恒电势电解NaBr溶液间接氧化乙二醛(OHC-CH0)制备乙醛酸: 。装置如图所示。下列说法不正确的是
。装置如图所示。下列说法不正确的是

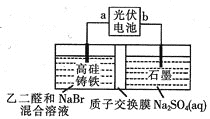
A.电极b为负极,高硅铸铁不损耗
B.阳极的电极反应式为
C.电池正常工作时,左室电解质溶液中 保持不变
保持不变
D.电解过程中,右室溶液的pH逐渐升高
-
胡妥油(D)用作香料的原料,它可由A合成得到:
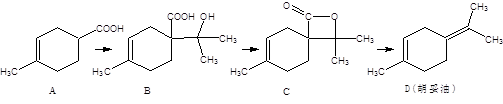
下列说法正确的是A.若有机物A是由异戊二烯和丙烯酸加热得到的,则该反应的反应类型属于加成反应B.有机物B 既能与O2催化氧化生成醛,又能跟NaHCO3溶液反应放出CO2气体C.有机物C 的所有同分异构体中不可能有芳香族化合物存在D.有机物D分子中所有碳原子一定共面
-
乙二醛是一种低级醛,它有着极其活跃的化学反应性,并有广泛的用途。
I.乙二醛的工业制法如下:
(1)乙醛(CH3CHO)液相硝酸氧化法
在Cu(NO3)催化下,用稀硝酸氧化乙醛制取乙二醛,反应的离子方程式为___________。该法具有原料易得、反应条件温和等优点,但也存在比较明显的缺点是____________ 。
(2)乙二醇(HOCH2CH2OH)气相氧化法
①已知: OHC-CHO(g) +2H2(g) HOCH2CH2OH(g) △H=-78kJ/mol K1
HOCH2CH2OH(g) △H=-78kJ/mol K1
2H2(g)+O2(g) 2H2O(g) △H=-484kJ/mol K2
2H2O(g) △H=-484kJ/mol K2
乙二醇气相氧化反应HOCH2CH2OH(g)+O2(g) OHC-CHO(g) + 2H2O(g)的相同温度下,该反应的化学平衡常数K=___ (用含K1、K2的代数式表示)。
OHC-CHO(g) + 2H2O(g)的相同温度下,该反应的化学平衡常数K=___ (用含K1、K2的代数式表示)。
②当原料气中氧醇比为1.35时,乙二醛和副产物CO2的产率与反应温度的关系如图所示。反应温度在450~ 495℃之间和超过495℃时,乙二醛产率降低的主要原因分别是____、____。

II.乙二醛的用途之一是可以电解氧化制备乙醛酸(OHC-COOH),其生产装置如图所示,通电后,阳极产生的Cl2与乙二醛溶液反应生成乙醛酸。
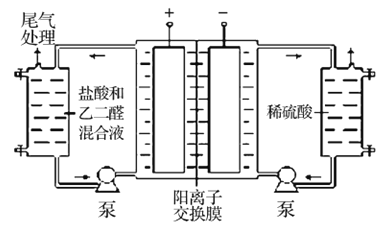
(3)阴极反应式为_________。
(4)阳极液中盐酸的作用,除了产生氯气外,还有__________作用。
(5)保持电流强度为aA,电解tmin,制得乙醛酸mg,列式表示该装置在本次电解中的电流效率η=__________ (已知:法拉第常数为f C·mol-l; )
)
2OHC-COOH(g)△H
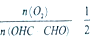 投料比进行上述反应,乙二醛的平衡转化率(a)和催化剂催化效率随温度变化如图1所示。
投料比进行上述反应,乙二醛的平衡转化率(a)和催化剂催化效率随温度变化如图1所示。

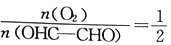 的投料比进行上述反应,乙二醛的平衡转化率(α)和催化剂的催化效率随温度的变化如图所示。下列叙述正确的是
的投料比进行上述反应,乙二醛的平衡转化率(α)和催化剂的催化效率随温度的变化如图所示。下列叙述正确的是






 )
)

 )
)



 )
)