-
下图为铜丝与浓硫酸反应并验证其产物性质的实验装置。

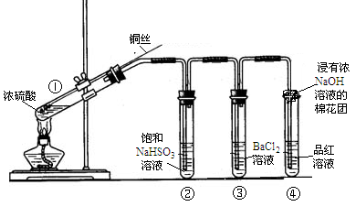
(1)①中反应的化学方程式是 。其中铜发生了 (填“氧化”或“还原”)反应,判断依据为 。
(2)②中饱和NaHSO3溶液的作用是除去①中挥发出的硫酸。加热一段时间后,③中溶液依然澄清,④中溶液褪色。想要立即终止铜与硫酸的反应,最恰当的方法是 。
a.上移铜丝,使其脱离硫酸
b.撤去酒精灯
c.拔去橡胶塞倒出硫酸
(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
| 加入试剂 | 现象 | 反应的离子方程式 |
| 第一份 | 加入NaOH溶液 | 有白色沉淀生成 | ____________ |
| 第二份 | 加入氯水 | 有白色沉淀生成 | ____________ |
完成上述反应的离子方程式。
(4)④中棉花团的作用是 。
(5)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色。取少量蓝色溶液于试管中,滴加NaOH溶液至过量,出现的现象是 。
-
下图为铜丝与浓硫酸反应并验证其产物性质的实验装置。
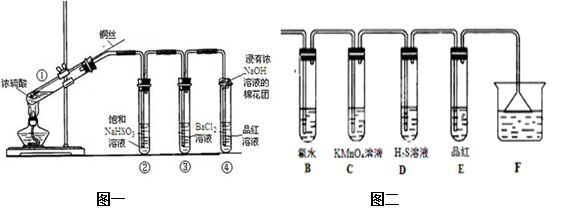
(1)①中反应的化学方程式是 。其中铜发生了 (填“氧化”或“还原”)反应,判断依据为 _______________ 。
(2)浓硫酸在此反应中体现了_________性和____________性。
(3)②中饱和NaHSO3溶液的作用是除去①中挥发出的硫酸。加热一段时间后,③中溶液依然澄清,④中溶液褪色。想要立即终止铜与硫酸的反应,最恰当的方法是 _____________。
a.上移铜丝,使其脱离硫酸 b.撤去酒精灯 c.拔去橡胶塞倒出硫酸
(4)反应停止后,待装置冷却,向③中溶液加入NaOH溶液,观察到的现象是__________。
(5)④中棉花团的作用是 ____ 。
(6)若将浓硫酸与铜反应后产生的气体通入图二的装置中则反应后,装置B中发生的现象是 ,反应的化学方程式为 ______________________;装置C中的现象是 ,表现了SO2的 性;装置D中现象是 ,表现了SO2的 性。
-
下图为铜丝与浓硫酸反应并验证其产物性质的实验装置。
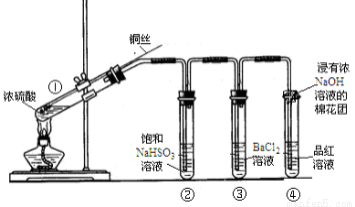
(1)①中反应的化学方程式是_________________________。
(2)②中饱和NaHSO3溶液的作用是除去__________。加热一段时间后,③中溶液依然澄清,想要立即终止铜与硫酸的反应,最恰当的方法是___________。
a.上移铜丝,使其脱离硫酸 b.撤去酒精灯 c.拔去橡胶塞倒出硫酸
(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
| 加入试剂 | 现象 | 反应的离子方程式 |
| 第一份 | 加入NaOH溶液 | 有白色沉淀生成 | _______________ |
| 第二份 | 加入氯水 | 有白色沉淀生成 | _______________ |
完成上述反应的离子方程式。
(4)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色。取少量蓝色溶液于试管中,滴加NaOH溶液过量,出现的现象是_________________。
-
某同学欲验证碳与浓硫酸反应产物的性质。现已将装置如图连接,请回答下列问题。
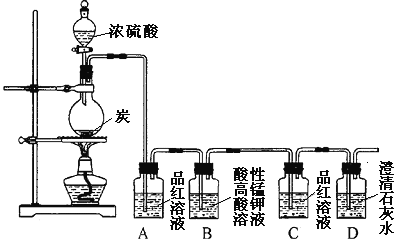
(1)烧瓶中发生反应的化学反应方程式是___________。
(2)实验中两次使用到品红溶液,其目的不同。A的使用目的是_____,通过洗气瓶C中无现象和___的现象,证明反应有_______(填化学式)生成。
(3)洗气瓶B中溶液颜色变浅,说明碳与浓硫酸反应的产物之一______(填名称)具有______的性质。
(4)实验完成后,取出洗气瓶A中的无色溶液于试管中,加热,可观察到__________。
-
(10分)已知浓硫酸和木炭粉在加热条件下可发生化学反应。
(1)上述反应的化学方程式为________。
(2)试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
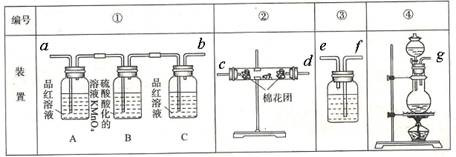
实验时可观察到装置①中A瓶中的溶液退色,C瓶中的溶液不退色。A瓶中的溶液的作用是
;B瓶中的溶液的作用是________;C瓶中的溶液的作用是________。
(3)装置②中所加固体药品是无水硫酸铜。可验证的产物是 ________。
(4)装置③中所盛溶液是澄清石灰水,可验证的产物是 ________。
-
已知浓硫酸和木炭粉在加热条件下可发生化学反应。
(1)上述反应的化学方程式为_____________________
(2)试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
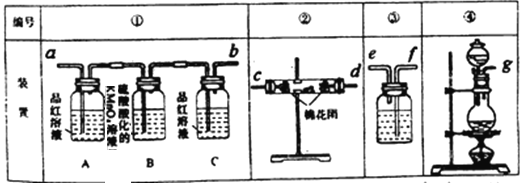
这些装置的连接顺序(按产物气流从左至右的方向)是(填装置中导管口的编号):
_________接__________ ,________接__________,___________ 接_______________。
-
某同学设计如下实验装置探究硫酸与金属、非金属的反应、验证其产物,并探究随着反应的进行,硫酸性质发生的变化。根据实验要求回答相关问题:
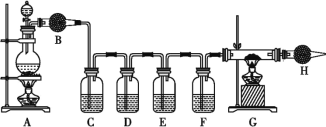
F装置用于检验二氧化碳。供选择的试剂有:只含碳的生铁、18 mol·L-1的硫酸、品红溶液、无水硫酸铜粉未、酸性高锰酸钾溶液、氧化铜、澄清的石灰水、碱石灰。(供选择的试剂可重复使用)
(1)打开分液漏斗的活塞,A装置中发生的反应6H2SO4(浓)+2Fe Fe2(SO4)3+6H2O↑+3SO2↑和(用化学方程式表示)_____,随反应的进行,硫酸的浓度变稀,又发生反应(用化学方程式表示)____
Fe2(SO4)3+6H2O↑+3SO2↑和(用化学方程式表示)_____,随反应的进行,硫酸的浓度变稀,又发生反应(用化学方程式表示)____
(2)B装置中的试剂是__________。
(3)E装置中的试剂是____________作用是______________。
(4)G装置中的试剂是__________,现象是______________。
(5)制备SO2的适宜药品为___________(填代号)。
①Na2SO3固体;②Na2SO3溶液;③20%硫酸;④70%硫酸;⑤铜片
(6)对SO2与氯水的反应进行探究。用注射器吸入一定量的饱和氯水和SO2,振荡,静置,再吸入少量品红溶液,发现品红溶液不褪色,用化学反应方程式解释其原因____________
-
(共14分)某同学设计如下实验装置探究硫酸与金属、非金属的反应、验证其产物,并探究随着反应的进行,硫酸性质发生的变化。根据实验要求回答相关问题:
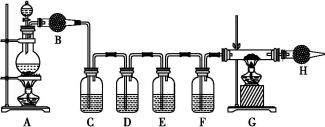
F装置用于检验二氧化碳。供选择的试剂有:只含碳的生铁、18 mol·L-1的硫酸、品红溶液、无水硫酸铜粉未、酸性高锰酸钾溶液、氧化铜、澄清的石灰水、碱石灰。(供选择的试剂可重复使用)
(1)打开分液漏斗的活塞,A装置中发生的反应6H2SO4(浓)+2Fe Fe2(SO4)3+6H2O↑+3SO2↑和 (用化学方程式表示),随反应的进行,硫酸的浓度变稀,又发生反应 (用化学方程式表示)。
Fe2(SO4)3+6H2O↑+3SO2↑和 (用化学方程式表示),随反应的进行,硫酸的浓度变稀,又发生反应 (用化学方程式表示)。
(2)B装置中的试剂是 。
(3)E装置中的作用是 。
(4)G装置中的试剂是 ,现象是 。
(5)从安全角度考虑,应后点燃 的酒精灯(填“A”或“G”)。你认为本实验尾气是否需要处理? (填“是”或“否”),如需处理,具体方案是 。
-
用如图所示实验装置探究铜丝与过量浓硫酸的反应。
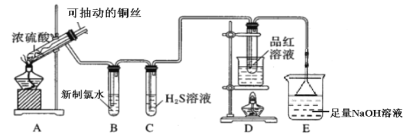
(1)写出A中发生反应的化学方程式__________。在此反应中,浓硫酸表现出来的性质有__________。(填字母序号)
A.强氧化性 B.酸性 C.吸水性 D.脱水性
(2)一段时间后,观察到B中溶液黄绿色褪去,B中反应的化学方程式为__________。C中的实验现象为__________。
(3)D中的实验现象是__________,一段时间后,点燃D处酒精灯,可以观察到__________。
(4)E装置中NaOH溶液的作用是__________。
(5)研究小组认为可以用H2O2溶液来验证E中溶液含有SO32-,进行了实验i。
| 实验序号 | 操作 | 现象 |
| i | a. 取少量E中溶液,向其中加入适量H2O2溶液,振荡,观察。 | 无明显现象 |
| b. 然后滴加__________,振荡,观察。 | 无明显现象 |
| c. 再滴加__________,振荡,观察。 | 白色沉淀 |
通过实验i可证明E中溶液含有SO32-,写出操作b、c中滴加的试剂是__________、__________。
(6)研究小组反思实验方案i不够严谨,设计了对比实验,证明了E中含有SO32-。该对比实验方案是__________。
-
某化学兴趣小组设计如下实验探究Fe与硫酸的反应并验证其产物的性质
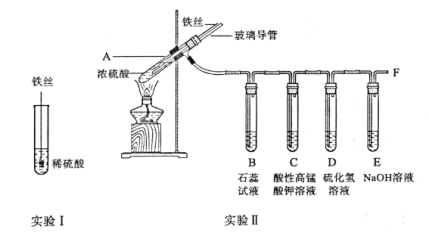
已知:浓H2SO4的沸点为338.2℃。
回答下列问题:
(1)实验Ⅰ的试管中发生反应的离子方程式为________。
(2)加热实验Ⅱ中的试管A使温度保持在250℃~300℃,要观察到A中产生大量气体,此时B中的现象为________;通过C中出现的现象证明该气体具有________性;D中发生反应的化学方程式为________;装置E的作用________(用离子方程式解释);
(3)实验Ⅱ结束后,冷却试管A中的溶液至室温,检验其中既有Fe3+又有Fe2+,F处始终未检测到可燃性气体。
①产生Fe2+的离子方程式为________
②若要检验Fe2+,下列试剂可行的是________(填序号)。
a. KSCN溶液 b. 酸性KMnO4溶液 c. KSCN溶液、氯水









