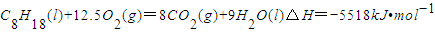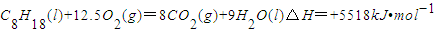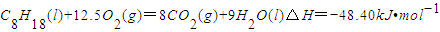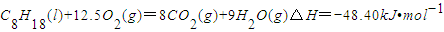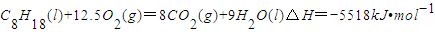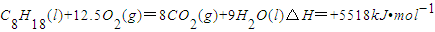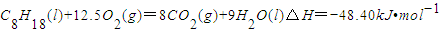-
已知在25 ℃、101 kPa下,0.5 mol辛烷C8H8燃烧生成二氧化碳和液态水时放出2 759 kJ热量。表示上述反应的热化学方程式正确的是( )
A. C8H18(l)+ O2(g)===8CO2(g)+9H2O(g) ΔH=-48.40 kJ·mol-1
O2(g)===8CO2(g)+9H2O(g) ΔH=-48.40 kJ·mol-1
B. C8H18(l)+ O2(g)===8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
O2(g)===8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
C. C8H18(l)+ O2(g)===8CO2(g)+9H2O(l) ΔH=+5 518 kJ·mol-1
O2(g)===8CO2(g)+9H2O(l) ΔH=+5 518 kJ·mol-1
D. 2C8H18(l)+25O2(g)===16CO2(g)+18H2O(l) ΔH=+11 036 kJ·mol-1
-
已知在25℃、101kPa下,0.5mol辛烷C8H18燃烧生成二氧化碳和液态水时放出2759kJ热量。表示上述反应的热化学方程式正确的是( )
A.C8H18(l)+ O2(g)=8CO2(g)+9H2O(g) ΔH= -48.40 kJ·mol-1
O2(g)=8CO2(g)+9H2O(g) ΔH= -48.40 kJ·mol-1
B.C8H18(l)+ O2(g)=8CO2(g)+9H2O(l) ΔH= -5518 kJ·mol-1
O2(g)=8CO2(g)+9H2O(l) ΔH= -5518 kJ·mol-1
C.C8H18(l)+ O2(g)=8CO2(g)+9H2O(l) ΔH= +5518 kJ·mol-1
O2(g)=8CO2(g)+9H2O(l) ΔH= +5518 kJ·mol-1
D.2C8H18(l)+25O2(g)=16CO2(g)+18H2O(l) ΔH= +11036 kJ·mol-1
-
已知在25℃,101kPa下,1gC8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )
A.
B.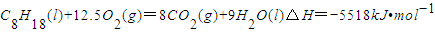
C.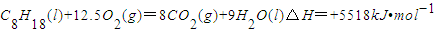
D.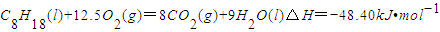
-
已知在25℃,101kPa下,1gC8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )
A.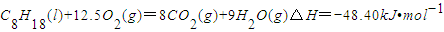
B.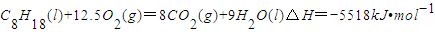
C.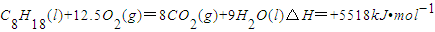
D.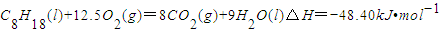
-
已知在25℃、101kPa下,1gC8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ 热量。表示上述反应的热化学方程式正确的是
A、C8H18(l)+25/2O2(g)=8CO2(g) +9H2O(g)△H= - 48.40kJ·mol -1
B、C8H18(l)+25/2O2(g)=8CO2 (g) +9H2O(l)△H= - 5518kJ·mol -1
C、C8H18(l)+25/2O2(g)=8CO2(g) + 9H2O(l) △H= + 5518kJ·mol -1
D、C8H18(l)+25/2O2(g)=8CO2 (g)+ 9H2O(l)△H= - 48.40kJ·mol -1
-
已知在25℃,101kPa下,lgC8H18(辛烷,相对分子质量为114)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的热化学方程式正确的是( )
A.C8H18(1)+ 25/2O2(g)=8CO2(g)+9H2O(1) △H=-5517.6kJ·mol-1
B.C8H18(1)+ 25/2O2(g)=8CO2(g)+9H2O(1) △H=+5517.6kJ·mol-1
C.C8H18(1)+ 25/2O2(g)=8CO2(g)+9H2O(g) △H=-48.40kJ·mol-1
D.C8H18(1)+ 25/2O2(g)=8CO2(g)+9H2O(1) △H=-48.40kJ·mol-1
-
已知在25℃,101kPa下,1gC8H28(辛烷)燃烧生成二氧化碳和液态水时放出48.4kJ热量.表示上述反应的热化学方程式正确的是
A. C8H28(l)+  O2(g)===8CO2(g)+9H2O(l) △H=-5517.6 KJ·mol—1
O2(g)===8CO2(g)+9H2O(l) △H=-5517.6 KJ·mol—1
B. C8H28(l)+  O2(g)===8CO2(g)+9H2O(l) △H=-48.4 KJ·mol—1
O2(g)===8CO2(g)+9H2O(l) △H=-48.4 KJ·mol—1
C. C8H28(l)+  O2(g)===8CO2(g)+9H2O(l) △H=+5517.6 KJ·mol—1
O2(g)===8CO2(g)+9H2O(l) △H=+5517.6 KJ·mol—1
D. C8H28(l)+  O2(g)===8CO2(g)+9H2O(l) △H=+48.4 KJ·mol—1
O2(g)===8CO2(g)+9H2O(l) △H=+48.4 KJ·mol—1
-
已知在25℃,101kPa下,1g液态C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40kJ热量。表示上述反应的热化学方程式正确的是
A. C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(g)ΔH=-48.40kJ·mol-1
B. C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1)ΔH=-5518kJ·mol-1
C. C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(1)ΔH=-5518kJ
D. C8H18(1)+22.5O2(g)=8CO2(g)+9H2O(g)ΔH=-5518kJ·mol-1
-
已知在25 ℃、101 kPa下,1 g C8H18(辛烷)燃烧生成二氧化碳和液态水放出48.40 kJ热量,表示上述反应的热化学方程式正确的是( )
A.C8H18(l)+O2(g)=8CO2(g)+9H2O(l)ΔH=-48.40kJ·mol-1
B.C8H18(l)+O2(g)=8CO2(g)+9H2O(l)ΔH=-5518 kJ·mol-1
kJ·mol-1
C.C8H18(l)+O2(g)=8CO2(g)+9H2O(l)ΔH=+5518kJ·mol-1
D.C8H18(l)+O2(g)=8CO2(g)+9H2O(l)ΔH=+48.40kJ·mol-1
-
已知在25 ℃,101 kPa下,1 g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.4 kJ热量。表示上述反应的热化学方程式正确的是( )
A.C8H18(l)+ O2(g)===8CO2(g)+9H2O(g) ΔH=-48.4 kJ·mol-1
O2(g)===8CO2(g)+9H2O(g) ΔH=-48.4 kJ·mol-1
B.C8H18(l)+ O2(g)===8CO2(g)+9H2O(l) ΔH=-5517.6 kJ·mol-1
O2(g)===8CO2(g)+9H2O(l) ΔH=-5517.6 kJ·mol-1
C.C8H18(l)+ O2(g)===8CO2(g)+9H2O(l) ΔH=+5517.6 kJ·mol-1
O2(g)===8CO2(g)+9H2O(l) ΔH=+5517.6 kJ·mol-1
D.C8H18(l)+ O2(g)===8CO2(g)+9H2O(l) ΔH=-48.4 kJ·m
O2(g)===8CO2(g)+9H2O(l) ΔH=-48.4 kJ·m ol-1
ol-1
O2(g)===8CO2(g)+9H2O(g) ΔH=-48.40 kJ·mol-1
O2(g)===8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
O2(g)===8CO2(g)+9H2O(l) ΔH=+5 518 kJ·mol-1