-
过氧化钙(CaO2)是一种白色、无毒、难溶于水的固体,能杀菌消毒,广泛用于果蔬保鲜、空气净化、污水处理等方面。工业生产过程如下:
①在NH4Cl溶液中加入Ca(OH)2;
②在第①步的生成的产物中加入30% H2O2,反应生成CaO2•8H2O沉淀;
③经过陈化、过滤,水洗得到CaO2•8H2O,再脱水干燥得到CaO2。
完成下列填空:
(1)第①步反应的化学方程式为 ________。
(2)生产中可循环使用的物质是 。
(3)检验CaO2•8H2O是否洗净的方法是 ________________ 。
(4)已知CaO2在350℃迅速分解生成CaO和O2。如图是实验室测定产品中CaO2含量的装置(夹持装置省略)。
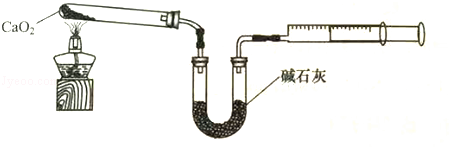
若所取产品质量是m g,测得气体体积为V mL(已换算成标准状况),则产品中CaO2的质量分数为 (用字母表示)。过氧化钙的含量也可用重量法测定,需要测定的物理量有 ______ 。
-
过氧化钙(CaO2)是一种难溶于水、溶于酸的白色固体,广泛用于果蔬保鲜、空气净化、污水处理等方面。以下是一种制备过氧化钙的实验方法。
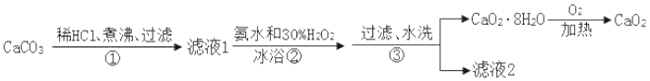
回答下列问题:
(1)下图是某学生的过滤操作示意图,其操作不规范的是____。
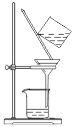
a.漏斗末端颈尖未紧靠烧杯壁
b.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
c.将滤纸湿润,使其紧贴漏斗壁
d.玻璃棒用作引流
(2)步骤②需要在冰浴下进行,原因是_______。
(3)步骤③检验 CaO2· 8H2O是否洗净的方法是:取最后一次洗涤液少许于试管中,_______。
(4)制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后可得到过氧化钙产品。该工艺方法的缺点是_______。
(5)写出②发生的化学方程式_______。
(6)已知CaO2在350℃迅速分解生成CaO和O2。下图是实验室测定产品中CaO2 含量的装置(夹持装置省略)。
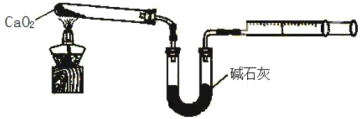
若所取产品质量是 m g,测得气体体积为 V mL(已换算成标准状况),则产品中CaO2的质量分数为_______(用字母表示)。
-
过氧化钙是重要的无机过氧化物。近年来,这种产品的用途,伴随着应用技术的开发在迅速增多,现已广泛用于化学工业和农业等方面的生产。工业上生产过氧化钙的主要流程如下:



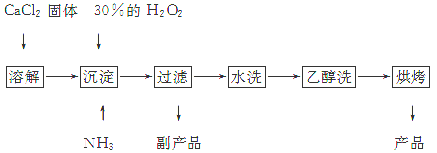
已知CaO2·8H2O呈白色,微溶于水,加热至350 ℃左右开始分解放出氧气。
(1)用上述方法制取CaO2·8H2O的化学方程式是_________________________________;
(2)检验“水洗”是否合格的方法是__________________________________________;
(3)沉淀时常用冰水控制温度在0 ℃左右,其可能原因是(写出两种):
①_______________________________________________________________________;②_______________________________________________________________________。
-
过氧化钙晶体﹝CaO2·8H2O﹞较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒, 也在食品、牙膏、化妆品等制造中用作添加剂,还可以作为鱼池增氧剂。现以贝壳为原料制备CaO2流程如下:
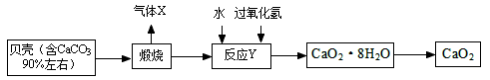
(1)将过氧化钙晶体与溶液分离的方法是_____。
(2)我国制碱工业的先驱侯德榜先生为纯碱和氮肥工业技术的发展做出了杰出的贡献。其制备 原料有气体 X、氨气、精制饱和食盐水,过程主要是先制得小苏打,再过滤并加热分解小苏打制得纯碱。
①实验过程中应该先向精制饱和食盐水中通入_____,其原因是_____。
②请写出制备纯碱第一步发生的化学方程式_____。
(3)反应Y 不能在较高温度下进行的原因是_____; 已知该反应是化合反应,则反应 Y 的化学方程式是___________________;获得的过氧化钙晶体中常含有 Ca(OH)2 杂质,原因是_________。
(4)现设计如下实验测定制得的过氧化钙晶体[CaO2·8H2O]中 CaO2 的质量分数:称取晶体样品25 g,加热到 220℃充分分解,其产物含有参与反应 Y 的固体物质和能使带火星木条复燃的气体等(此时所得气体混合物的总质量为1.6 g)(已知杂质不发生变化),则该晶体样品中 CaO2 的质量分数是_____。
-
过氧化钙晶体﹝CaO2·8H2O﹞较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒。以贝壳为原料制备CaO2流程如下:
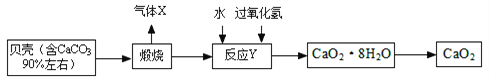
(1)气体X的名称是__________,实验室常用_____________溶液来吸收;将过氧化钙晶体与溶液分离的方法是________________。
(2)反应Y需控制温度在0~2℃,可将反应容器放在_________________中,该反应是化合反应,反应产物是CaO2·8H2O,请写出该反应的化学方程式_____________________________________。
(3)获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是___________________________。
-
ClO2与Cl2的氧化性相近。在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。(已知:装置C的作用是吸收Cl2)
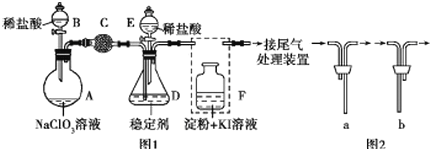
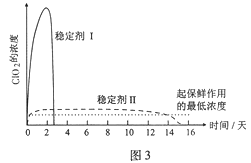
(1)仪器B的名称是________。安装F中导管时,应选用图2中的_________________。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O.为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜_______________(填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,NaClO2中Cl的化合价为______。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为__________。
(5)工业上可用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应离子方程式为___________________。(已知:在酸性条件下SO32-被ClO3-氧化为SO42-)
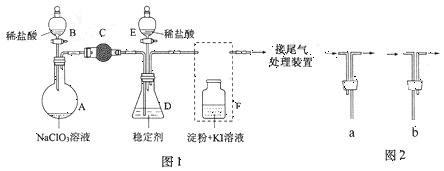
(6)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示,若将其用于水果保鲜,你认为效果较好的稳定剂是__________,原因是________________。
-
氯及其化合物在自来水消毒和果蔬保鲜等方面应用广泛.
(1)写出实验室制取氯气的离子方程式 .
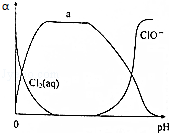
(2)新制饱和氯水中部分含氯成分所占分数(a)随pH变化的关系如图所示.
①则曲线a所代表的是 (填化学式,下同),未在图中绘出的是 ,杀菌效果与pH的关系是 .
②已知:次氯酸或氯水可被FeCl2、H2O2、Na2SO3等物质还原成Cl﹣.一种测定氯水中氯元素总量的实验步骤如下:
步骤1:取一定量的试样,加入足量的 溶液,充分反应.
步骤2:加热.
步骤3:再冷却,加入足量的 溶液.
步骤4:过滤、洗涤、干燥、称量沉淀质量.
步骤5:将实验步骤1~4重复2次.
(3)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为 ,ClO2比Cl2的杀菌效果更好,则等物质的量的ClO2杀菌效果是Cl2的 倍.
-
ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。
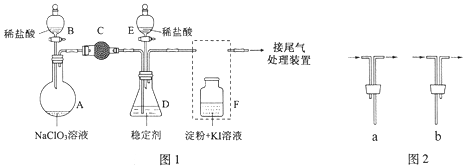
(1)仪器D的名称是____。安装F中导管时,应选用图2中的_____。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜____(填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是_____。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为____,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是______。
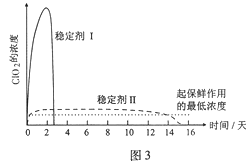
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示。若将其用于水果保鲜,你认为效果较好的稳定剂是_______,原因是_________。
-
ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。
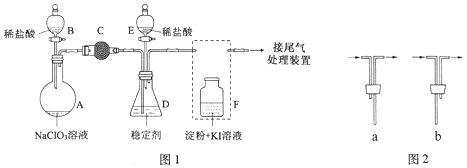
(1)仪器D的名称是____。安装F中导管时,应选用图2中的_____。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜____(填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是_____。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为____,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是______。
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示。若将其用于水果保鲜,你认为效果较好的稳定剂是_______,原因是_________。
-
Ⅰ、ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。
某兴趣小组通过上图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。
(1)仪器B、D的名称是_________________、___________________。
(2)打开B的活塞,A中制得ClO2和Cl2,写出该反应的化学方程式:___________。
(3)为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜_______(填“快”或“慢”)。
(4)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是______________________________。
(5)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为______________________________________。在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是_______________。在虚线框中F装置上面的导管应选图2中的______。
Ⅱ、如图为苯和溴的取代反应的实验装置图,其中A为由具有支管的试管制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑粉.

(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应.写出A中所发生有机反应的化学方程式(有机物写结构简式):__________。
(2)试管C中苯的作用是____________________.反应开始后,观察D和E两试管,看到的现象为__________、____________________.
(3)反应2~3min后,在B中的NaOH溶液里可观察到的现象是_____________.
(4)在上述整套装置中,具有防倒吸作用的仪器有____________(填字母).















