-
磷的含氧酸有磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸(H3PO2)等多种,它们在工业上都是重要的化工原料。
(1)亚磷酸(H3PO3)是一种二元弱酸,写出H3PO3与过量NaOH溶液反应的化学方程式:_______。某温度下,0.01 mol • L-1 H3PO3溶液的pH为2.7,该温度下,H3PO3 的一级电离常数 Kal=_______。 (已知:lg2 = 0.3,lg3 = 0.5,lg5 = 0.7,H3PO3 的第二步电离忽略不计)
(2)某实验小组用NaOH溶液处理含H3PO3废水,当溶液中c (Na+) =c(H2PO3-) + 2c(HPO32-)时,溶液呈______性(填“酸”“碱”或“中”)。
(3)已知:常温下,磷酸(H3PO4)的 Kal=7.ll×10-3、Ka2 = 6.23×10-8、Ka3 = 4.5 ×10-13, 则常温下,Na2HPO4溶液中H2PO4-、HPO42-和PO43-的浓度由大到小的顺序为________。
(4)向某浓度的磷酸溶液中滴加NaOH溶液,其pH与溶液中H3PO4、H2PO4-、HPO42-和PO43-的物质的量分数为δ (平衡时某物种的浓度与整个物种浓度之和的比值)的关系如图所示。以酚酞为指示剂,当溶液由无色变为浅红色时,发生主要反应的离子方程式是_________。
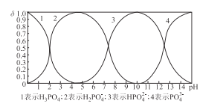
(5)已知:常温下,Ksp(FePO4) = l.3×10-22、Ksp(A1PO4) = 5.2 ×10-19。常温下,向含Fe3+、A13+的混合溶液中滴加Na3PO4溶液,当FePO4、AlPO4同时生成时,溶液中c(Fe3+):c(Al3+ ) =_________。
-
化学反应原理对于研究化学物质有十分重要的意义。
(1)已知次磷酸(H3PO2,一元中强酸)和亚磷酸(H3PO3,结构式为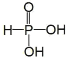 ,二元中强酸)均是重要的精细化工产品。
,二元中强酸)均是重要的精细化工产品。
①写出次磷酸的结构式:_____________________________________。
②已知某温度下0.01 mol·L-1的NaOH溶液pH=10,将该NaOH溶液与等浓度等体积的次磷酸溶液混合,混合后溶液pH=7,则此时c(OH-)—c(H3PO2)=___________。(用具体数值表示)
(2)实验室配制FeCl3溶液时,需要将FeCl3固体溶解在较浓的盐酸中,其原因是_______________________________________________________(用离子方程式和必要的文字说明)。
已知25℃时,Fe(OH)3的Ksp=4.0×10-38,配制100ml 5 mol·L-1的FeCl3溶液,至少需要加入_______mL 2 mol·L-1的盐酸(忽略加入盐酸的体积)。
(3)工业废水中的Cr2O72-对生态系统有很大损害。常用的处理方法有两种。
①还原沉淀法:Cr2O72- Cr3+
Cr3+ Cr(OH)3。常温下,要使Cr3+沉淀完全,溶液的pH应调至________。(已知Cr(OH)3的Ksp=10-32)
Cr(OH)3。常温下,要使Cr3+沉淀完全,溶液的pH应调至________。(已知Cr(OH)3的Ksp=10-32)
②电解法:用铁和石墨做电极,电解产生的还原剂将Cr2O72-还原成Cr3+,最终产生Cr(OH)3沉淀。若有1mol Cr2O72-被还原,理论上导线中通过___________mol电子。
-
磷能形成多种含氧酸。
(1)一元中强酸次磷酸(H3PO2)是一种精细化工产品,向10 mL H3PO2溶液中加入10 mL等物质的量浓度的NaOH溶液后,所得的溶液中只有H2PO2-、OH-两种阴离子。
① 写出H3PO2溶液与足量NaOH 溶液反应后形成的正盐的化学式:_______,该正盐溶液中各离子浓度由大到小的顺序为____________。
② 若25℃时,K (H3PO2) = 1×10-2,则0.01 mol · L-1的H3PO2溶液的pH =________。
(2)亚磷酸(H3PO3)是二元中强酸,25℃时亚磷酸的电离常数为K1= 3.7×10-2、K2=2.6×10-7。
试从电离平衡移动的角度解释K1、K2数据的差异______________。
(3) 25 ℃时,HF的电离常数为K = 3.6×10-4; H3PO4的电离常数为K1=7.5×10-3,K2=6.2×10-8,K3=4.4×10-13。足量NaF溶液和H3PO4溶液反应的离子方程式为______。
(4)相同温度下,等物质的量浓度的上述三种磷的含氧酸中。c(H+)由大到小的顺序为______________________________________________________(用酸的分子式表示)。
-
(6分)判断含氧酸强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强。如下表所示
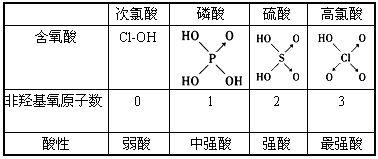
(1)亚磷酸(H3PO3)和亚砷酸(H3AsO3)分子式相似,但它们的酸性差别很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性。由此可推出它们的结构式分别为 、
、 。
。
简述二者酸性强弱原因_____________________。
(2)亚磷酸和亚砷酸与过量的氢氧化钠溶液反应的化学方程式分别为:
①___________________; ②_______________________。
-
磷是重要的元素,能形成多种含氧酸。回答下列问题:
(1)次磷酸(H3PO2)是一元酸,其电离常数的值K=9×103。向10mL0.1 mol•L-1H3PO2溶液中加入30mL等物质的量浓度的NaOH溶液,写出反应的离子方程式_________,c(Na+)+(H2PO2-)+c(H3PO2)=______(忽略混合后溶波体积的变化)。
(2)亚磷酸(H3PO3)是二元弱酸, 25℃时亚磷酸的电离常数的值为K1=1×10-2、k2=2.6×10-7,则NaH2PO3溶液显性_____(填“酸”“碱”或“中”),原因是____(结合化学用语及数据计算进行解释)
(3)已知HF的电离常数的值为K=3.6×10-4,将足量HF溶液和Na2HPO3溶液反应,其离子方程式为______。
(4)亚磷酸具有强还原性。化学实验小组利用滴定法测定某亚磷酸溶液的浓度,取25.00mL的亚磷酸溶液放入锥形瓶中,用0.10 mol•L-1的高锰酸钾溶液进行滴定,反应的离子方程式是5H3PO3+ 2MnO4-+6H+ = 5H3PO4+ 2Mn2+ +3H2O。
三次滴定实验的数据分别如下:
| 实验编号 | 滴定前读数 | 滴定后读数 |
| 1 | 0.50 | 22.50 |
| 2 | 1.50 | 24.50 |
| 3 | 1.00 | 22.00 |
①亚磷酸溶液的物质的量浓度为______。
②关于该实验下列说法正确的是______(填写序号)。
a 取亚磷酸溶液的滴定管,洗涤后未润洗,导致结果偏低
b 盛高锰酸钾溶液的滴定管滴定前有气泡,滴定后无气泡,导致结果偏高
c 滴定过程中眼睛只注视滴定管中液面变化,并做好记录
d 锥形瓶未干燥底部有水,会导致结果偏低
-
已知吡啶( )与苯环性质相似。有机物M与磷酸在一定条件下形成磷酸吡醛,
)与苯环性质相似。有机物M与磷酸在一定条件下形成磷酸吡醛,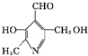 (M)+H3PO4
(M)+H3PO4 H2O+
H2O+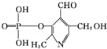 (磷酸吡醛),磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )
(磷酸吡醛),磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )
A.M能使酸性高锰酸钾溶液褪色
B.1 mol M能与金属钠反应,消耗2 mol Na
C.1 mol磷酸吡醛与NaOH溶液反应,最多消耗3 mol NaOH
D.M与足量H2反应后所得有机物的分子式为C8H17O3N
-
铜、磷及其化合物在生产、生活中有重要的用途,回答下列问题:
(1)磷的一种化合物叫亚磷酸(H3PO3)。已知:
Ⅰ、0.1mol/L H3PO3溶液的pH=1.7;
Ⅱ、H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ、H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成.
①关于H3PO3的说法:a强酸;b弱酸;c二元酸;d三元酸;e氧化性酸;f还原性酸,其中正确的是__________
A.bdf B.bcf C.ade D.bce,
②写出H3PO3与少量NaOH溶液反应的离子方程式__________;
③Na2HPO3为__________(填“正盐”或“酸式盐”)
(2)碘化亚铜可作催化剂,饲料添加剂等,是难溶于水的固体.铜可以与氢碘酸发生置换反应得到氢气,试从离子浓度对离子反应方向影响的角度解释此反应能够发生的原因__________,CuSO4溶液也能使淀粉-KI试纸变蓝,用离子方程式说明其原理__________;
(3)纳米氧化亚铜是一种具有良好光电效应的材料,工业上制备它的方法之一是:先向KOH溶液中加入一定量的CuSO4溶液,再加入一定量的肼(N2H4),加热并保持反应体系的温度在90℃,反应完全后,分离、洗涤、真空干燥所得到的固体样品。检验反应混合体系内纳米Cu2O已经生成的实验方法的名称是__________。
-
次磷酸(H3PO2)是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。下列有关说法正确的是
A.用惰性电极电解NaH2PO2溶液,其阳极反应式为:2H2O-4e-=O2↑+4H+
B.H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-=PO23-+3H2O
C.将H3PO2溶液加入到酸性重铬酸钾溶液中,H3PO2的还原产物可能为H3PO4
D.H3PO2溶于水的电离方程式为H3PO2 H++H2PO2-
H++H2PO2-
-
在工业上次磷酸(H3PO2)常用于化学镀银,发生的反应如下:____Ag++___ H3PO2+___H2O→____Ag↓+____ H3PO4+___H+
请回答下列问题:
(1)H3PO2中,P元素的化合价为_____;该反应中,H3PO2作_____(填“氧化剂”或“还原剂”)。
(2)上述离子方程式中,各物质的化学计量数分别为___________。
(3)若反应中生成10.8g Ag,则转移的电子数为__________。
(4)H3PO2是一元中强酸,写出其与足量NaOH 溶液反应的离子方程式:________。
-
次磷酸(H3PO2)是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。下列有关说法正确的是
A.H3PO2溶于水的电离方程式为:H3PO2 3H++PO23-
3H++PO23-
B.H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-=PO23-+3H2O
C.将H3PO2溶液加入到酸性高锰酸钾溶液中,H3PO2的氧化产物为H3PO4
D.用惰性电极电解NaH2PO2溶液,其阳极反应式为:H2PO2-4e-+2H2O =O2↑+4H+

 ,二元中强酸)均是重要的精细化工产品。
,二元中强酸)均是重要的精细化工产品。
 (M)+H3PO4
(M)+H3PO4 (磷酸吡醛),磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )
(磷酸吡醛),磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )