-
下列反应中铁元素被氧化的是
A.Fe2O3 +6HCl→2FeCl3 +3H2O B.3Fe +4H2O→Fe3O4 + 4H2↑
C.2FeCl3+2KI→2FeCl2 +I2 +2KCl D.3NaOH +FeCl3→Fe(OH)3↓+3NaCl
高二化学单选题简单题查看答案及解析
-
已知反应①2FeCl3+2KI=2FeCl2+2KCl+I2 ②KClO3+6HCl=KCl+3Cl2↑+3H2O
③2FeCl2+Cl2=2FeCl3 ,下列物质的氧化能力强弱顺序正确的是( )
A. FeCl3>Cl2>I2> KClO3 B. KClO3>Cl2> FeCl3>I2
C. Cl2>KClO3> FeCl3>I2 D. KClO3>Cl2>I2> FeCl3
高二化学选择题中等难度题查看答案及解析
-
(每空2分,共10分)铁元素是重要的金属元素,单质铁在工业和生活中使用得最为广泛。铁还有很多重要的化合物及其化学反应。
如铁与水反应:3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g) △H
(1)上述反应的平衡常数表达式K=_____________。
(2)已知:①3Fe(s)+2O2(g)=Fe3O4(s) △H1=-1118.4kJ·mol-1
②2H2(g)+O2(g)=2H2O(g) △H2=-483.8 kJ·mol-1
③2H2(g)+O2(g)=2H2O(l) △H3=-571.8 kJ·mol-1
则△H=_____________。
(3)在t℃时,该反应的平衡常数K=16,在2L恒温恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
Fe
H2O(g)
Fe3O4
H2
甲/mol
1.0
1.0
1.0
1.0
乙/mol
1.0
1.5
1.0
1.0
①甲容器中H2O的平衡转化率为_____________(结果保留一位小数)。
②下列说法正确的是_____________(填编号)
A.若容器压强恒定,则反应达到平衡状态
B.若容器内气体密度恒定,则反应达到平衡状态
C.甲容器中H2O的平衡转化率大于乙容器中H2O的平衡转化率
D.增加Fe3O4就能提高H2O的转化率
(4)若将(3)中装置改为恒容绝热(不与外界交换能量)装置,按下表充入起始物质,起始时与平衡后的各物质的量见表:
Fe
H2O(g)
Fe3O4
H2
起始/mol
3.0
4.0
0
0
平衡/mol
m
n
p
q
若在达平衡后的装置中继续加入A、B、C三种状况下的各物质,见表:
Fe
H2O(g)
Fe3O4
H2
A/mol
3.0
4.0
0
0
B/mol
0
0
1
4
C/mol
m
n
p
q
当上述可逆反应再一次达到平衡状态后,上述各装置中H2的百分含量按由大到小的顺序排列的关系是___________(用A、B、C表示)。
高二化学填空题极难题查看答案及解析
-
下列氧化还原反应中,实际参加反应的氧化剂与还原剂的物质的量之比正确
①KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O;1∶6
②Fe2O3+2Al
Al2O3+2Fe;1∶2
③SiO2+3C
SiC(硅为+4价)+2CO↑;1∶2
④3NO2+H2O===2HNO3+NO;2∶1
A. ①③ B. ②③ C. ②④ D. ①④
高二化学单选题简单题查看答案及解析
-
下列属于氧化还原反应的是( )
A.2HNO3+Ba(OH)2═Ba(NO3)2+2H2O
B.Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
C.KClO3+6HCl═3Cl2↑+KCl+3H2O
D.K2O+H2O═2KOH
高二化学单选题简单题查看答案及解析
-
下列反应不属于氧化还原反应的是
A.Al (OH)3+3HCl==AlCl3+3H2O B.3Fe+4H2O(g)
Fe3O4+4H2
C.3NO2+H2O==2HNO3+NO D.Cl2+H2O==HCl+HClO
高二化学选择题简单题查看答案及解析
-
下列离子方程式书写正确的是
A.将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O
B.向AlCl3溶液中滴加氨水:Al3++3OH-=Al(OH)3↓
C.Fe2O3与氢碘酸反应:Fe2O3+6H+=2Fe3++3H2O
D.向氯化亚铁溶液中滴加稀硝酸:3Fe2++4H++ NO3-= 3Fe3++NO↑+2H2O
高二化学选择题中等难度题查看答案及解析
-
在一个容积可变的密闭容器中发生反应:3Fe(s)+4H2O(g)
Fe3O4(s)+4H2(g)。
回答下列问题:
(1)增加Fe的量,正反应速率 (填“增大”、“减小”或“不变”,下同)。
(2)将容器的容积缩小一半,正反应速率 ,逆反应速率 。
(3)保持容器的容积不变,充入N2使体系压强增大,正反应速率 ,逆反应速率 。
(4)保持压强不变,充入N2使容器的容积增大,正反应速率 ,逆反应速率 。
高二化学填空题中等难度题查看答案及解析
-
反应3Fe(s)+4H2O(g)
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。下列叙述能表明反应达到平衡状态的是
A.容器内压强不再改变 B.
(H2O)=
(H2)
C.气体的密度不再改变 D.反应不再进行
高二化学选择题中等难度题查看答案及解析
-
对于反应3Fe(s)+4H2O(g)
Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是( )
A.K=
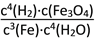
B.K=
C.增大c(H2O)或减小c(H2),会使该反应平衡常数减小
D.改变反应的温度,平衡常数不一定变化
高二化学选择题简单题查看答案及解析