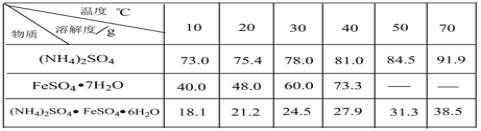-
某兴趣小组用铝箔制备纳米Al2O3、AlCl3·6H2O及铵明矾晶体(NH4Al(SO4)2•12H2O,摩尔质量为453g•mol-1),具体流程如图:
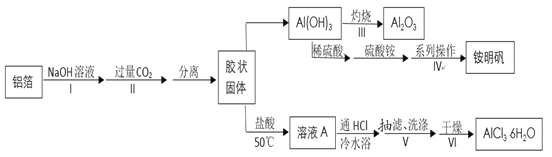
已知:a.AlCl3·6H2O易溶于水、乙醇及乙醚;
b.铵明矾晶体无色、透明,可溶于水、不溶于乙醇。120℃时失去结晶水,280℃以上分解。
请回答:
(1)步骤Ⅰ的离子方程式为______。
(2)下列操作或描述正确的是_____。
A.步骤IV制备铵明矾利用了物质的溶解度差异
B.步骤III灼烧时需将氢氧化铝放在蒸发皿里用高温炉灼烧至恒重
C.步骤II生成的固体可用抽滤法分离,为加快过滤速度,可用玻璃棒轻轻搅拌
D.步骤IV中可以选择乙醇洗涤晶体,如果在常压下快速干燥,温度选择低于120℃
(3)由溶液A制备AlCl3·6H2O的过程中要通入HCl气体,其作用是______(写两条)。
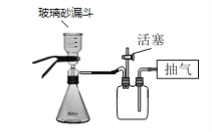
(4)步骤V抽滤时不能用滤纸,原因是_____。若用如图装置图进行抽滤,则抽滤结束时应进行的操作是______。
(5)用电子天平称取2.760g的铵明矾粗产品,用水溶解后取相同体积的两份溶液。第一份用EDTA滴定法测得n(Al3+)为0.002900mol;第二份用BaCl2溶液滴定法测得n(SO42-)为0.006300mol。则该试样中铵明矾的纯度为______。
-
明矾[KAl(SO4)2·12H2O]是一种复盐,在造纸等方面应用广泛。某兴趣小组采用10.0 g废易拉罐(含90%的Al,还含有少量的Fe、Mg等杂质)制备明矾的实验方案如图1:
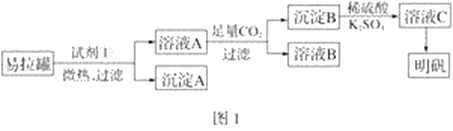
(1)试剂①应选用________(填代号)。
a.盐酸 b.H2SO4溶液
c.氨水 d.NaOH溶液
(2)易拉罐溶解过程中主要反应的化学方程式为___________________________。
(3)溶液B中溶质的主要成分为________________(填化学式)。
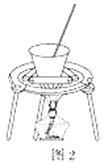
(4)从溶液C中得到明矾的实验操作步骤为蒸发浓缩、________(填操作名称)、过滤、洗涤、干燥。如图2所示,蒸发操作中的一处错误是________________________________。
(5)该小组在实验完成之后,得到118.5 g明矾,则明矾的回收率为________。(已知:明矾的摩尔质量为474 g·mol-1)
-
煅烧铵明矾晶体时发生的主要反应为:4[NH4Al(SO4)2·12H2O]  2Al2O3+N2↑+2NH3↑+3SO2↑+53H2O+5SO3↑,将产生的气体通过如图所示的装置(广口瓶中的试剂均足量)。
2Al2O3+N2↑+2NH3↑+3SO2↑+53H2O+5SO3↑,将产生的气体通过如图所示的装置(广口瓶中的试剂均足量)。
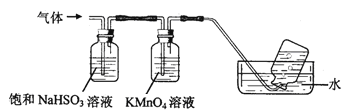
(1)集气瓶中最终收集到的气体是______ (填化学式,下同)。
(2)通过足量饱和NaHSO3溶液后大量减少的气体有______ 。
(3)KMnO4溶液颜色逐渐褪去,发生反应的离子方程式为______ 。
(4)向硫酸铝铵溶液中逐滴加入氢氧化钡溶液,反应后溶液中溶质的成分不可能是______ (填字母)。
A.(NH4)2SO4、Al2(SO4)3 B.(NH4)2SO4
C.(NH4)2SO4、Ba(AlO2)2 D.(NH4)2SO4、Al2(SO4)3、Ba(OH)2
-
铵明矾NH4Al(SO4)2·12H2O是分析化学常用基准试剂,其制备过程如下。下列分析不正确的是
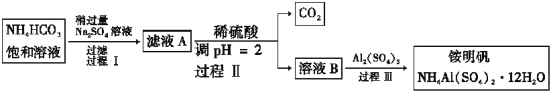
A. 过程Ⅰ反应:2NH4HCO3+Na2SO4===2NaHCO3↓+(NH4)2SO4
B. 检验溶液B中阴离子的试剂仅需BaCl2溶液
C. 若省略过程Ⅱ则铵明矾产率明显减小
D. 向铵明矾溶液中逐滴加入NaOH溶液先后观察到:刺激性气体逸出→白色沉淀生成→白色沉淀消失
-
某兴趣小组用铝箔制备 、
、 及明矾大晶体,具体流程如下:
及明矾大晶体,具体流程如下:
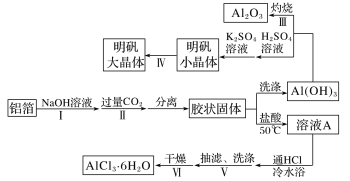
已知:抽滤是一种过滤的方式。
请回答:
(1)步骤Ⅰ中的化学方程式___________;
(2)步骤Ⅱ中生成 的离子方程式_____________;
的离子方程式_____________;
(3)写出 的电离方程式_____________。
的电离方程式_____________。
(4)步骤Ⅲ,下列操作合理的是______。
A. 坩埚洗净后,无需擦干,即可加入 灼烧
灼烧
B. 为了得到纯 ,需灼烧至恒重
,需灼烧至恒重
C. 若用坩埚钳移动灼热的坩埚,需预热坩埚钳
D. 坩埚取下后放在石棉网上冷却待用
E. 为确保称量准确,燃烧后应趁热称重
(5)由溶液A制备 的装置如图。
的装置如图。
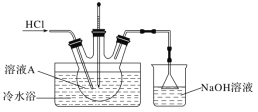
①通入HCl的作用是___________和降低 的溶解度,使其以_______(填化学式)晶体形式析出。
的溶解度,使其以_______(填化学式)晶体形式析出。
②烧杯中NaOH溶液的作用是___________,倒置漏斗的作用是__________________。
-
铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:
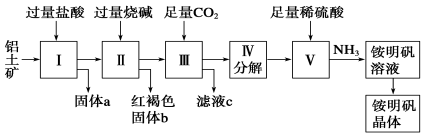
请回答下列问题:
(1)固体a的化学式为________。
(2)由图中Ⅴ制取铵明矾溶液的化学方程式为____ _,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)________、冷却结晶、过滤洗涤。
(3)以1 000 kg含氧化铝36%的铝土矿为原料制取Al2(SO4)3,需消耗质量分数为98%的硫酸(密度1.84 g·cm-3)________ L(保留一位小数)。
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为________。
-
铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制铵明矾晶体[NH4Al(SO4)2]的工艺流程如图所示:
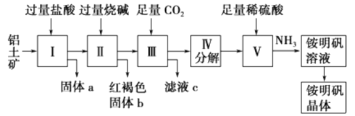
请回答下列问题:
(1)固体a的化学式为________,固体b化学式为________,Ⅲ中通入足量CO2气体发生反应的离子方程式为________________。
(2)由Ⅴ制取铵明矾溶液的化学方程式为__________________。
(3)由Ⅰ→Ⅱ→Ⅲ→Ⅳ都要用到的分离方法是__________________,由铵明矾溶液中制铵明矾晶体的操作是__________________。
(4)如果先向铝土矿加入过量氢氧化钠,再加入过量盐酸,此时首先出现的固体a是__________。
-
实验室利用马矿的矿渣(成分Fe2O3、FeO、Al2O3、SiO2)制备明矾[KAl(SO4)2·12H2O]和绿矾FeSO4·7H2O。流程如下:
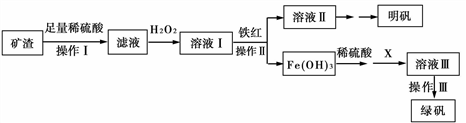
(1)操作I得到的滤渣主要成分是__________。
(2)加入H2O2的离子反应方程式为__________。
(3)若X是一种固体单质,且溶液Ⅲ的溶质只有一种,则X化学式为_________。
(4)向明矾水溶液中加过量的NaOH溶液,其离子方程式为_________。
(5)绿矾放置在空气中,可能被氧气氧化,请设计实验判断绿矾是否被氧化(简述实验过程、现象和结论)____ 。
(6)若实验室取用1kg矿渣(含铁元素5.6%)进行实验,操作Ⅱ中消耗铁红80g,假设每个过程反应都恰好完全进行,且忽略损失,则理论上得到绿矾__________g
-
硫酸亚铁铵晶体[(NH4)2SO4·FeSO4·6H2O]又称摩尔盐,难溶于乙醇,常用于定量分析。某实验小组利用工业废铁屑制取摩尔盐,并测定其纯度,工艺流程图如下。
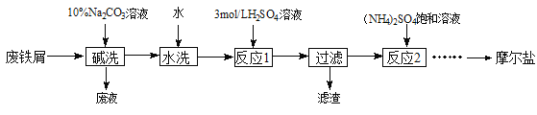
已知:硫酸铵、FeSO4·7H2O、硫酸亚铁铵在水中的溶解度
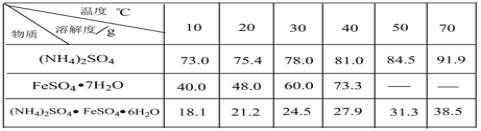
(1)碱洗的目的是_________。
(2)反应1温度需控制在70~75℃,可采取的措施是________。
(3)反应2中常用3 mol·L-1的硫酸调节溶液的pH为1~2,其目的是_______。
(4)请补充完整由反应2所得溶液获得硫酸亚铁铵晶体的实验方案:____、过滤、用乙醇洗涤、低温干燥。
(5)为测定硫酸亚铁铵(NH4)2SO4·FeSO4·6H2O晶体纯度,做了如下实验:
准确称取0.4000g上述硫酸亚铁铵晶体置于锥形瓶中溶解,加适量稀硫酸酸化,用0.0100 mol·L-1 标准KMnO4溶液滴定,当MnO 恰好完全被还原为Mn2+时,消耗KMnO4溶液的体积为20.00 mL。
恰好完全被还原为Mn2+时,消耗KMnO4溶液的体积为20.00 mL。
请回答下列问题:
①滴定终点的现象为____________。
②上述样品中(NH4)2SO4·FeSO4·6H2O晶体(相对分子质量为392)的质量分数为______。
③在上述方案的基础上,下列措施能进一步提高测定准确度的有_____(填字母)。
A.适当增加称量样品的质量 B.用盐酸替代H2SO4溶液
C.用酚酞做指示剂 D.多次实验,取平均值
-
下列关于铝及其化合物的说法不正确的是
A.Al既可用于食品包装,也可用做建筑材料
B.Al2O3既可用来冶炼金属Al,也可用做耐火材料
C.明矾[KAl(SO4)2·12H2O]因为有强氧化性,所以既可用做净水剂,也可用作消毒剂
D.Al(OH)3既可用作治疗胃酸过多的药物,也可用来制备一些铝盐