利用反应 8NH3+6NO212H2O+7N2 可脱除烟气中的 NO2。下列有关该反应的说法中正确的是
A.NH3是氧化剂
B.NO2发生氧化反应
C.还原性:NO2>N2
D.每生成 0.7mol N2,反应转移 2.4×6.02×1023 个电子
高一化学单选题中等难度题
利用反应 8NH3+6NO212H2O+7N2 可脱除烟气中的 NO2。下列有关该反应的说法中正确的是
A.NH3是氧化剂
B.NO2发生氧化反应
C.还原性:NO2>N2
D.每生成 0.7mol N2,反应转移 2.4×6.02×1023 个电子
高一化学单选题中等难度题
利用反应 8NH3+6NO212H2O+7N2 可脱除烟气中的 NO2。下列有关该反应的说法中正确的是
A.NH3是氧化剂
B.NO2发生氧化反应
C.还原性:NO2>N2
D.每生成 0.7mol N2,反应转移 2.4×6.02×1023 个电子
高一化学单选题中等难度题查看答案及解析
利用反应 8NH3+6NO2 12H2O+7N2可脱除烟气中的 NO2。下列有关该反应的说法中正确的是
A.NH3 是氧化剂
B.NO2 发生氧化反应
C.NO2在反应中得到电子
D.每生成 0.7mol N2,反应转移 2.4×6.02×1023个电子
高一化学多选题简单题查看答案及解析
利用某分子筛作催化剂,NH3可脱除废气中的NO和NO2,生成两种无毒物质,其反应历程如图所示,下列说法正确的是( )
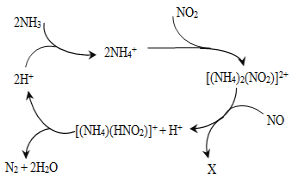
A.X是N2
B.NH中含有非极性共价键
C.NH3、NH、H2O中的质子数、电子数均相同
D.上述历程的总反应为:2NH3+NO+NO22N2+3H2O
高一化学单选题中等难度题查看答案及解析
氨气可以用来处理氮氧化物,例如氨气与二氧化氮发生如下反应:6NO2+8NH37N2+12H2O,下列关于该反应说法正确的是
A. NH3是氧化剂 B. H2O是氧化产物
C. NO2发生氧化反应 D. 生成1 mol H2O转移2 mol的电子
高一化学选择题困难题查看答案及解析
利用反应 6NO2 + 8NH3===7N2 + 12H2O 构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是 ( )
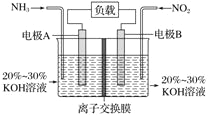
A. 电流从右侧电极经过负载后流向左侧电极
B. 为使电池持续放电,离子交换膜需选用阴离子交换膜
C. 电极 A 极反应式为 2NH3 - 6e- ===N2 + 6H+
D. 当有 4.48 L NO2( 标准状况 ) 被处理时,转移电子为 0.8 mol
高一化学单选题困难题查看答案及解析
NH3和NO2在催化剂作用下反应:8NH3+6NO2=7N2+12H2O。若还原产物比氧化产物少0.1 mol,则下列判断正确的是
A. 转移电子4.8NA个 B. 还原剂比氧化剂多0.2 mol
C. 生成气体的体积42.56 L(标准状况) D. 被还原的氮原子是11.2 g
高一化学单选题困难题查看答案及解析
NH3和NO2反应:8NH3+6NO2=7N2+12H2O。若还原产物比氧化产物少0.2 mol,下列判断正确的是( )
A. 转移电子7.2NA B. 生成气体的体积33.6 L(标准状况)
C. 还原剂比氧化剂多0.4 mol D. 被还原的氮原子是55.2 g
高一化学null困难题查看答案及解析
氮氧化物是造成雾霾天气的主要原因之一,消除氮氧化物有多种方法。
(1)目前,应用最广泛的烟气氮氧化物脱除技术是NH3催化还原法,化学反应可表示为:2NH3(g)+NO(g)+NO2(g)=2N2(g)+3H2O(g) △H<0。
①该反应中,反应物总能量_____(填“>”、“<”或“=”)生成物总能量。
②当该反应有2mol N2(g)生成时,转移电子的物质的量为______mol。
(2)也可以利用甲烷催化还原氮氧化物.已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ/mol
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ/mol
则CH4(g)将NO(g)还原为N2(g)的热化学方程式是______________。
(3)还可利用ClO2 消除氮氧化物的污染,反应过程如下(部分反应物或生成物略去):
NO NO2
 N2
N2
反应I的产物中还有两种强酸生成,且其中一种强酸为硝酸,且硝酸与NO2物质的量相等,则化学反应方程式为_____,反应中若生成22.4L N2(标准状况),则消耗ClO2_____g。
(4)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。
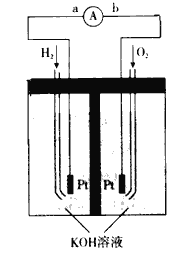
①氢氧燃料电池的能量转化主要形式是_______,工作时电流方向为____(用a、b和箭头表示)。
②负极的电极反应式为________________。
③电极表面镀铂粉的原因为____________。
高一化学综合题困难题查看答案及解析
氮氧化物是造成雾霾天气的主要原因之一,消除氮氧化物有多种方法。
(1)目前,应用最广泛的烟气氮氧化物脱除技术是NH3催化还原法,化学反应可表示为:2NH3(g)+NO(g)+NO2(g)== 2N2(g)+3H2O(g) △H<0
①该反应中,反应物总能量_______(填“>”、“<”或“=”)生成物总能量。
②当该反应有2mol N2(g)生成时,转移电子的物质的量为________mol。
③该反应中,还原剂为_______(填化学式),氧化产物与还原产物的质量比为_______。
(2)也可以利用甲烷催化还原氮氧化物,已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ/mol ;CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H2=-867kJ/mol
则CH4(g)将NO(g)还原为N2(g)的热化学方程式是_______。
(3)锌锰干电池是应用最普遍的电池之一(如图所示),总反应方程式为: Zn+2MnO2+2NH4Cl=ZnCl2+2NH3↑+Mn2O3+H2O
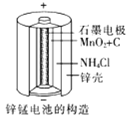
①锌锰干电池的负极材料是________,
②负极发生的电极反应方程式为:_______
③正极发生的电极反应方程式为:________。
④若反应消耗32.5 g 负极材料,则电池中转移电子的数目为_______。
高一化学综合题简单题查看答案及解析
将20 mL NO2和NH3的混合气体,在一定条件下充分反应,化学方程式为: 6NO2+8NH3=7N2+12H2O,已知参加反应的NO2比参加反应的NH3少2 mL(气体体积均在相同状况下测定),则原混合气体中NO2和NH3的物质的量之比是( )
①3:2 ②2:3 ③3:7 ④3:4
A.①③ B.②④ C.①② D.③④
高一化学选择题简单题查看答案及解析