处理某废水时,反应过程中部分离子浓度与反应进程关系如下图,反应过程中主要存在N2、HCO3−、ClO−、CNO−(C+4价,N-3价)、Cl−等微粒。下列说法不正确的是

A.该废水呈强酸性
B.废水处理后转化为无害物质
C.反应的离子方程式:3ClO−+2CNO−+H2O == N2+2HCO3−+3Cl−
D.每处理1 mol CNO−转移3 mol e−
高二化学单选题中等难度题
处理某废水时,反应过程中部分离子浓度与反应进程关系如下图,反应过程中主要存在N2、HCO3−、ClO−、CNO−(C+4价,N-3价)、Cl−等微粒。下列说法不正确的是

A.该废水呈强酸性
B.废水处理后转化为无害物质
C.反应的离子方程式:3ClO−+2CNO−+H2O == N2+2HCO3−+3Cl−
D.每处理1 mol CNO−转移3 mol e−
高二化学单选题中等难度题
处理某废水时,反应过程中部分离子浓度与反应进程关系如下图,反应过程中主要存在N2、HCO3−、ClO−、CNO−(C+4价,N-3价)、Cl−等微粒。下列说法不正确的是

A.该废水呈强酸性
B.废水处理后转化为无害物质
C.反应的离子方程式:3ClO−+2CNO−+H2O == N2+2HCO3−+3Cl−
D.每处理1 mol CNO−转移3 mol e−
高二化学单选题中等难度题查看答案及解析
根据环保要求,在处理有氰电镀废水时,剧毒的CN-离子在催化剂TiO2颗粒作用下,先用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),再在酸性条件下继续与NaClO反应生成N2、CO2和Cl2。环保工作人员在密闭系统中用如图装置进行实验,测定CN-被处理的百分率。
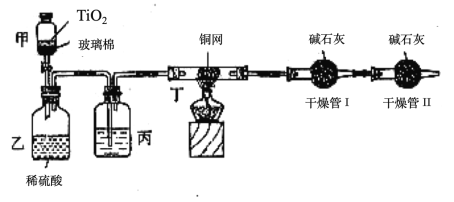
现将浓缩后含CN-离子的污水与过量NaClO溶液的混合液倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
(1)根据题意,写出相关主要反应的离子方程式:甲中的反应_________________,乙中的反应:_____________________。
(2)上述实验是通过测定CO2的量来确定对CN-的处理效果。丙装置中的试剂是______________,丁装置的目的是________________________;干燥管Ⅱ的作用是______________________。
(3)假定上述每一个装置都充分吸收,则利用该装置测得的CN-被处理的百分率与实际值相比_____(填“偏高”或“偏低”),简述可能的原因:______________________。
(4)含氰废水也可采用电化学方法进行处理。在碱性条件下,使用惰性电极电解含氰废水,氰离子被氧化为无毒的物质,其中阳极电极反应式是___________________。
高二化学实验题简单题查看答案及解析
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。
(1)含氰废水中的CN-有剧毒。在微生物的作用下,CN-能够被氧气氧化成HCO3-,同时生成NH3,该反应的离子方程式为_______。
(2)高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。
① Na2FeO4中铁元素的化合价是______价。
② 用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原因是_______(用离子方程式表示)。
③ 工业上可用FeCl3、NaOH 、NaClO三种物质在一定条件下反应制得Na2FeO4,完成下列化学方程式:2FeCl3 +10NaOH+3NaClO=2_____+5_____+9_______。
高二化学填空题困难题查看答案及解析
某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种离子。在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中不正确的是
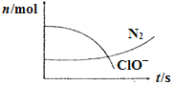
A.还原剂是含CN-的物质,氧化产物不只有N2
B.氧化剂是ClO-,还原产物是HCO3-
C.参与反应的氧化剂与还原剂的物质的量之比为2:5
D.标准状况下若生成2.24LN2则转移电子为1mol
高二化学多选题中等难度题查看答案及解析
某课题组采用活性炭回收海带化工提碘废水中残留的低浓度碘(主要以I-形式存在,杂质不参与反应),实验过程如下:
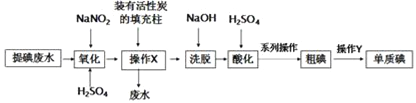
已知:3I2+6NaOH=5NaI+NaIO3+3H2O;
I2+2S2O32-=2I-+S4O62-。
请回答:
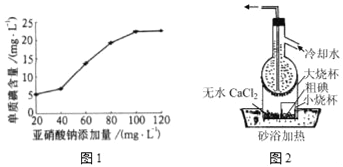
(1)结合图1可知,NaNO2最适宜的添加量为_____mg•L-1。
(2)操作X的目的是_____。
(3)系列操作中涉及抽滤操作,下列有关抽滤的说法中不正确的是_____。
A.选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B.当溶液具有强酸性、强氧化性时,可用玻璃砂漏斗代替布氏漏斗
C.抽滤不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
D.洗涤沉淀时,应开大水龙头,使洗涤剂快速通过沉淀物
(4)进行操作Y时所用装置如图2所示(省去了夹持装置),则操作Y的名称为_____;该装置中有两处不合理,请指出其中的一处_____。
(5)称取0.5080g粗碘试样于250mL碘量瓶中,加入足量的KI溶液,加盖摇匀至碘完全溶解.迅速用0.1200mol•L-1Na2S2O3标准溶液滴定至浅黄色,再加入淀粉指示剂,继续滴定至蓝色褪去即为终点,共消耗Na2S2O3标准溶液24.00mL。则粗碘试样中碘单质的纯度为_____。
高二化学简答题中等难度题查看答案及解析
电镀厂曾采用有氰电镀工艺,处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,在酸性条件下CNO-继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并通过测定二氧化碳的量确定CN-被处理的百分率。
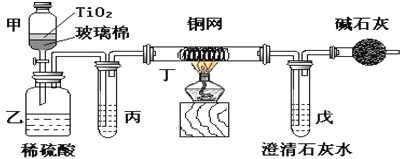
将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200 mL(其中CN-的浓度为0.05 mol•L-1倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
(1)甲中反应的离子方程式为________________________,乙中反应的离子方程式为________________________。
(2)乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等。丙中加入的除杂试剂是饱和食盐水,其作用是_____________________,丁在实验中的作用是______________,装有碱石灰的干燥管的作用是______________________________。
(3)戊中盛有含Ca(OH)2 0.02mol的石灰水,若实验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于__________。该测得值与工业实际处理的百分率相比总是偏低,简要说明可能原因之一_______________________。
高二化学实验题中等难度题查看答案及解析
一定温度下,向300 mL 1 mol/L的NaOH溶液中通入b mol CO2,下列说法正确的是
A.通入CO2过程中溶液的Kw减小
B.当b= 0.2时,所得溶液中部分离子浓度关系为:c (HCO3-) > c (CO32-) > c ( OH-) > c (H+)
C.b= 0.3与b= 0.15时,所得溶液中的微粒种类不相同
D.当恰好生成NaHCO3时,溶液中存在:c(Na+)+c(H+)==c(HCO3-)+c( OH-)
高二化学选择题极难题查看答案及解析
根据右表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )

A.c(HCO3-)>c(ClO-)>c(OH-)
B.c(ClO-)>c(HCO3-)>c(OH-)
C.c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)
D.c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-)
高二化学选择题中等难度题查看答案及解析
某氮肥厂氨氮废水中的氮元素多以NH和NH3·H2O的形式存在,该废水的处理流程如下:
(1)过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30℃,通空气将氨赶出并回收。
用离子方程式表示加NaOH溶液的作用:______________________________________。
(2)过程Ⅱ:在微生物作用的条件下,NH经过两步反应被氧化成NO
。两步反应的能量变化示意图如下:
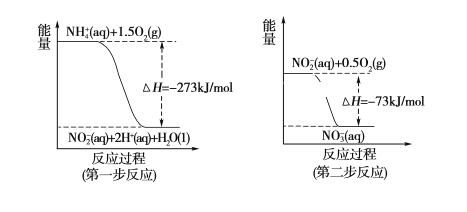
第一步反应是________反应(选填“放热”或“吸热”),判断依据是________。
(3)过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比是________。
高二化学填空题中等难度题查看答案及解析
根据右表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是

A. c(HCO3—)>c(ClO-)>c(OH-)
B. c(ClO-)>c(HCO3—)>c(H+)
C. c(HClO)+ c(ClO-)= c(HCO3—)+ c(H2CO3)
D. c(Na+)+ c(H+)= c(HCO3—)+c(ClO-)+c(OH-)
高二化学选择题困难题查看答案及解析