-
活性炭可处理大气污染物NO。为模拟该过程,T℃时,在3L密闭容器中加入NO和活性炭粉,反应体系中各物质的量变化如下表所示。下列说法正确的是
活性炭/mol
NO/mol
X/mol
Y/mol
起始时
2.030
0.100
0
0
10min达平衡
2.000
0.040
0.030
0.030
A. X一定是N2,Y一定是CO2
B. 10min后增大压强,NO的吸收率增大
C. 10min后加入活性炭,平衡向正反应方向移动
D. 0~10min的平均反应速率v(NO)=0.002 mol/(L•min)
高二化学单选题简单题查看答案及解析
-
活性炭可处理大气污染物NO。在2 L密闭容器中加入NO和活性炭(无杂质),反应方程式为NO+C
E+F(未配平)。当温度为T时,经过5 min达到平衡,测得平衡时各物质的物质的量如下表:
活性炭
NO
E
F
初始时(mol)
2.050
0.200
0
0
平衡时(mol)
2.000
0.100
0.050
0.050
则下列说法正确的是
A.该反应的平衡常数为1/4
B.增加活性炭的量,能缩短达到平衡所用的时间
C.容器中压强不变可以说明该反应达到平衡状态
D.达到平衡时,用E表示该反应的速率为0.01 mol·L-1·min-1
高二化学选择题中等难度题查看答案及解析
-
活性炭可处理大气污染物NO。在2 L密闭容器中加入NO和活性炭(无杂质),反应方程式为NO+C
E+F(未配平)。当温度为T时,经过5 min达到平衡,测得平衡时各物质的物质的量如下表:
活性炭
NO
E
F
初始时(mol)
2.050
0.200
0
0
平衡时(mol)
2.000
0.100
0.050
0.050
则下列说法正确的是
A.该反应的平衡常数为1/4
B.增加活性炭的量,能缩短达到平衡所用的时间
C.容器中压强不变可以说明该反应达到平衡状态
D.达到平衡时,用E表示该反应的速率为0.01 mol·L-1·min-1
高二化学选择题困难题查看答案及解析
-
活性炭可处理大气污染物NO。T℃时,在1L密闭容器中加入NO气体和炭粉,发生反应生成两种气体A和B,测得各物质的物质的量如下:
活性炭/mol
NO/mol
A/mol
B/mol
起始状态
2.030
0.100
0
0
2 min时
2.000
0.040
0.030
0.030
(1)2 min内,用NO表示该反应的平均速率v(NO)=________mol·L-1·min-1;
(2)该反应的化学方程式是________________________________________;
(3)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是_________。
①v(NO)∶v(A)∶v(B)=2∶1∶1
②混合气体的密度不再改变
③总压强不再改变
④混合气体的平均相对分子质量不再改变
(4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O。
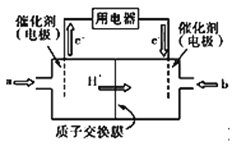
①a处通入的物质是________,电极反应式为:____________________;
②b处电极反应式为_________________________;
③电池工作时H+由________极移向_______极(填正、负极)。
高二化学填空题中等难度题查看答案及解析
-
活性炭可处理大气污染物NO,反应原理:C(s)+2NO(g)
N2(g)+CO2(g)。T℃时,在2L密闭容器中加入0.100molNO和2.030mol活性炭(无杂质),平衡时活性炭物质的量是2.000mol。下列说法不合理的是
A.该温度下的平衡常数是:K=
B.达到平衡时,NO的转化率是60%
C.3min末达到平衡,则v(NO)=0.01mol/(L·min)
D.若平衡时再加入0.100molNO,则达到新平衡时NO的转化率比原平衡时低
高二化学单选题中等难度题查看答案及解析
-
活性炭可处理大气污染物NO,反应原理:C(s)+2NO(g)
N2(g)+CO2(g)。T ℃时,在2 L密闭容器中加入0.100 mol NO和2.030 mol活性炭(无杂质),平衡时活性炭物质的量是2.000 mol。下列说法不合理的是( )
A. 该温度下的平衡常数:K=
B. 达到平衡时,NO的转化率是60%
C. 3 min末达到平衡,则v(NO)=0.01 mol·L-1·min-1 D. 升高温度有利于活性炭处理更多的污染物NO
高二化学选择题中等难度题查看答案及解析
-
研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
(1
)一定温度下,在2L的密闭容器中,SO2、O2、SO3三种气体的物质的量随时间变化的曲线如下图所示,请回答下列问题:
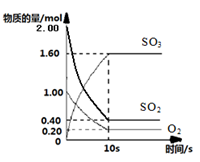
①反应的化学方程式为
②反应开始到10s,用SO2表示的反应速率为
③O2的平衡转化率为
(2)对于反应:2SO2(g)+O2(g)
2SO3(g),当反应达到平衡时,如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)= ;υ(SO3)= 。
(3)已知:2SO2(g)+O2(g)
2SO3(g)ΔH=-196.6kJ·mol-1
2NO(g)+O2(g)
2NO2(g)ΔH=-113.0kJ·mol-1
则反应NO2(g)+SO2(g)
SO3(g)+NO(g)的ΔH=_________kJ·mol-1。
(4)一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是_________
a、体系压强保持不变 b、混合气体颜色保持不变
c、SO3和NO的体积比保持不变 d、每消耗1 mol SO3的同时生成1 mol NO2
高二化学填空题简单题查看答案及解析
-
车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”。活性炭可处理大气污染物NO。在5 L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F。当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如下表:
物质
T/℃
活性炭
NO
E
F
初始
3.000
0.10
0
0
T1
2.960
0.020
0.040
0.040
T2
2.975
0.050
0.025
0.025
(1)写出NO与活性炭反应的化学方程式 ;
(2)计算上述反应T1℃时的平衡常数K1= ;
(3)上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为 ;
(4)右图为在T1℃达到平衡后在t2、t3、t4、t5时改变某一个反应条件,平衡体系中反应速率随时间变化的情况,且所改变的条件均不同。已知t3-t4阶段为使用催化剂。请判断该反应△H 0(填“>”或“<”)。
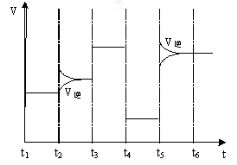
高二化学填空题极难题查看答案及解析
-
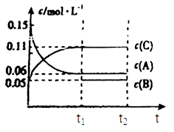
向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体,一定条件下发生反应,各物质浓度随时间变化如下左图所示。右图为t2时刻后改变容器中条件,平衡体系中速率随时间变化的情况,且四个阶段都各改变一种条件,所用条件均不同。已知t3-t4阶段为使用催化剂。
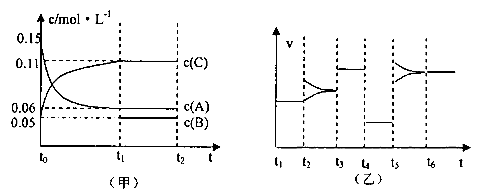
(1)若t1=15s,则t0—t1阶段以C浓度变化表示的反应速率v(C)为=_________________。
(2)若t2—t3阶段,C的体积分数变小,此阶段v(正)_____________v(逆)(填“>”“<”“=”)
(3)t4—t5阶段改变的条件为_________________,B的起始物质量为_________________。
(4)t5—t6阶段容器内A的物质的量共减小0.03mol,而此过程中容器与外界的热交换总量为akJ,写出该反应的热化学方程式_________________。
高二化学简答题困难题查看答案及解析
-
向某密闭容器中加入0.3mol A、0.1mol C和一定量的气体B三种气体,在一定条件下发生反应,各物质浓度随时间变化如下面左图所示。下面右图为t2时刻后改变容器中条件,平衡体系中速率随时间变化的情况且t2—t5四个阶段都各改变一种条件,所用条件均不同。t3—t4阶段为使用催化剂。

(1)若t1=15s,则t0—t1阶段以C浓度变化表示的反应速率为v(C)=________mol/(L∙s);
(2)若t2—t3阶段,C的体积分数变小,此阶段v正________v逆(填“大于”、“小于”或“等于”)
(3)B的起始物质的量为________mol;
(4)t1时刻,平衡常数K=________;
(5)t5—t6阶段容器内A的物质的量共减小0.03mol,而此过程中容器与外界的热交换总量为a KJ,写出该反应的热化学方程式________;
(6)若t2时刻后图像变化如下图,则改变条件为
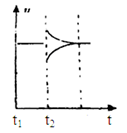
a.恒温恒压下,按照2:1比例充入任意量的B和C
b.恒温恒压下,加入0.24mol A、0.06mol B和0.14mol C
c.恒温恒压下,加入0.12mol A、0.1mol B和0.22mol C
d.恒温恒压下,加入0.14mol B和0.30mol C
高二化学填空题困难题查看答案及解析