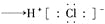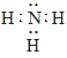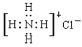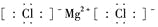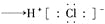-
碱金属元素和卤族元素广泛存在,用化学用语回答下列问题。
(1)氢氟酸可以用来雕刻玻璃。用电子式表示氟化氢的形成过程__________。
(2)过氧化钠可以用于潜水艇中氧气的来源,其与二氧化碳反应的化学方程式是_____。
(3)次氯酸钠溶液(pH>7)和溴化钠溶液混合,可以作为角膜塑形镜的除蛋白液。二者混合后,溶液变成淡黄色,该反应的离子方程式是_____________________。
(4)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl +S +SO2。组装该电池必须在无水条件下进行,原因是_____________(用化学方程式表示)。
(5)关于碱金属和卤族元素,下列说法一定正确的是____________。
A.从上到下,单质密度依次增大 B.从上到下,单质熔沸点依次升高
C.从上到下,原子半径依次增大 D.单质都可以与水反应
(6)常温下,KMnO4固体和浓盐酸反应产生氯气。为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
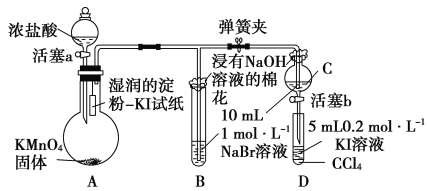
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
①验证氯气的氧化性强于碘的实验现象是____________________。
②B中溶液发生反应的离子方程式是__________________________。
③为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是______________。
-
碱金属元素和卤族元素广泛存在,用化学用语回答下列问题。
(1)氢氟酸可以用来雕刻玻璃。用电子式表示氟化氢的形成过程____________。
(2)过氧化钠可以用于潜水艇中氧气的来源,其与二氧化碳反应的化学方程式是________。
(3)次氯酸钠溶液(pH>7)和溴化钠溶液混合,可以作为角膜塑形镜的除蛋白液。二者混合后,溶液变成淡黄色,该反应的离子方程式是_________________________。
(4)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl +S +SO2。组装该电池必须在无水、无氧的条件下进行,原因是____________________(用化学方程式表示)。
(5)关于碱金属和卤族元素,下列说法一定正确的是____________。
A. 从上到下,单质密度依次增大 B. 从上到下,单质熔沸点依次升高
C. 从上到下,原子半径依次增大 D. 单质都可以与水反应
-
卤族元素是典型的非金属元素,其单质及其化合物具有广泛的用途。已知:KMnO4与浓盐酸常温下反应可生成氯气。根据所学化学知识及所给信息,回答下列有关问题:
(1)下列可以用来判断氯、溴、碘元素非金属性强弱的是 (填序号)。
①HCl、HBr、HI的热稳定性逐渐减弱;
②AgCl、AgBr、AgI的颜色逐渐加深;
③ HCl、HBr、HI的酸性依次减弱;
④ Cl2、Br2、I2的颜色逐渐加深;
⑤ Cl2、Br2、I2和H2反应条件由光照(或点燃)→ 一定温度→ 持续加热;条件由易到难;
⑥Cl2、Br2、I2的氧化性逐渐减弱。
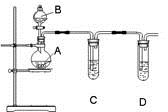
(2)某化学探究小组选用右图所示的装置和下列所给的试剂来证明非金属性:Cl>I,请你按照他们的设计思路完成该实验。
可供选择的试剂有:①浓盐酸,②硝酸银溶液,③KMnO4,④稀盐酸,⑤淀粉碘化钾溶液, ⑥MnO2, ⑦NaOH溶液;⑧浓硫酸
烧瓶A中应盛放的药品是 (填序号),试管C中应盛放的药品是 (填序号),则装置D的作用是 。观察到 现象,即可证明非金属性Cl>I。
(3)一定条件,在水溶液中1 mol Cl-、ClOX-(x=1,2,3,4)的能量(KJ)相对大小如图所示。
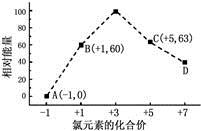
①D是 (填离子符号)。
②B→A+C反应的离子方程式为 ;生成1molC时, KJ的热(填吸收或放出以及具体数值)
-
用相应的化学用语回答下列问题
(1)用化学方程式说明实验室不能用带玻璃塞试剂瓶装NaOH溶液的原因_________
(2)用化学方程式说明用氢氟酸雕刻玻璃的原因_________
(3)生产过程中产生的SO2、Cl2等大气污染物,若将二者按照一定比例通入水中可减少或消除污染。写出该反应的离子反应方程式_______。
(4)Sr是第5周期第IIA族元素,用离子方程式表示SrCO3与稀盐酸的反应_____
-
下面关于硅及其化合物的叙述中,不正确的是( )
A.可用氢氟酸在玻璃上雕刻花纹
B.玻璃、陶瓷、水泥都属于传统的硅酸盐产品
C.硅胶可用作食品干燥剂
D.硅元素化学性质不活泼,在自然界中可以游离态形式存在
-
下面关于硅及其化合物的叙述中,不正确的是 ( )
A.可用氢氟酸在玻璃上雕刻花纹
B.晶体硅可用作半导体材料
C.硅胶可用作食品干燥剂
D.硅元素化学性质不活泼,在自然界中可以游离态形式存在
-
下列有关化学用语的表示正确的是( )
A. 的电子式:
的电子式:
B.氨的电子式: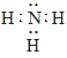
C.用电子式表示氯化氢的形成过程:
D.6 个质子 8 个中子的碳元素的核素符号:
-
用化学用语回答下列问题
(1)画出钾原子的原子结构示意图:____________。
(2)写出氨分子的结构式:__________________。
(3)用电子式表示氟化钙(CaF2)的形成过程:_________________。
(4)完成下表
| K层为最外层时,最多能容纳的电子数 | _________ |
| 除K层外,其他各层为最外层时,最多能容纳的电子数 | _________ |
| 次外层最多能容纳的电子数 | _________ |
| 倒数第3层最多能容纳的电子数 | _________ |
| 第n层里最多能容纳的电子数 | _________ |
-
下列有关化学用语的表示正确的是( )
A.NH4Cl的电子式: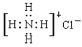
B.氨的电子式:
C.用电子式表示氯化氢的形成过程:
D.6个质子8个中子的碳元素的核素符号:14C
-
下列化学用语的书写,正确的是
A. 氯原子的结构示意图: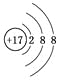
B. 6个质子8个中子的碳元素的核素符号:12C
C. 氯化镁的电子式: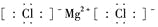
D. 用电子式表示氯化氢的形成过程: