-
下列说法中正确的是
①外围电子构型为nsnnpn的原子形成的化合物的种类最多; ②在硫酸铜氨溶液中加入乙醇有深蓝色晶体析出; ③H2O是一种非常稳定的化合物,这是由于H2O分子间存在氢键所致; ④P4、BF3、CH3Cl三种分子中所有原子的最外层均满足8e-稳定结构; ⑤乙醇分子中只含σ键. ⑥键角是描述分子立体结构的重要参数,键长的大小与成键原子的半径和成键数目有关,键能越大,键长越长,共价化合物越稳定
A.①③⑤正确 B.③④⑥正确 C.①②⑤正确 D.⑤正确,其他均不正确
高二化学单选题中等难度题查看答案及解析
-
下列说法中正确的是( )
①外围电子构型为nsnnpn的原子形成的化合物的种类最多
②在硫酸铜溶液中加入过量氨水最后生成深蓝色溶液
③H2O是一种非常稳定的化合物,这是由于H2O分子间存在氢键所致
④P4、BF3、CH3Cl三种分子中所有原子的最外层均满足8e﹣稳定结构
⑤乙醇分子中只含σ键.
A.①③⑤ B.③④ C.①②⑤ D.⑤
高二化学单选题中等难度题查看答案及解析
-
将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出晶体Cu(NH3)4SO4·H2O。
(1)Cu2+基态核外电子排布式为 ;
的空间构型为 。(用文字描述)
(2)乙醇分子中氧原子轨道杂化类型为 。与NH3互为等电子体的一种阳离子为 (填化学式)。
(3)1mol[Cu(NH3)4]2+中σ键的数目为 。
(4)某含有结晶水的铜的氯化物的晶胞结构如图所示,该化合物的化学式是 。
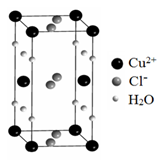
高二化学填空题简单题查看答案及解析
-
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液;在深蓝色溶液中加入等体积的95%乙醇,深蓝色溶液变浑浊,静置后有深蓝色晶体析出。下列对此现象说法正确的是
A.[Cu(NH3)4]SO4中所含的化学键有离子键、极性键和配位键
B.[Cu(NH3)4]2+的空间构型为平面正方形,中心离子Cu2+采用sp3杂化
C.[Cu(NH3)4]SO4会与乙醇发生反应生成深蓝色晶体
D.[Cu(NH3)4]SO4含有NH3分子,其水溶液中也含有NH3分子
高二化学选择题困难题查看答案及解析
-
向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解病得到深蓝色的透明液体;若向试管中加入一定量乙醇,析出深蓝色晶体。结合有关知识,回答下列问题:
(1)Cu、N、O、S元素第一电离能由大到小的顺序是_______(填元素符号);蓝色沉淀溶解时发生反应的离子方程式是________________。
(2)Cu(NH3)4SO4·H2O晶体中中心离子是_______,配体是_____,配位数是_____,存在的化学键有____________(填字母序号)。
a.离子键 b.极性键 c.非极性键 d.配位键
(3)SO42-的空间构型是_____________,其中S原子的杂化轨道类型是___________,SO3的空间构型是_________,其中S原子的杂化轨道类型是_______,属于______分子(填“极性”或“非极性”)。
(4)已知纳米氧化亚铜(Cu2O)是一种用途广泛的光电材料,已知高温下Cu2O比CuO稳定。
①写出基态Cu+的价电子排布式____________;按照元素周期表分区,Cu属于____区。
②从核外电子排布角度解释高温下Cu2O比CuO更稳定的原因____________。
高二化学简答题中等难度题查看答案及解析
-
向盛有硫酸铜水溶液的试管里滴入氨水,首先形成难溶物,继续滴加氨水,难溶物溶解得到深蓝色透明溶液。若加入乙醇将析出深蓝色晶体。下列说法正确的是
A. 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B. 在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3提供孤对电子
C. 沉淀溶解后将生成深蓝色的正四面体形的配离子[Cu(NH3)4]2+
D. 加入极性较小的溶剂乙醇后,将析出[Cu(H2O)4]SO4•H2O晶体
高二化学单选题中等难度题查看答案及解析
-
向盛有硫酸铜水溶液的试管里滴入氨水,首先形成难溶物,继续滴加氨水,难溶物溶解得到深蓝色透明溶液。若加入乙醇将析出深蓝色晶体。下列说法正确的是
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3提供孤对电子
C.沉淀溶解后将生成深蓝色的正四面体形的配离子[Cu(NH3)4]2+
D.加入极性较小的溶剂乙醇后,将析出[Cu(H2O)4]SO4•H2O晶体
高二化学选择题中等难度题查看答案及解析
-
向硫酸铜水溶液中逐滴加入氨水,先形成蓝色沉淀,继续滴加氨水,沉淀溶解,得到深蓝色的透明溶液,再向溶液中加入乙醇有深蓝色晶体(化学式为[Cu(NH3)4]SO4·H2O)析出。
(1)写出上述实验前两步反应的离子方程式__________,____________。
(2)铜元素基态原子的电子排布式为_________________,铜单质晶体中的原则堆积模型属于_________堆积(填堆积模型名称)。
(3)在上述深蓝色晶体所含的非金属元素中,电负性最大的是_________(填元素符号),第一电离能最大的是_________(填元素符号)。该晶体中的阴离子的立体构型是_________,阴离子的中心原子的杂化方式为_________。
(4)氨的沸点_________(填“高于”或“低于”)膦(PH2),原因是_____________。
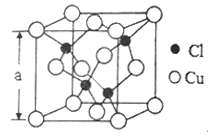
(5)Cu的一种氯化物晶胞结构如图所示,该氯化物的化学式是______________。若该晶体的密度为pg·cm-3,以NA表示阿伏伽德罗常数,则该晶胞的边长为a=_____________nm。
高二化学填空题中等难度题查看答案及解析
-
下列说法不正确的是
A. 向硫酸铜溶液中加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解后得到深蓝色的透明溶液,形成该溶液是因为产生了配合离子[Cu(NH3)4] 2+
B. NH4+的空间构型是正四面体形
C. 氨气极易溶于水的重要原因之一:氨分子与水分子之间能形成氢键
D. 由于氢键的作用,使NH3、H2O、HF的沸点反常,且沸点高低顺序为HF>H2O>NH3
高二化学选择题中等难度题查看答案及解析
-
铜及其化合物是人类最早使用的金属材料,铜及其化合物在现代的生产生活中仍然具有极其重要的作用。将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出深蓝色的晶体。
(1)乙醇常温是液体而乙烷是气体的最主要原因:__________________;[Cu (NH3)4 ]SO4中,存在的化学键类型有 ______(填选项)。
A、离子键 B、金属键 C、配位键 D、非极性键 E、极性键
(2)乙醇可以在铜做催化剂的条件下被氧化为乙醛,请问乙醛分子中碳原子杂化类型为 ______。
(3)上述实验中涉及到的元素中,四种非金属元素的电负性由大到小的顺序为 ______。
(4)上述实验中最终析出的晶体的化学式是_________
A、[Cu (NH3)4]SO4•H2O B、[Cu (NH3)4]SO4•3H2O C、[Cu (NH3)4]SO4•5H2O
(5)[Cu (NH3)4 ]2+具有对称的空间构型,[Cu (NH3)4 ]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu (NH3)4 ]2+的空间构型为__________。
(6)1mol[Cu (NH3)4 ]2+中含有σ键数目为___________mol
(7)从结构的角度分析NH3 比NF3的键角大的原因:___________________
高二化学填空题中等难度题查看答案及解析