-
含硫化合物多为重要的化工原料。请回答下列问题:
I.多硫化物是含多硫离子(Sx2-)的化合物,可用作废水处理剂、硫化剂等。
(1)Na2S2的电子式为___。
(2)Na2S5(易溶于水)在酸性条件下可生成H2S和S,该反应的离子方程式为___。
(3)黄铁矿(FeS2)是工业上制硫酸的重要原料,在氧气中煅烧生成Fe2O3和SO2,其煅烧的化学方程式为___。
II.焦亚硫酸钠(Na2S2O5)是一种食品抗氧化剂,易溶于水。
(4)焦亚硫酸钠(Na2S2O5)中硫元素的化合价为___。
(5)向某些饮料中添加少量焦亚硫酸钠(Na2S2O5),可降低饮料中溶解氧的含量,发生反应的离子方程式为__。
(6)向饱和碳酸钠溶液中通入过量SO2可制得焦亚硫酸钠,发生反应的化学方程式为__。
高一化学解答题中等难度题查看答案及解析
-
含硫化合物多为重要的化工原料。请回答下列问题:
I.多硫化物是含多硫离子(Sx2-)的化合物,可用作废水处理剂、硫化剂等。
(1)Na2S2的电子式为___。
(2)Na2S5(易溶于水)在酸性条件下可生成H2S和S,该反应的离子方程式为___。
(3)黄铁矿(FeS2)是工业上制硫酸的重要原料,在氧气中煅烧生成Fe2O3和SO2,其煅烧的化学方程式为___。
II.焦亚硫酸钠(Na2S2O5)是一种食品抗氧化剂,易溶于水。
(4)焦亚硫酸钠(Na2S2O5)中硫元素的化合价为___。
(5)向某些饮料中添加少量焦亚硫酸钠(Na2S2O5),可降低饮料中溶解氧的含量,发生反应的离子方程式为__。
(6)向饱和碳酸钠溶液中通入过量SO2可制得焦亚硫酸钠,发生反应的化学方程式为__。
高一化学解答题中等难度题查看答案及解析
-
(11分)离子反应是中学化学中重要的反应类型,回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有 (填编号)。
①单质 ②氧化物 ③化合物 ④盐
(2)可用图示的方法表示不同反应类型之间的关系。如分解反应和氧化还原反应可表示为下图。请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系。
(3)有一瓶澄清的溶液,其中可能含有H+ 、NH4+ 、Mg2+ 、Ba2+ 、Al3+ 、I- 、NO3-、CO32- 、
SO42-、AlO2- ,取该溶液进行以下实验:
①取pH试纸检验,表明溶液呈强酸性。排除_________离子存在。
②取出部分溶液,加入少量CCl 4 及数滴新制氯水,经振荡后CCl4 呈紫红色,可以排除_______存在。
③另取部分溶液逐渐加入NaOH溶液,使溶液从酸性逐渐变为碱性,在反应过程中均无沉淀产生,则可排除_________的存在。
④取部分上述碱性溶液加Na 2 CO 3溶液,有白色沉淀生成,证明______存在,又排除________存在。
⑤根据上述实验事实还不能确定是否存在的离子是____ ____;
高一化学填空题中等难度题查看答案及解析
-
(1)铁及其化合物在生活、生产中有广泛的应用。请回答下列问题:
①黄铁矿(FeS2,二硫化亚铁)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为3FeS2+8O2=6SO2+Fe3O4,氧化产物为_____,若有3mol FeS2参加反应,转移__________mol电子。
②FeCl3与氢碘酸反应时可生成棕色物质I2,该反应的离子方程式为_________________。
(2)对反应NH3+O2—NO+H2O(未配平,反应条件略去)作分析,该反应中,还原剂是_______,还原产物是________,被还原的物质是_________。参加反应的氧化剂为3.2g时,反应转移的电子的物质的量为________________。
(3)对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施。含氰废水中的CN-有剧毒。在微生物的作用下,CN-能够被氧气氧化成HCO
,同时生成NH3,该反应的离子方程式为____________(提示:反应过程中N元素化合价不发生改变)。
高一化学填空题中等难度题查看答案及解析
-
离子反应是中学化学中重要的反应类型.回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有______
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)可用图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为下图.请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系.
(3)离子方程式是重要的化学用语.下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点.①所有的离子方程式均可以表示一类反应 ②酸碱中和反应均可表示为:H++OH-=H2O 高一化学解答题中等难度题查看答案及解析
-
离子反应是中学化学中重要的反应类型,回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有_______(填序号)。
①单质;②氧化物;③电解质;④盐;⑤化合物
(2)将两种化合物一起溶于水得到一种无色透明的溶液,溶液中含有下列离子中的某些离子: K+、Mg2+、Fe3+、Ba2+、SO42-、OH-、CO32-和Cl-,取该溶液进行如下实验:取少量溶液滴入紫色石蕊试液,溶液呈蓝色。取少许溶液滴入BaCl2溶液,无白色沉淀产生。另取少许溶液滴入AgNO3 溶液,产生不溶于稀硝酸的白色沉淀。再取少许原溶液滴入H2SO4溶液,有白色沉淀产生。
①根据以上现象判断,原溶液中肯定不存在的离子是_______________________________;肯定存在的离子是________________________,可能存在的离子是____________________
②在该溶液中加入AgNO3 溶液发生反应的离子方程式为_______________________________
高一化学填空题中等难度题查看答案及解析
-
离子反应是中学化学中重要的反应类型,回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在_____________(填编号)。
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)将两种化合物一起溶于水得到一种无色透明溶液,溶液中含有下列离子中的某些离子:K+、Mg2+、Fe3+、Ba2+、SO42-、OH-、CO32-和Cl-,取该溶液进行如下实验:
Ⅰ取少量溶液滴入紫色石蕊试液,溶液呈蓝色。
Ⅱ取少许溶液滴入BaCl2溶液,无白色沉淀产生。
Ⅲ取少许溶液先滴加硝酸再加AgNO3溶液,产生白色沉淀。
Ⅳ再取少许原溶液滴入少量H2SO4溶液,有白色沉淀产生。
①根据以上现象判断,原溶液中肯定不存在的离子是__________;肯定存在的离子是________。
②写出实验Ⅲ和Ⅳ中可能发生反应的离子方程式:
Ⅲ、 _________________________________ ,__________________________________。
Ⅳ、___________________________________。
③如溶液中各种离子的浓度相等,确定溶液中_________(填有或无)K+,判断依据是________。
高一化学综合题中等难度题查看答案及解析
-
Ⅰ.离子反应和氧化还原反应都是高中化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有______。(填序号)
①单质 ②化合物 ③氧化物 ④酸 ⑤碱 ⑥盐 ⑦电解质
人们常用图示法表示不同反应类型之间的关系,如化合反应和氧化还原反应的关系可用图1表示。图2为离子反应、氧化还原反应和置换反应三者之间的关系,则表示置换反应的是____(填字母),请写出符合图2阴影部分的一个离子方程式______。
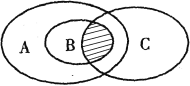
图1 图2
Ⅱ.现有失去标签的四瓶无色溶液A,B,C,D,只知它们是K2CO3,K2SO4,Na HSO4和Ba(NO3)2,为鉴别它们,进行如下实验:
①A+D→溶液+气体 ②B+C→溶液+沉淀
③B+D→溶液+沉淀 ④A+B→溶液+沉淀
⑤将④得到的沉淀物加入③所得的溶液中,沉淀很快溶解并产生无色无味的气体。
根据以上实验事实,请完成如下问题:
(3)写出各物质化学式:A__________;B__________;C__________;D__________。
(4)写出实验③中反应中相关的离子方程式。____________________________。
(5)书写离子方程式
①NaHCO3溶液与H2SO4溶液混合:_________________________。
②向石灰水中通入过量二氧化碳________________________________。
③氢氧化亚铁和浓盐酸反应____________________________________。
④醋酸溶液和碳酸镁悬浊液混合生成气体并得到澄清溶液______________________________。
高一化学填空题简单题查看答案及解析
-
离子反应、氧化还原反应都是中学化学中重要的反应类型。请回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有_____________。
A.单质 B.氧化物 C.电解质 D.盐 E.化合物
(2)人们常用图示的方法表示不同反应类型之间的关系。如分解反应和氧化还原反应可表示为下图。右图为离子反应、氧化还原反应和置换反应三者之间的关系,则表示离子反应、氧化还原反应、置换反应的字母依次是_____________

(3)将NaBr溶液加入AgC1沉淀中,产生AgBr黄色沉淀。从离子反应发生的条件分析,AgCl与AgBr相比较,溶解度较大的是_____________。
(4)已知某氧化还原反应Au2O3 + 4Na2S2O3 + 2H2O =Au2O+ 2Na2S4O6 +4NaOH
① 用单线桥标出电子转移的方向和数目________________。
② 反应中,被氧化的元素是______________,氧化剂是_________________。
③ 比较该反应中氧化剂和氧化产物的氧化性相对强弱_________________________。
高一化学综合题中等难度题查看答案及解析
-
NH3是重要的化工原料。
(1)工业生产硝酸的尾气中含有氮氧化物NOx(NO和NO2的混合物,假设不含N2O4),对生态环境和人类健康带来较大的威胁。工业上可用氨催化吸收法处理NOx,反应原理为:4x NH3 + 6NOx
(2 x + 3)N2 + 6x H2O
某化学兴趣小组模拟该处理过程的实验装置如下(夹持装置已略去):
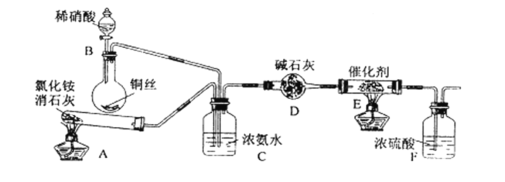
①装置A中发生反应的化学方程式为____________________。
②装置B中发生反应的化学方程式为____________________。
③装置D中碱石灰的作用是__________________________。
(2)按下图装置进行NH3性质实验。
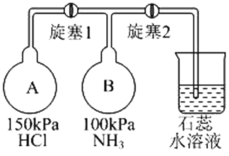
①先打开旋塞1,B瓶中的现象是_________________________________ ,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是_________________ 。
(3)下图是甲同学设计收集氨气的几种装置,其中可行的是________,集气的原理是________。
a.
b.
c.
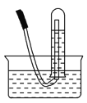 d.
d. (4)为防止污染环境,以下装置(盛放的液体均为水)可用于吸收多余氨气的是________(填序号)。
①.
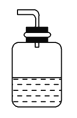 ②.
②. 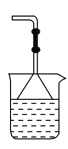 ③.
③.  ④.
④. 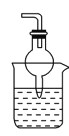
高一化学实验题中等难度题查看答案及解析