-
A、B、C、D、E、F、G七种前四周期元素且原子序数依次增大,A原子中各个电子层的电子数目相等,B的基态原子有3个不同的能级且各能级中电子数相等,D的基态原子与B的基态原子的未成对电子数目相同,E与元素C属于同一主族, F2+的3d轨道有9个电子,G原子第N电子层有3对成对电子,请回答下列问题:
(1)根据对角线规则,请写出A元素最高价氧化物对应水化物与NaOH反应的离子方程式: 。
(2)F的基态原子电子排布式为 。
(3)C、D、E原子的第一电离能由小到大的顺序为 (用元素符号回答)
(4)已知EG3分子中E与G之间的共用电子对偏向G,且EG3分子遇水会猛烈的发生水解反应,请写出EG3中心原子E的杂化类型是 , EG3遇水反应的化学方程式: 。
(5)向FSO4(aq)中逐滴加入氨水至过量,会观察到 现象。后一步反应的离子反应方程式为: 。
高二化学填空题简单题查看答案及解析
-
前四周期元素A、B、C、D、E的原子序数依次增大,基态A原子核外电子占锯3个轨道,基态B原子核外电子占据3个能级且每个能级上电子数相等,C的双原子单质分子中σ键和π键数目之比为1:2,D的最高正化合价和最低负化合价之和等于4;基态E原子核外有6个未成对电子。
(1)基态E原子的核外电子排布式为______;基态D原子核外电子占据的能量最高的能级符号为_____________。
(2)A元素的各级电离能如下:
能级(I)
I1
I2
I3
I4
I5
电离能/kJ·mol-1
800.6
2427
3660
25026
32827
分析上表数据知,相邻两个电子的电离能中,I3和I4之间差异最大,其主要原因是______________。
(3)A、B、C元素的最高价氧化物对应的水化物酸性依次增强,其原因是________。
(4)氯元素与A、B、C元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp3杂化、立体构型为三角锥形的是_______(填分子式)。
(5)(DC)4为热色性固体,且有色温效应。低于-30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色。在淡黄色→橙黄色→深红色的转化中,破坏的作用力是____;在常压下,(DC)4高于130℃分解为相应的单质,这一变化中破坏的作用力是_______。在B、C、D的简单气态氢化物中,属于非极性分子的是______(填分子式,下同),常与Cu2+、Zn2+、Ag+等形成配离子的是_______________。
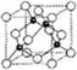
(6)A、C形成立方晶体,晶体结构类似金刚石,如图所示。已知:该晶体密度为ρg·㎝-3,NA代表阿伏伽德罗常数的值。
①该晶体的化学式为__________。
②在该晶体中,A与C形成共价键的键长(d)为_____pm。
高二化学推断题困难题查看答案及解析
-
X、Y、Z、M、R五种元素的原子序数依次增大,只有X、Y、Z为短周期元素,相关信息如表:
元素
相关信息
X
基态原子核外有3个能级,且各能级电子数目相等
Y
常见化合价只有0、-1、-2
Z
单质为黄绿色有毒气体
M
第四周期d区元素,基态原子的核外有6个未成对电子
R
第五周期,与X处于同一主族
(1)元素X、Y电负性的大小顺序是______(用元素符号表示)。
(2)XYZ2分子中所有原子均满足8电子构型,分子中σ键与π键的数目比为______。
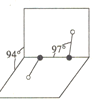
(3)元素Y可形成一种氢化物的空间结构如图所示,中心原子Y的杂化方式是______,该分子为______(填“极性”或“非极性”)分子。
(4)元素M基态原子的价电子排布式为______,MO5中M的化合价为+6价,则该分子中含有过氧键的数目为______。
(5)元素R与Z可形成化合物RZ2,用价层电子对互斥理论推断该分子的空间构型为______,分子中Z-R-Z的键角______120°(填“>”、“=”或“<”)。
高二化学推断题中等难度题查看答案及解析
-
A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
A
原子核外有6种不同运动状态的电子
C
基态原子中s电子总数与p电子总数相等
D
原子半径在同周期元素中最大
E
基态原子最外层电子排布式为3s23p1
F
基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反
G
基态原子核外有7个能级且能量最高的能级上有6个电子
H
是我国使用最早的合金中的最主要元素
请用化学用语填空:
(1) A元素在元素周期表中的位置________;A、B、C三种元素的第一电离能由大到小的排序为_____(用元素符号填写);
(2) B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为____,B元素所形成的单质分子中σ键与π键数目之比为____。
(3) G元素的低价阳离子的离子结构示意图是________,F元素原子的外围电子排布图是________,H元素的基态原子核外电子排布式是________。
(4) D元素的单质及其常见化合物的焰色反应主要利用了原子光谱中的______(A.原子吸收光谱B.原子发射光谱)
(5) 上述元素属于p区的是_______(用元素符号填写);
高二化学推断题中等难度题查看答案及解析
-
A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
A
原子核外有6种不同运动状态的电子
C
基态原子中s电子总数与p电子总数相等
D
原子半径在同周期元素中最大
E
基态原子最外层电子排布式为3s23p1
F
基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反
G
基态原子核外有7个能级且能量最高的能级上有6个电子
H
是我国使用最早的合金中的最主要元素
请用化学用语填空:
(1)A元素位于元素周期表第_______周期_______族;C元素和F元素的电负性比较,较小的是________。
(2)D的单质在空气中燃烧时火焰的颜色是__________________,请用原子结构的知识解释发光的原因:__________________________。
(3)H元素位于元素周期表的_________区。基态E原子的L层电子排布图为__________。
(4)B元素与宇宙中含量最丰富的元素形成的最简单化合物的VSEPR模型为________,B元素与同周期相邻两元素的电离能大小关系为______________ , 请解释原因__________________________________。
(5)G元素的低价阳离子的离子结构示意图是________,F元素原子的价电子的电子排布图是________。
(6)在基态G中,电子占据的最高能层符号为________,该能层具有的原子轨道数为____________。
(7)G的高价阳离子的溶液与H单质反应的离子方程式为___________________________;
(8)与E元素成对角线关系的某元素的最高价氧化物的水化物具有两性,写出该两性物质与D元素的最高价氧化物的水化物反应的离子方程式:________________________。
高二化学填空题中等难度题查看答案及解析
-
A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
A
原子核外有6种不同运动状态的电子
C
基态原子中s电子总数与p电子总数相等
D
原子半径在同周期元素中最大
E
基态原子价层电子排布式为3s23p1
F
基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反
G
基态原子核外有7个能级且能量最高的能级上有6个电子
H
是我国使用最早的合金中的最主要元素
请用化学用语填空:
(1)A元素在元素周期表中的位置______,B元素和C元素的第一电离能比较,较大的是___________,C元素和F元素的电负性比较,较小的是_____________。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的分子构型为____________,B元素所形成的单质分子中
键与π数目之比为_________。
(3)G元素的低价阳离子的结构示意图是_________________,F元素原子的价电子排布图是__________,H元素的基态原子核外电子排布式是________________________________________。
(4)G的高价阳离子的溶液与H单质反应的离子方程式为_____________________________;与E元素成对角关系的某元素的最高价氧化物对应的水化物具有两性,该两性物质与D元素的最高价氧化物对应的水化物反应的化学方程式为________________________________。
高二化学填空题困难题查看答案及解析
-
X、Y、Z、M、Q、R是元素周期表前四周期元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
X
原子核外有6种不同运动状态的电子
Y
基态原子中s电子总数与p电子总数相等
Z
原子半径在同周期元素中最大
M
逐级电离能(kJ·mol-1)依次为 578、1817、2745、11575、14830、18376
Q
基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反
R
基态原子核外有7个能级且能量最高的能级上有6个电子
请用化学用语填空:
(1)X元素位于元素周期表第____周期____族; R是________区的元素。
(2)请写出Q元素基态原子的外围电子排布图____。
(3)X、Y、Z、M四种元素的原子半径由小到大的顺序是________。(用元素符号表示)
(4)R元素可形成R2+和R3+,其中较稳定的是R3+,原因是________。
(5)含Z元素的焰火显黄色,主要与________有关。
(6)M元素原子的逐级电离能越来越大的原因是________。
(7)与M元素成“对角线规则”关系的某短周期元素T的最髙价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物的水化物反应的化学方程式:________;己知T元素和Q元素的电负性分别为1.5和3.0,则它们形成的化合物是________。(填“离子化合物”或“共价化合物”)
高二化学推断题简单题查看答案及解析
-
X、Y、Z、M、Q、R是元素周期表前四周期元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
X
原子核外有6种不同运动状态的电子
Y
基态原子中s电子总数与p电子总数相等
Z
原子半径在同周期元素中最大
M
逐级电离能(kJ/mol)依次为 578、1 817、2 745、11 575、14 830、18 376
Q
基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反
R
基态原子核外有7个能级且能量最高的能级上有6个电子
请用化学用语填空:
(1)请写出Q元素基态原子的外围电子排布图:_______。
(2)X、Y、Z、M四种元素的原子半径由大到小的顺序是__________(用元素符号表示)。
(3)R元素可形成R2+和R3+,其中较稳定的是R3+,原因是__________。
(4)写出Z元素的原子核外电子排布式_________。
(5)Q元素原子的未成对电子个数是________ 个。
高二化学综合题中等难度题查看答案及解析
-
X、Y、Z、M、Q、R是元素周期表前四周期元素,且原子序数依次增大,其相关信息如下表:
元素
相关信息
X
原子核外有6种不同运动状态的电子
Y
基态原子中s电子总数与p电子总数相等
Z
原子半径在同周期元素中最大
M
逐级电离能(kJ·mol-1)依次为 578、1817、2745、11575、14830、18376
Q
基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反
R
基态原子核外有7个能级且能量最高的能级上有6个电子
请用化学用语填空:
(1)X元素位于元素周期表第____周期____族; R是________区的元素。
(2)请写出Q元素基态原子的外围电子排布图____。
(3)X、Y、Z、M四种元素的原子半径由小到大的顺序是________。(用元素符号表示)
(4)R元素可形成R2+和R3+,其中较稳定的是R3+,原因是________。
(5)含Z元素的焰火显黄色,主要与________有关。
(6)M元素原子的逐级电离能越来越大的原因是________。
(7)与M元素成“对角线规则”关系的某短周期元素T的最髙价氧化物的水化物具有两性,写出该两性物质与Z元素的最高价氧化物的水化物反应的化学方程式:________;己知T元素和Q元素的电负性分别为1.5和3.0,则它们形成的化合物是________。(填“离子化合物”或“共价化合物”)
高二化学推断题简单题查看答案及解析
-
X、Y、Z、W、Q、R为原子序数依次增大的前四周期元素。其相关信息如下表:
元素代号
相关信息
X
原子核外电子总数与周期序数相等
Y
原子核外电子占3个不同能级,且每个能级上排布的电子数相同
Z
最简单气态氢化物能使湿润的红色石蕊试纸变蓝
W
原子的L电子层上有2对成对电子
Q
元素的最高正价与最低负价的代数和为6
R
单质是日常生活中用途最广、用量最大的金属材料
请回答下列问题:
(1)基态R原子的核外电子排布式为________,R与YW易形成配合物R(YW)5,在R(YW)5中R 的化合价为_________。
(2)Y、Z、W三种元素的电负性由小到大的顺序为_________(用元素符号表示)。
(3)基态Q原子的最高能层具有的原子轨道数为________。
(4)下列关于Y2X2的说法中正确的是______(填字母)。
A. Y2X2中的所有原子都满足8电子稳定结构
B.每个Y2X2分子中σ键和π键数目之比为1:1
C. Y2X2是由极性键和非极性键构成的非极性分子
D. Y2X2的分子构型为直线形
(5)ZQ3中心原子的杂化轨道类型为______,其分子空间构型为_______。
高二化学简答题困难题查看答案及解析