-
工业废气的氮氧化物(NO、NO2等,用通式NOx表示)是主要的大气污染物之一。为了保护环境,工业上常通入氨气与之发生反应:NOx+NH3→N2+H2O(未配平)。有关此反应,下列说法中正确的是( )
A.当x=2时,有1 mol气体被还原,转移的电子为2 mol
B.当x=1时,每生成2.5 mol N2,被氧化的气体有4 mol
C.无论x为何值,N2既是氧化产物又是还原产物
D.当x=2时,反应通式配平后H2O的化学计量数为8
高三化学选择题中等难度题查看答案及解析
-
工业废气的氮氧化物(NO、NO2等,用通式NOx表示)是主要的大气污染物之一.为了保护环境,工业上常通入氨气与之发生反应:NOx+NH3→N2+H2O(未配平).有关此反应,下列说法中正确的是( )
A.当x=2时,有1mol气体被还原,转移的电子为2mol
B.当x=1时,每生成2.5molN2,被氧化的气体有4mol
C.无论x为何值,N2既是氧化产物又是还原产物
D.当x=2时,反应通式配平后H2O的化学计量数为8高三化学选择题中等难度题查看答案及解析
-
工业废气中的氮氧化物(如NO、NO2等,用通式NOx表示)是主要的大气污染物之一.为了保护环境,工业上常通入氨气与之发生如下反应:NOx+NH3―→N2+H2O来消除污染.有关此反应,下列说法中错误的是
A.N2既是氧化产物又是还原产物
B.当x=1时,每生成2.5 mol N2,被氧化的气体有3 mol
C.当x=2时,有1 mol气体被还原,转移电子4 mol
D.反应通式配平表示为:6NOx+4xNH3===(3+2x)N2+6xH2O
高三化学选择题中等难度题查看答案及解析
-
工业废气的氮氧化物(如NO、NO2等,用通式NOx表示)是主要的大气污染物之一。为了保护环境,工业上常通入氨气与之发生如下反应:NOx+NH3→N2+H2O。有关此反应,下列说法中错误的是
A.N2既是氧化产物又是还原产物
B.反应通式配平为6NOx+4xNH3=(3+2x)N2+6xH2O
C.当x=1时,每生成2.5mol N2,被氧化的气体有3mol
D.当x=2时,有1mol气体被还原时,转移的电子为4mol
高三化学选择题中等难度题查看答案及解析
-
工业废气中氮氧化物是造成污染的主要来源之一.为了防治污染,工业上常通入氨气与氮氧化物反应:NOx+NH3→N2+H2O.现有NO、NO2的混合气体3L,可用同温同压下的NH3 3.5L恰好与它完全反应生成N2.则原混合气体中NO和NO2的物质的量之比为
A.1∶1 B.1∶2 C.1∶3 D.1∶4
高三化学选择题简单题查看答案及解析
-
为了保护环境,工业上常用氨气除去废气中氮氧化物(NOx):NOx+NH3→N2+H2O(l)。已知某厂每升废气中含NOx 0.0672L(只含NO和NO2),向100.000L废气中通入10.000L氨气可使NOx完全转化,测得反应后气体体积变为103.952L(气体体积均折算到标准状况)。有关说法中正确的是
A.每生成1.5mol N2,被氧化的气体有3mol
B.处理过程中转移的电子数约为1.339NA
C.NOx 中的 x 值为1.2
D.除去废气中的NOx,至少需氨0.24mol
高三化学选择题中等难度题查看答案及解析
-
工业废气中氮氧化物是主要污染物,为了治理污染,常通入NH3,发生反应NOx+NH3―→N2+H2O来治理污染.现有NO、NO2的混合气体3 L,用同温同压下3.5 LNH3使其恰好完全转化为N2,则混合气体中NO、NO2的物质的量之比为( )
A.1∶1 B.1∶3 C.2∶1 D.1∶4
高三化学选择题中等难度题查看答案及解析
-
氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2。某同学在实验中对NH3与NO2反应进行了探究。回答下列问题:
(1)氨气的制备
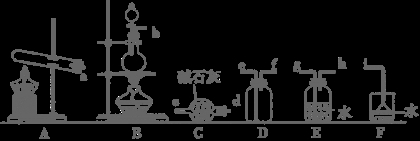
①氨气的发生装置可以选择上图中的 ,反应的化学方程式为 。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→ (按气流方向,用小写字母表示)
(2)氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2 (两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。
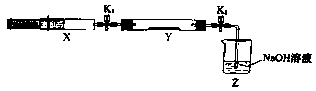
操作步骤
实验现象
解释原因
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中
①Y管中
②反应的化学方程式
将注射器活塞退回原处并固定,待装置恢复到室温
Y管中有少量水珠
生成的气态水凝聚
打开
③
④
高三化学实验题困难题查看答案及解析
-
工业废气和汽车尾气含有多种氮氧化物,以NOx表示,NOx能破坏臭氧层,产生光化学烟雾,是造成大气污染的来源之一。按要求回答下列问题:
(1)NO2与N2O4存在以下转化关系:2NO2(g)
N2O4(g)。
①已知:标准状况(25℃、101kPa)下,由最稳定的单质生成1mol化合物的焓变(或反应热),称为该化合物的标准摩尔生成焓。几种氧化物的标准摩尔生成焓如表所示:
物质
NO(g)
NO2(g)
N2O4(g)
CO(g)
标准摩尔生成焓/(kJ·mol-1)
90.25
33.18
9.16
-110.53
则NO2转化成N2O4的热化学方程式为__。
②将一定量N2O4投入固定容积的恒温容器中,下述现象能说明反应达到平衡状态的是__(填标号)。
A.v(N2O4)=2v(NO2) B.气体的密度不变
C.
不变 D.气体的平均相对分子质量不变
③达到平衡后,保持温度不变,将气体体积压缩到原来的一半,再次达到平衡时,混合气体颜色____填“变深”“变浅”或“不变”),判断理由是___。
(2)在容积均为2L的甲、乙两个恒容密闭容器中,分别充入等量NO2,发生反应:2NO2(g)
2NO(g)+O2(g)。保持温度分别为T1、T2,测得
n(NO2)与n(O2)随时间的变化如图所示:
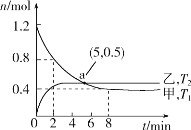
①T1时,反应从开始到第2min,平均速率v(O2)=__,该温度下平衡常数K=__。
②实验测得:v正=k正c2(NO2),v逆=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响,下列有关说法正确的是__(填标号)。
A.反应正向放热
B.a点处,v逆(甲)<v逆(乙)
C.k正(T2)>k正(T1)
D.温度改变,k正与k逆的比值不变
(3)硫代硫酸钠(Na2S2O3)在碱性溶液中是较强的还原剂,可用于净化氧化度较高的NOx废气,使之转化为无毒、无污染的N2。请写出NO2与硫代硫酸钠碱性溶液反应的离子方程式:__。
高三化学综合题简单题查看答案及解析
-
工业废气中氮氧化合物是造成污染的主要来源.为治污,工业上通常通入NH3与之发生下列反应:NOX+NH3→N2+H2O.现有NO、NO2的混合气3L,可用同温同压下的3.5LNH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比( )
A.1:3
B.2:1
C.1:1
D.1:4高三化学选择题中等难度题查看答案及解析