-
下表是元素周期表的一部分。
1
①
2
②
③
3
④
⑤
⑥
⑦
根据表中元素的位置,回答下列问题:
(1)元素②最外层有____个电子,最低负化合价为____。
(2)元素③、④、⑦的简单离子中,半径最小的是____(填离子符号,下同),半径最大的是____。
(3)元素②、⑥的单质与元素①的单质反应生成的化合物中,____(填化学式)更稳定,①、②形成的另一 种化合物可用于漂白,是利用其________。
(4)实验室中,元素⑤的氢氧化物可由铝盐与____反应生成,其氢氧化物能溶于表中____(填序号) 的最高价氧化物对应的水化物中。
高一化学填空题中等难度题查看答案及解析
-
下表为元素周期表短同期的一部分, A、B、C、D、E五种元素在周期表中的位置如下图所示。C元素的原子最外层电子数为次外层的3倍。
A
E
C
B
D
回答下列问题:
(1)B元素在周期表中的位置为__________。
(2)D的最高价氧化物对应水化物的化学式为__________。
(3)下列事实能说明C元素的非金属性比硫元素的非金属性强的是__________。
a.C单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molC单质比1molS得电子多
c.C和S两元素的简单氢化物受热分解,前者的分解温度高
d. C元素的简单氢化物沸点高于S元素的简单氢化物
(4)B与D两元素的单质反应生成化合物M,它的结构类似甲烷,写出M的电子式_____。
(5)A与镁形成的1mol化合物N与水反应,生成2molMg(OH)2和1mol气态烃,该烃分子中碳氢质量比为9:1,写出N与水反应的化学方程式______________________________。
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol/LNaOH溶液和1molO2,则两种气体的分子式及物质的量分别为__________。
高一化学综合题中等难度题查看答案及解析
-
根据A-K在周期表中的位置(如图),回答下列问题:
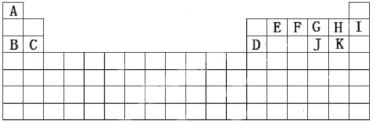
(1)最外层电子数是次外层电子数2倍的元素在周期表中的位置______________,化学性质最不活泼的元素是____________________(填化学符号或者化学式,下同)。
(2)E元素最高价氧化物的电子式____________________。
(3)D的最高价氧化物与K的最高价氧化物对应的水化物反应的离子方程式为_______________。
(4)A分别与F、G、H形成的简单化合物中,稳定性由强到弱的顺序为____________。
(5)C、D、G、H、J离子半径由大到小的顺序是___________________。
(6)用电子式表示化合物
的形成过程:_________________________。
高一化学推断题简单题查看答案及解析
-
不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如右图所示.试根据元素在周期表中的位置,分析图中吗线的变化特点,并回答下列问题.
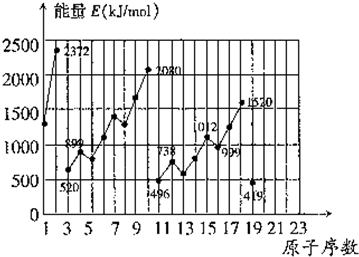
(1)同主族内不同元素的E值变化的特点是:______.各主族中E值的这种变化特点体现了元素性质的______变化规律.
(2)同周期内,随原子序数增大,E值增大.但个别元素的E值出现反常.现试预测下列关系式中正确的是______(填写编号)①E(砷)>E(硒) ②E(砷)<E(硒) ③E(溴)>E(硒) ④E(溴)<E(硒)
(3)估计1mol气态Ca原子失去最外层一个电子所需能量E值的范围:______<E<______.
(4)10号元素E值较大的原因是______.高一化学解答题中等难度题查看答案及解析
-
(17分)根据下表部分短周期元素的性质或原子结构,用化学用语回答下列问题。
元素编号
元素性质或原子结构
R
元素所处的周期数、主族序数、原子序数均相等
T
最外层电子数是次外层电子数的2倍
X
元素最高正价+7价
Y
第三周期金属元素中原子半径最小
Z
常温下单质为双原子分子,其氢化物水溶液呈碱性
(1)写出元素T的原子结构示意图________;元素Z单质的电子式________;写出X在周期表中的位置; 元素T的最高价氧化物的结构式________.
(2)探寻物质的性质差异是学习的重要方法之一。上述T、X、Y、Z四种元素最高价氧化物的水化物的酸性最强的是________(填化学式),其中化学性质明显不同于其他三种化合物的
是________(填化学式),理由是。
(3)写出R、T、X、三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的一种物质的化学式________
(4)由表中元素形成的常见物质A、B、C、D、E可发生以下反应:
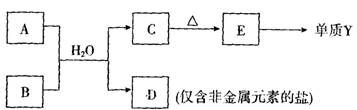
A溶液与B溶液(呈碱性)反应的离子方程式为________。
D中含有化学键的类型是________,属于________(填“离子”或“共价”)化合物。
高一化学填空题中等难度题查看答案及解析
-
根据下表部分短周期元素的性质或原子结构,用化学用语回答下列问题.
(1)写出元素T的原子结构示意图________;元素Z单质的电子式________; 元素T的最高价氧化物的结构式________.元素编号 元素性质或原子结构 R 元素所处的周期数、主族序数、原子序数均相等 T 最外层电子数是次外层电子数的2倍 X 元素最高正价+7价 Y 第三周期金属元素中原子半径最小 Z 常温下单质为双原子分子,其氢化物水溶液呈碱性
(2)探寻物质的性质差异是学习的重要方法之一.上述T、X、Y、Z四种元素最高价氧化物的水化物的酸性最强的是________(填化学式)
(3)写出R、T、X三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的一种物质的化学式________.高一化学填空题中等难度题查看答案及解析
-
下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
请根据要求用元素符号或化学式回答下列问题:a b c d e f g h i j m n o
(1)表中所列元素中,原子最外层有2个电子的元素为______.
(2)画出d元素原子的结构示意图______,其气态氢化物溶于水显______性.(填“酸”或“碱”)
(3)比较元素g和元素h形成的最高价氧化物的水化物的碱性强弱______>______.
(4)表中j元素在元素周期表中的位置是______.
(5)表中所列元素中,最高价氧化物对应水化物碱性最强的是______(填写化合物的化学式,下同),具有两性的是______.高一化学解答题中等难度题查看答案及解析
-
下图是元素周期表的一部分,根据元素在周期表中的位置回答下列问题,
①
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
(1)元素⑤在周期表中的位置描述为____________,元素⑧的元素符号__________________。
(2)元素①~⑩的最高价氧化物的水化物中,碱性最强的是________________(填化学式)。
(3)元素②的单质的电子式______________,元素②的简单氢化物与其最高价氧化物的水化物反应,生成物中含有的化学键________________(填“离子键”、“极性键”或“非极性键”),元素①、②、③的简单氢化物的沸点由高到低的顺序是___________________(用化学式表示)。
(4)非金属性比较
a.装置1可用于比较元素①、②、⑤的非金属性强弱,则B中发生反应的离子方程式为:_______。
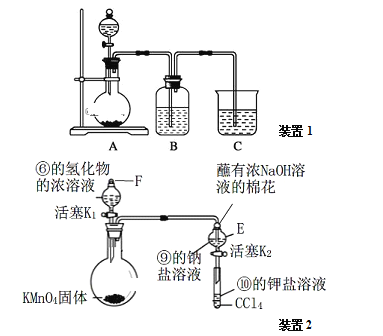
b.打开装置2中玻璃塞F和活塞K1,使液体滴入烧瓶中,待E中溶液颜色不再变化后,打开活塞K2,将E中溶液滴入小试管中,关闭活塞K2,取下小试管振荡,静置,下层液体呈现紫红色。上述实验_______(填“能”或“不能”)证明非金属性⑥>⑨>⑩。
高一化学综合题简单题查看答案及解析
-
下表是元素周期表的一部分。
根据①~⑿元素在周期表中的位置,回答下列有关问题:(请用化学符号填写)
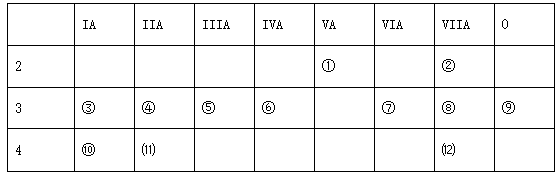
(1)写出下列元素符号:① ,⑥ 。
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 。(用化学式填写)
(3)在这些元素中单质的氧化性最强的是 ,还原性最强的是 。化学性质最不活泼的元素是 。(用化学式填写)
(4)画出原子结构示意图:⑾ 。
(5)用电子式表示⑦和⑩形成化合物的过程: 。
(6)⑦和⑧分别形成的气态氢化物的化学式是 、 。其中相对不稳定的是 。
(7)在③与④中,化学性质较活泼的是 ,(填元素符号)
在⑧与⑿中,化学性质较活泼的是 ,(填元素符号)如何证明(用离子方程式表示):
。
高一化学填空题简单题查看答案及解析
-
下表是元素周期表的一部分。
根据①~⑫元素在周期表中的位置,回答下列有关问题:(请用化学符号填写)
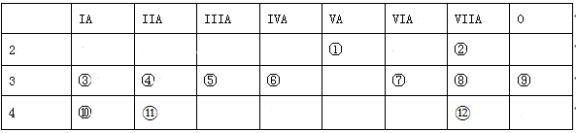
(1)写出下列元素符号:① ,⑥ 。
(2)在这些元素的最高价氧化物对应水化物中,酸性最强的是 ,呈两性的氢氧化物是 。(用化学式填写)
(3)在这些元素中单质的氧化性最强的是 ,还原性最强的是 。化学性质最不活泼的元素是 。(用化学式填写)
(4)用电子式表示⑦和⑩形成化合物的过程: 。
(5)⑦和⑧分别形成的气态氢化物中相对不稳定的是 。
高一化学填空题中等难度题查看答案及解析