-
某同学完成如下探究实验:
实验目的:比较Cl2、Br2、I2三种单质的氧化性强弱
实验药品:NaBr溶液、KI溶液、氯水、淀粉溶液
实验记录:
| 实验步骤 | 实验现象 | 实验结论 |
| 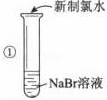
| 溶液变为橙黄色 | Ⅰ________ |
| 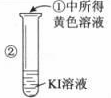
| 溶液变为黄色 | 氧化性:Br2>I2 |
| 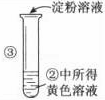
| Ⅱ___________ |
反思与评价:
(1)Ⅰ________;Ⅱ________。
(2)步骤①反应的离子方程式为:________。
(3)检验②中所得黄色溶液含I2的另一种方法是(简述实验操作和相应的实验现象)________。
(4)你认为上述实转设计(填“能”或“不能)____达到实验目的,理由是_______。
-
下述实验能达到预期目的的是 ( )
| 编号 | 实验内容 | 实验目的 |
| A | 将SO2通入酸性KMnO4溶液中,使其褪色。 | 证明SO2具有漂白性 |
| B | 将Cl2通入NaBr溶液中 | 比较Cl2与Br2的氧化性强弱 |
| C | 除去CO2中混有少量的CO,点燃燃烧 | 除去CO杂质 |
| D | 盐酸与Na2CO3反应生成CO2 | 证明非金属性:Cl > C |
-
(10分)为了比较卤素单质的氧化性强弱,可在实验室先制取Cl2(利用MnO2与浓盐酸反应可制取Cl2),并将Cl2依次通入NaBr溶液和KI-淀粉溶液中。如图所示仪器及药品,试回答:
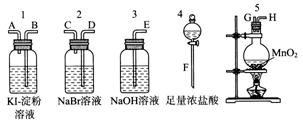
(1)若所制取气体从左向右流向时,上述仪器接口的连接顺序为________接________、________接________、________接________、________接________。(填字母)
(2)实验开始后装置5中反应的离子方程式为______________________________。
(3)装置3的作用是__________________________________,反应的离子方程式为_______________________________。
(4)装置1中产生的现象是:溶液先变蓝一段时间后蓝色褪去,生成两种强酸,请写出蓝色褪去的化学方程式:___________________________________________________。
-
某研究性学习小组进行如下探究活动:
实验目的:探究Cl2、Br2、I2的氧化性强弱。
查阅资料:①常温下,高锰酸钾与浓盐酸反应产生氯气;②溴单质易挥发,碘单质易升华;③淀粉溶液遇到碘单质变蓝色;④溴、碘在不同溶剂中所形成溶液(从稀到浓)的颜色变化如图所示。
| 水 | 四氯化碳 |
| 溴 | 黄→棕 | 橙→橙红 |
| 碘 | 深黄→褐 | 紫→深紫 |
实验方案:该小组设计下图所示装置实验(夹持仪器已略去,装置气密性完好)
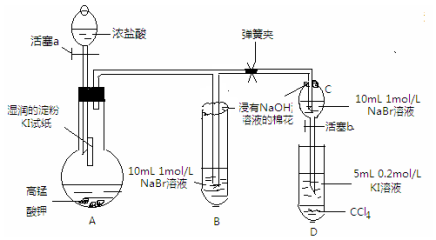
实验过程:
Ⅰ 先打开弹簧夹,再打开活塞a,滴加浓盐酸
Ⅱ 当B和C中的溶液都变黄时,加紧弹簧夹
Ⅲ 当B中的溶液由黄色变为棕色时,关闭活塞a
Ⅳ … …
回答以下问题:
(1)验证氯气的氧化性强于碘的实 验现象是 ,写出该反应的化学方程式 ;
验现象是 ,写出该反应的化学方程式 ;
(2)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 ,写出该反应的离子方程式 ;
(3)由实验得到的氯、溴、碘单质的氧化性由强到弱的顺序为  ;
;
(4)你认为实验中为什么要加过程Ⅲ这一步操作,请简述个人观点
-
某研究性学习小组进行如下探究活动:
实验目的:探究Cl2、Br2、I2的氧化性强弱。
查阅资料:①常温下,高锰酸钾与浓盐酸反应产生氯气;②溴单质易挥发,碘单质易生华;③淀粉溶液遇到碘单质变蓝色;
④溴、碘在不同溶剂中所形成溶液(从稀到浓)的颜色变化如图所示。
| 水 | 四氯化碳 |
| 溴 | 黄→棕 | 橙→橙红 |
| 碘 | 深黄→褐 | 紫→深紫 |
实验方案:该小组设计下图所示装置实验(夹持仪器已略去,装置气密性完好)
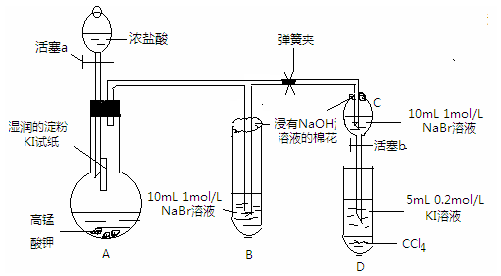
实验过程:
Ⅰ 先打开弹簧夹,再打开活塞a,滴加浓盐酸
Ⅱ 当B和C中的溶液都变黄时,加紧弹簧夹
Ⅲ 当B中的溶液由黄色变为棕色时,关闭活塞a
Ⅳ … …
回答以下问题:
⑴验证氯气的氧化性强于碘的实验现象是________,写出该反应的化学方程式________;
⑵为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是________,写出
该反应的离子方程式________;
⑶由实验得到的氯、溴、碘单质的氧化性由强到弱的顺序为________;
⑷你认为实验中为什么要加过程Ⅲ这一步操作,请简述个人观点
-
(9分)为了比较卤素单质的氧化性强弱,可在实验室先制取Cl2,并将Cl2依次通入NaBr溶液和淀粉KI溶液中。有如下图所示的仪器(橡胶塞均为双孔)及药品,试回答:
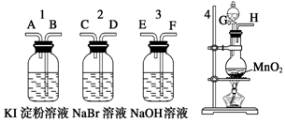
(1)若所制气体从左向右流向时,上述仪器接口的连接顺序为H接____、___接___、___接___。
(2)装置3的作用是_______________,反应的离子方程式为________________________。
(3)装置1中产生的现象是_________________,反应的化学方程式为_______________。
(4)通过本实验可得到的结论是____________________________________。
-
为了比较卤素单质的氧化性强弱可在实验室先制取Cl2(利用MnO2与浓盐酸反应可制取Cl2)并将Cl2依次通入NaBr溶液和KI淀粉溶液中。如图所示仪器及药品试回答: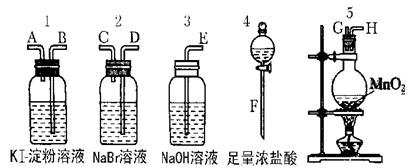
(1)若所制取气体从左向右流向时上述仪器接口的连接顺序为F接G、H接______、______接______、A接E。
(2)实验开始后装置5中反应的化学方程式为______________________。
(3)装置3的作用是________________________
反应的离子方程式为______________________________________。
(4)装置1中产生的现象是___________ 反应的离子方程式为____________________。
(5)若溴离子的还原性弱于碘离子的还原性,通过实验,卤素单质的氧化性由强到弱的顺序为__________________。
-
下面是某同学完成的探究实验报告的一部分:
实验名称:卤素单质的氧化性强弱比较
实验药品:KBr溶液、KI溶液、氯水、溴水、碘水、四氯化碳、淀粉碘化钾试纸。
实验设计如下
| 实验步骤 | 实验结论 |
| ①氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 | 氧化性从强到弱的顺序:氯、溴、碘 |
| ②NaBr溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 |
| ③KI溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 |
下列有关该实验的说法不正确的是( )
A. 完成该实验需用到的实验仪器有试管和胶头滴管
B. CCl4在实验中所起的作用是萃取剂
C. ③中反应的离子方程式为Cl2+2I-===2Cl-+I2
D. 上述步实验能很好的探究卤素单质的氧化性强弱
-
下述实验不能达到预期目的的是( )
| 编号 | 实验内容 | 实验目的 |
| A | 将铜片分别与浓、稀硝酸反应 | 探究浓、稀硝酸氧化性的相对强弱 |
| B | 将Cl2通入NaBr溶液中,然后加入CCl4,振荡、静置 | 比较氯与溴的氧化性强弱 |
| C | 将SO2通入酸性KMnO4溶液中 | 证明SO2具有漂白性 |
| D | 向盛有20 g蔗糖的烧杯中加入几滴水,搅拌均匀。再加入少许浓硫酸,迅速搅拌 | 探究浓硫酸的脱水性 |
-
下述实验不能达到预期目的是( )
| 选项 | 实验内容 | 实验目的 |
| A | 将铜片分别与浓、稀硝酸反应 | 探究浓、稀硝酸氧化性的相对强弱 |
| B | 将Cl2通入NaBr溶液中,然后加入CCl4,振荡、静置 | 比较氯与溴的氧化性强弱 |
| C | 将SO2通入酸性KMnO4溶液中 | 证明SO2具有漂白性 |
| D | 向盛有20g蔗糖的烧杯中加入几滴水,搅拌均匀,再加入少许浓硫酸,迅速搅拌 | 探究浓硫酸的脱水性 |







