-
(10分)试回答下列各问题:
(1)如图Ⅰ所示是1 mol NO2和CO反应生成 CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:________。
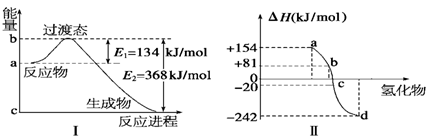
(2)化学反应的焓变与反应物和生成物的键能有关。
①已知:H2(g)+Cl2(g) === 2HCl(g) ΔH=-185 kJ/mol;
键能ΔH298(H—H)=436 kJ/mol,ΔH298(Cl—Cl)=247 kJ/mol,则ΔH298(H—Cl)=________。
②图Ⅱ表示氧族元素中的氧、硫、硒(Se)、碲生成氢化物时的焓变数据,根据这组焓变数据可确定a、b、c、d分别代表的元素,试写出硒化氢发生分解反应的热化学方程式:________。
(3)已知: ①Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g) ΔH=-a kJ/mol
2Fe(s)+3CO2(g) ΔH=-a kJ/mol
②3Fe2O3(s)+CO(g)  2Fe3O4(s)+CO2(g) ΔH=-b kJ/mol
2Fe3O4(s)+CO2(g) ΔH=-b kJ/mol
③Fe3O4(s)+CO(g)  3FeO(s)+CO2(g) ΔH=+ckJ/mol
3FeO(s)+CO2(g) ΔH=+ckJ/mol
则FeO(s) +CO(g)  Fe(s)+CO2(g) ΔH=-________。
Fe(s)+CO2(g) ΔH=-________。
-
试回答下列各问题:
(1)如图Ⅰ所示是1 mol NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:________________________________________________________________________。
(2)化学反应的能量变化与反应物和生成物的键能有关。
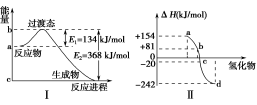
①已知: H2(g)+Cl2(g) = 2HCl(g) ΔH=-185 kJ/mol;
E(H—H)=436 kJ/mol,E(Cl—Cl)=247 kJ/mol,则E(H—Cl)=________。
②图Ⅱ表示氧族元素中的氧、硫、硒、碲生成氢化物时的ΔH数据,根据ΔH数据可确定a、b、c、d分别代表哪种元素,试写出硒化氢在标准状况下,发生分解反应的热化学方程式:
________________________________________________________________________。
(3)已知:Fe2O3(s)+3CO(g) = 2Fe(s)+3CO2(g) ΔH=-25 kJ/mol ①
3Fe2O3(s)+CO(g) = 2Fe3O4(s)+CO2(g) ΔH=-47 kJ/mol ②
Fe3O4(s)+CO(g) = 3FeO(s)+CO2(g) ΔH=+19 kJ/mol ③
请写出CO还原FeO的热化学方程式:_______________________________________________________。
-
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
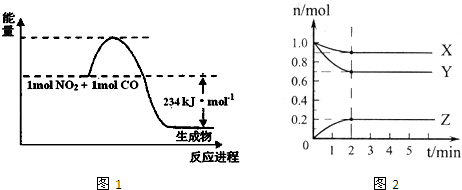
(1)如图1是1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图(图中涉及物质均为气态),请写出NO2和CO反应的热化学方程式 。
(2)在0.5L的密闭容器中,充入一定量的氮气和氢气进行反应,三种气体的物质的量随时间的变化曲线如图2所示。则Y是 ,2min内N2的反应速率υ(N2)= 。
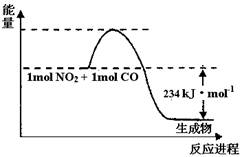
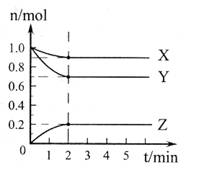
图1 图2
(3)硝酸工业在国民经济、国防工业和航天事业中占有重要地位。随着化学纤维、近代有机合成、火箭、导弹等工业的迅速发展,需要使用大量的硝酸。
①工业生产中用铂系金属作为催化剂,用氨氧化法制取硝酸。第一步反应为氨在催化剂作用下与氧气发生反应生成NO,写出反应化学方程式 。
②铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3 → Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)。反应中还原产物是 ,0.6mol Cu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则得到标准状况下气体体积为 L。
-
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.请回答下列问题:
(1)如图1是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图(图中涉及物质均为气态),请写出NO2和CO反应的热化学方程式________.
(2)在0.5L的密闭容器中,充入一定量的氮气和氢气进行反应,三种气体的物质的量随时间的变化曲线如图2所示.则Y是________,2min内N2的反应速率υ(N2)=________.
(3)硝酸工业在国民经济、国防工业和航天事业中占有重要地位.随着化学纤维、近代有机合成、火箭、导弹等工业的迅速发展,需要使用大量的硝酸.
①工业生产中用铂系金属作为催化剂,用氨氧化法制取硝酸.第一步反应为氨在催化剂作用下与氧气发生反应生成NO,写出反应化学方程式________.
②铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平).反应中还原产物是________,0.6mol Cu被硝酸完全溶解后,如果得到的NO和NO2物质的量相同,则得到标准状况下气体体积为________L.
-
请回答下列问题:
Ⅰ.如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图(图中涉及物质均为气态),请写出NO2和CO反应的热化学方程式:______
Ⅱ.现有①BaCl2②水晶③金属铝④Na2SO4⑤冰⑥碘片六种物质,按下列要求回答(填编号,下同):
(1)熔化时不需要破坏化学键的是_______,熔化时需要破坏共价键的是_______,能导电的是______。
(2)属于离子化合物的是________,只有离子键的物质是________,属于共价化合物的是______。
(3)①的电子式是________;⑤的结构式是________,⑤的空间构型是______,⑤中分子间作用力除了范德华力外,还含有______,因此而引起一些特殊的性质,请举出一种:______。
-
参考下列图表和有关要求回答问题。
(1)图Ⅰ是1 mol NO2(g)和1 molCO(g)反应生成CO2和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________,ΔH的变化是________(填“增大”“减小”或“不变”)。请写出NO2和CO反应的热化学方程式____________________;
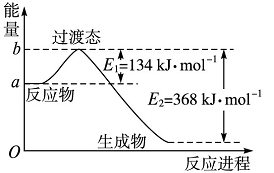
图Ⅰ
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1
则甲醇完全燃烧的热化学方程式为________________________;
(3)下表是部分化学键的键能数据:
| 化学键 | P—P | P—O | O=O | P=O |
| 键能/(kJ·mol-1) | a | b | c | x |
已知白磷的标准燃烧热ΔH为-d kJ·mol-1,白磷及其完全燃烧的产物结构如图Ⅱ所示,则上表中x=__________kJ·mol-1(用含有a、b、c、d的代数式表示)。
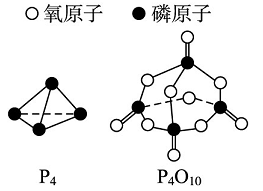
图Ⅱ
-
(1)右图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式 。
(2)己知下列热化学方程式:
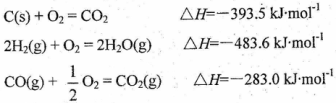
由此可知反应: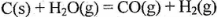 的焓变为 。
的焓变为 。
(3)在一固定体积的密闭容器中,进行如下化学反应
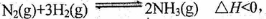 其化学平衡常数K与t的关系如下表:
其化学平衡常数K与t的关系如下表:

请完成下列问题:
①试比较K1、K2的大小,K1 K2(填写“>”“=”或“<”)
②下列各项能作为判断该反应达到化学平衡状态的依据的是 (填写字母序号)
A.容器内N2、H2、NH3的浓度之比为1:3:2
B.2v(正)(N2)=v(逆)(H2)
C.容器内压强保持不变
D.混合气体的密度保持不变
E.混合气体的平均相对分子质量不再改变
F.混合气体中各成分的浓度不再改变
-
试回答下列各题:
(1)如图1所示是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: ______________________________。
(2)化学反应的焓变与反应物和生成物的键能有关。
①已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ·mol-1

请填空:
| 共价键 | H—H | Cl—Cl | H—Cl |
| 键能/(kJ·mol-1) | 436 | 247 | ________ |
②图2中表示氧族元素中氧、硫、硒、碲生成氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素,试写出硒化氢在热力学标准状态下,发生分解反应的热化学方程式: ___________________________________。
-
Ⅰ己知1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化如下图所示。
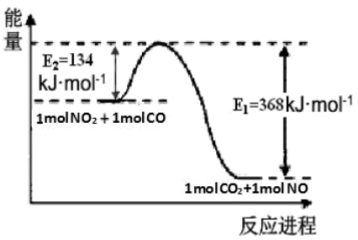
(1)请写出NO2和CO反应的热化学方程式________________________。
Ⅱ某温度时,在0.5L密闭容器中,某一反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析求得:
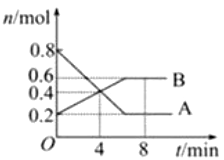
(2)该反应的化学方程式为_________________。
(3)反应开始至4min时,B的平均反应速率为___________。
(4)第4min时,正、逆反应速率的大小关系为:v(正)_______v(逆)(填“>”、“<”或“=”,下同)。
(5)第8min时,v(正)______v(逆)。
-
(1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:_______________________________________________________。
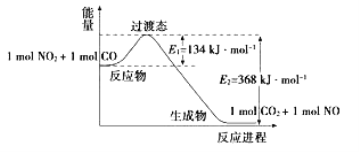
(2)总反应:Pb + PbO2 + 2H2SO4 = 2PbSO4 + 2H2O写出下列的电极反应式
负极:_____________________________
正极:_____________________________________

2Fe(s)+3CO2(g) ΔH=-a kJ/mol
2Fe3O4(s)+CO2(g) ΔH=-b kJ/mol
3FeO(s)+CO2(g) ΔH=+ckJ/mol
Fe(s)+CO2(g) ΔH=-________。








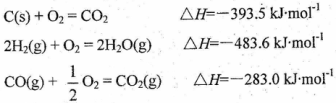
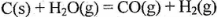 的焓变为
的焓变为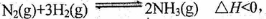 其化学平衡常数K与t的关系如下表:
其化学平衡常数K与t的关系如下表:



