-
肼(N2H4)是一种重要的液态火箭燃料,具有强还原性,工业上利用尿素[CO(NH2)2]、NaClO在NaOH 溶液中发生反应生成水合肼(N2H4·H2O)、Na2CO3等物质。
(1)下列物质的摩尔质量与肼的摩尔质量相同的是______(填字母)。
A.氧气 B.硫化氢 C.硅化氢 D.氟气
(2)上述生成水合肼的反应中尿素作_____(填“氧化剂”或“还原剂”),上述反应的化学方程式为_________________。
(3)发射“神舟飞船的长征火箭用肼作燃料,以二氧化氮作氧化剂,两者反应会生成氮气和水。该反应中每生成6.72 L(标准状况)N2,转移电子的物质的量为________。
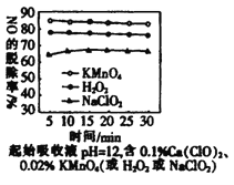
(4)肼燃烧易产生NO,可用漂白粉溶液脱除NO。为提高NO的脱除率,在其他条件相同时,向漂白粉溶液中分别加入三种不同添加剂,测得其对NO脱除率的影响如图所示。由图可知,KMnO4、H2O2、NaClO2 的氧化性由弱到强的顺序是_______________。
-
资源化利用二氧化碳不仅可减少温室气体的排放,还可重新获得燃料或重要工业产品。
(1)以CO2与NH3为原料可合成化肥尿素[CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H =-159.47 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H =+116.49 kJ·mol-1
③H2O(l)=H2O(g)△H =+88.0 kJ·mol-1
试写出NH3和CO2合成尿素和液态水的热化学方程式______________。
(2)已知:
| 化学键 | Si—Cl | H—H | H—Cl | Si—Si |
| 键能/kJ·mol-1 | 360 | 436 | 431 | 176 |
且硅晶体中每个硅原子和其他4个硅原子形成4个共价键。工业上所用的高纯硅可通过下列应反制取:SiCl4(g)+2H2(g) Si(s)+4HCl(g),该反应的△H=___ kJ·mol-1。
Si(s)+4HCl(g),该反应的△H=___ kJ·mol-1。
(3)在一定条件下,二氧化碳转化为甲烷的反应如下:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH<0向一容积为2L的恒容密闭容器中充入一定量的CO2和H2,在300℃时发生上述反应,达到平衡时各物质的浓度分别为CO2:0.2mol·L-1,H2:0.8mol·L-1,CH4:0.8mol·L-1,H2O:1.6mol·L-1,起始充入CO2和H2的物质的量分别为_____、_____,CO2的平衡转化率为______。
CH4(g)+2H2O(g) ΔH<0向一容积为2L的恒容密闭容器中充入一定量的CO2和H2,在300℃时发生上述反应,达到平衡时各物质的浓度分别为CO2:0.2mol·L-1,H2:0.8mol·L-1,CH4:0.8mol·L-1,H2O:1.6mol·L-1,起始充入CO2和H2的物质的量分别为_____、_____,CO2的平衡转化率为______。
(4)观察如图所示的两个装置,图1装置中铜电极上产生大量的无色气泡,图2装置中铜电极上无气体产生,而铬电极上产生大量的有色气体。根据上述现象试推测金属铬具有的两种重要化学性质为
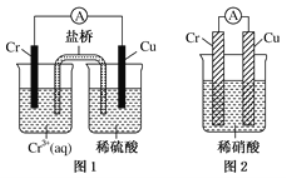
① ____________________________________。
② ____________________________________。
-
肼(N2H4)作为火箭发动机的燃料,可通过反应NaClO + 2NH3 = N2H4 + NaCl + H2O制取。某化学兴趣小组尝试在实验室制取N2H4,设计了如下实验:
(1)制备NaClO溶液,装置如图所示。(已知:3Cl2 + 6NaOH 5NaCl + NaClO3 + 3H2O)
5NaCl + NaClO3 + 3H2O)
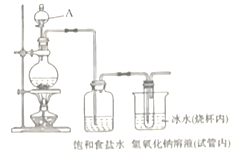
①仪器A的名称是________________。
②连接好装置,装药品之前,必须进行的一项操作是_________。
③圆底烧瓶内发生反应的化学方程式为_______________;当生成71g氯气时,被氧化的HCl为_________mol。试管内发生反应的离子方程式为_________。
④饱和食盐水的作用是_____________,冰水的作用是____________。
(2)将NaClO溶液倒入烧杯中,持续通入NH3制取N2H4。制取氨气的化学方程式为_______。
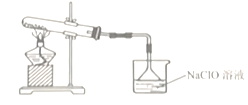
(3)火箭发射时用N2H4作燃料,用N2O4助燃,燃烧生成两种可参与大气循环的物质。写出该反应的化学方程式______________。
-
NaClO2是一种重要的杀菌消毒剂,工业上制备NaClO2的原理为ClO2+H2O2+NaOH→NaClO2+H2O+O2(未配平)。下列说法错误的是
A.该制备反应中,H2O2是还原剂
B.氧化剂与还原剂的物质的量之比为2:1
C.生成标准状况下的11.2L气体,转移2mol电子
D.制备过程中,混合液的碱性将减弱
-
肼(N2H4)具有强还原性,可用作火箭燃料、抗氧剂等。
(1)肼可以由氨气反应制得,已知部分化学键键能如下表所示:
| 化学键 | H-H | N≡N | N-H |
| 键能/kJ·mol-1 | a | b | c |
工业上合成氨的反应 N2(g)+3H2(g) ⇌ 2NH3(g) ΔH=_____kJ·mol-1.
(2)肼—空气燃料电池是一种环保型燃料电池,结构如图 1 所示
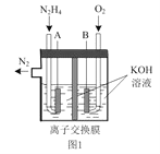
①肼—空气燃料电池的负极反应式为_____
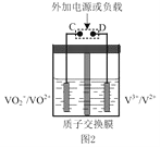
②全钒液流可充电电池结构如图 2 所示,将肼—空气燃料电池的 A 极与全钒液流可充电电池的 C 极相连,B 极与 D 极相连,写出阴极的电极反应____
(3)肼可用于处理高压锅炉水中的氧,防止锅炉被腐蚀,与使用 Na2SO3 处理水中溶解的 O2 相比,肼的优点是_____
-
氯气及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)NaClO有较强的氧化性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式_________________________。
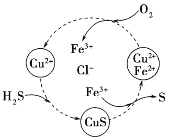
(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应可以回收S,其物质转化如图所示。该图示的总反应为_________________________。
(3)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出在碱性条件下用Al粉还原NO3-,产物是N2。发生的反应可表示如下,请完成方程式的配平。
___Al+___NO3-+___ =___AlO2-+___N2↑+___H2O
-
为了保护环境,充分利用资源,可将工业废弃物转变成重要的化工原料。回答下列问题:
(1)可用NaClO3氧化酸性FeCl2废液得到FeCl3,FeCl3具有净水作用,但腐蚀设备。
①写出NaClO3氧化酸性FeCl2的离子方程式:__________________________。
②若酸性FeCl2废液中:c(Fe2+)=2.0×10-2 mol∕L,c(Fe3+)=1.0×10-3 mol∕L,c(Cl-)=5.3×10-2 mol∕L,则该溶液的c(H+)约为_________。
③与明矾净水原理相似,FeCl3净水的原理是:________________(用恰当文字回答)
(2)可用废铁屑为原料,按下图的工艺流程制备聚合硫酸铁(PFS),PFS是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。
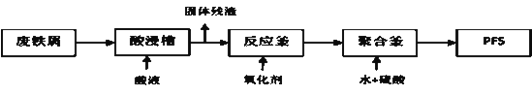
①酸浸时最合适的酸是______________。
②反应釜中加入的氧化剂,下列试剂中最合适的是____________(填标号)。
a.HNO3 b.KMnO4 c.Cl2 d.H2O2
③检验其中Fe2+是否完全被氧化,可选择__________(填标号)。
a.KMnO4溶液 b.Na2SO3溶液 c.KSCN溶液
-
(Ⅰ)开发新型替代燃料成为各国关注的重要科研项目,中国现已成为世界第三大利用植物秸秆(主要成分纤维素)生产燃料乙醇的国家.已知在25℃条件下,2.3g乙醇完全燃烧生成CO2和液态H2O时放出68.34kJ的热量,写出乙醇燃烧的热化学方程式:______.
(Ⅱ)乙醇的催化氧化反应在有机合成工业有着广泛的用途.某同学用如图所示的方法进行乙醇的催化氧化实验:向试管中加入3-4mL无水乙醇,浸入50℃左右的热水中,将铜丝烧热,迅速插入乙醇中,反复多次.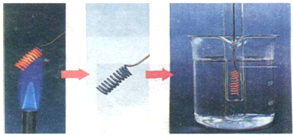
(1)在上述实验过程中,铜丝绕成螺旋状的作用是______.
(2)铜丝的颜色先后发生的变化是______;请写出相应的两个化学方程式______ 2CuO
-
Na2S2O3是重要的化工原料,用途很广,其还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,主要用于治疗氰化物中毒。工业上可利用反应Na2CO3+2Na2S+4SO2===3Na2S2O3+CO2制取Na2S2O3,下列说法正确的是( )
A.Na2S2O3只有还原性
B.氧化产物与还原产物的物质的量之比为1∶2
C.每生成1 mol Na2S2O3,转移4×6.02×1023个电子
D.每吸收4 mol SO2就会放出22.4 L CO2
-
尿素[CO(NH2)2]是一种高效的肥料。在土壤中,尿素发生水角时缓慢释放出的氨气和二氧化碳都能被作物质吸收利用[CO(NH2)2+H2O===CO2+2NH3]。试回答:
⑴尿素中碳、氧、氮、氢元素的质量比为。
⑵120g尿素完全水解,可产生二氧化碳的质量为g,氨气的质量为g。








