-
三氧化二猛(Mn2O3)在现代工业上应用广泛。以软锰矿(主要成分为MnO2)和硫锰矿(主要成分为MnS)为原料制备高纯度硫酸锰进而制备三氧化二锰的工艺流程如下(两种矿物中均不存在单质杂质):
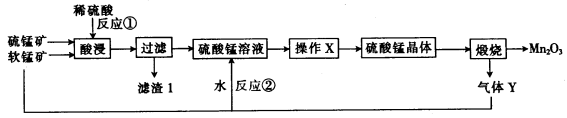
(1)滤渣1中存在一种非金属单质,则“酸浸”时反应①的化学方程式为___________。
(2)操作X为蒸发浓缩、_____________、洗涤烘干。经操作X之后得到MnSO4 • H2O。在洗涤操作中,常用酒精洗涤MnSO4 • H2O晶体,主要目的是_________________。
(3) 气体Y直接排放会污染空气,将Y的水溶液与软锰矿反应可得硫酸锰,反应②的化学方程式为____________。
(4) Mn2O3与MnO2类似,也能与浓盐酸反应,其反应的离子方程式为___________。
(5)用标准的BaCl2溶液测定样品中MnSO4 • H2O的质量分数时,发现样品纯度大于100%(测定过程中产生的误差可忽略),其原因可能是__________(任写一点)。
-
三氧化二锰(Mn2O3)在现代工业上应用广泛,在锂离子电池的制备中有重要的作用。用软锰矿(主要成分为MnO2)和硫锰矿(主要成分为MnS)制备高纯度Mn2O3的工艺流程如图所示。
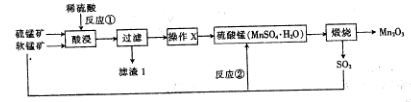
(1)反应①中会生成一种非金属单质,则该非金属单质是_________________,该反应的还原剂是________________。(填化学式)
(2)操作X为蒸发浓缩、__________、过滤、洗涤烘干。在洗涤操作中,常用酒精洗涤MnSO4·H2O晶体,主要目的是________________;
(3)Mn2O3与MnO2类似,加热时也能与浓盐酸反应放出Cl2,该反应的离子方程式为_____________;
-
三氧化二锰(Mn2O3)在现代工业上位用广泛,在锂离子电池的制备中有重要的作用。 用软锰矿 (主要成分为MnO2)和硫锰矿(主要成分为MnS)制备高纯度Mn2O3的工艺流程如图所示。
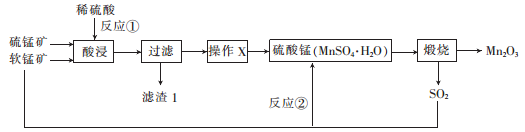
(1) 反应①中会生成一种非金属单质,则该非金属单质是___________,该反应的还原剂是__________。(填化学式)
(2) 操作X为蒸发浓缩、_____________、过滤、洗涤烘干。在洗涤操作中,常用酒精洗涤MnSO4 •H2O晶体,主要目的是______________。
(3) Mn2O3与MnO2类似,加热时也能与浓盐酸反应放出Cl2,该反应的离子方程式为__________。
-
MnO2是一种重要的化工原料,可用于合成工业的催化剂和氧化剂。采用软锰矿(主要成分为MnO2)可制备高纯MnO2,其流程如下:

下列叙述错误的是
A. “含Mn2+、A13+的溶液”中还含Fe3+
B. 加入“氨水”同时搅拌,搅拌的目的是提高反应速率
C. “滤渣”可完全溶解在NaOH溶液中
D. 电解含Mn2+的溶液,MnO2为阳极产物
-
高锰酸钾是常用的氧化剂。工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体。中间产物为锰酸钾。下图是实验室模拟制备KMnO4晶体的操作流程:
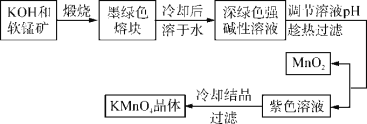
已知:锰酸钾(K2MnO4)是墨绿色晶体,其水溶液呈深绿色,这是锰酸根离子(MnO )在水溶液中的特征颜色,在强碱性溶液中能稳定存在;在酸性、中性和弱碱性环境下,MnO
)在水溶液中的特征颜色,在强碱性溶液中能稳定存在;在酸性、中性和弱碱性环境下,MnO 会发生自身氧化还原反应,生成MnO
会发生自身氧化还原反应,生成MnO 和MnO2。
和MnO2。
回答下列问题:
(1)KOH的电子式为____________。
(2)调节溶液pH过程中,所得氧化产物与还原产物的物质的量之比为____________。
(3)趁热过滤的目的是_____________________________________________。
(4)已知20 ℃时K2SO4、KCl、CH3COOK的溶解度分别为11.1 g、34 g、217 g,则从理论上分析,选用下列酸中________(填标号),得到的高锰酸钾晶体纯度更高。
A.稀硫酸 B.浓盐酸 C.醋酸 D.稀盐酸
(5)产品中KMnO4的定量
①配制浓度为0.1250 mg· mL-1的KMnO4标准溶液100 mL。
②将上述溶液稀释为浓度分别为2.5、5.0、7.5、10.0、12.5、15.0(单位:mg·L-1)的溶液,分别测定不同浓度溶液对光的吸收程度,并将测定结果绘制成曲线如下。
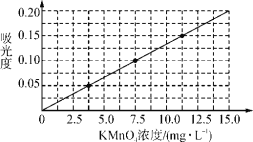
③称取KMnO4样品(不含K2MnO4)0.1250 g按步骤①配得产品溶液1000 mL,取10 mL稀释至100 mL,然后按步骤②的方法进行测定,两次测定所得的吸光度分别为0.149、0.151,则样品中KMnO4的质量分数为________。
(6)酸性KMnO4溶液与FeSO4溶液反应的离子方程式为____________________。
-
Ⅰ.高锰酸钾是锰的重要化合物和常用氧化剂,在实验室和医疗上有非常广泛的应用。如图1是工业上用软锰矿(主要含MnO2)制备高锰酸钾晶体的一种工艺流程:
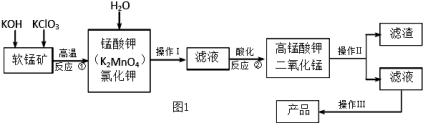
(1)第①步加热熔融应在铁坩埚中进行,而不用瓷坩埚的原因是(用化学方程式表示)。写出反应①的离子方程式;
(2)反应②的产物中,氧化产物与还原产物的物质的量的比是
(3)反应②中“酸化”时应选择下列酸中的(填序号)
a.稀盐酸b.稀硫酸c.亚硫酸
(4)操作Ⅱ的名称是,实验室进行该操作需用到的玻璃仪器有
Ⅱ.某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质
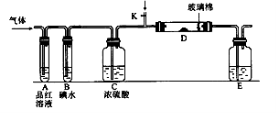
(5)若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?(填“相同”或“不相同”)。
(6)若装置B中装有5.0mL1.0mol/L的碘水,当通入足量C l2完全反应后,共转移了5.0×10-2mol电子,该反应的化学方程式为;
l2完全反应后,共转移了5.0×10-2mol电子,该反应的化学方程式为;
(7)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4∶3。当Cl2与含X的溶液完全反应后,有浅黄色沉淀产生,取少量上层清加入盐酸酸化的氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式。
-
高锰酸钾是锰的重要化合物和常用氧化剂,在实验室和医疗上有非常广泛的应用。以下是工业上用软锰矿(主要含MnO2)制备高锰酸钾晶体的一种工艺流程:
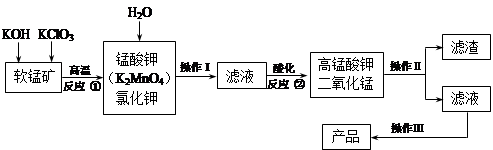
(1)操作Ⅱ的名称是_______,实验室进行该操作须用到的玻璃仪器有 ;
(2)反应②的产物中,氧化产物与还原产物的物质的 量之比是______;
(3)反应②中“酸化”时不能选择下列酸中的______(填字母序号)
a.稀盐酸 b.稀硫酸 c.稀醋酸
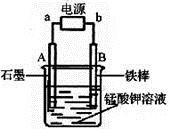
(4)电解锰酸钾溶液也可以制备高锰酸钾,其阴极反应式为:2H2O + 2e-= 2OH-+ H2↑,如图,b为电源的_______极,电解池的阳极反应式是_______;若电解过程中收集到2.24 L H2(标准状况),则得到高锰酸钾______g。(提示:阴离子放电顺序MnO42->OH-)
-
KMnO4在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
Ⅰ.将软锰矿(主要成分MnO2)粉碎后,与KOH固体混合,通入空气充分焙烧,生成暗绿色熔融态物质。
Ⅱ.冷却,将固体研细,用稀KOH溶液浸取,过滤,得暗绿色溶液。
Ⅲ.向暗绿色溶液中通入CO2,溶液变为紫红色,同时生成黑色固体。
Ⅳ.过滤,将紫红色溶液蒸发浓缩,冷却结晶,过滤,洗涤,干燥,得KMnO4固体。
资料:K2MnO4为暗绿色固体,在强碱性溶液中稳定,在近中性或酸性溶液中易发生歧化反应(Mn的化合价既升高又降低)。
(1)Ⅰ中,粉碎软锰矿的目的是___________________。
(2)Ⅰ中,生成K2MnO4的化学方程式是______________________________。
(3)Ⅱ中,浸取时用稀KOH溶液的原因是_________________。
(4)Ⅲ中,CO2和K2MnO4在溶液中反应的化学方程式是_____________________。
(5)将K2MnO4溶液采用惰性电极隔膜法电解,也可制得KMnO4,装置如图:
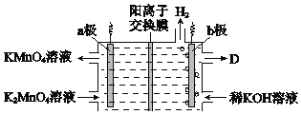
①b极是______极(填“阳”或“阴”),D是_______________。
②结合电极反应式简述生成KMnO4的原理:_______________________________。
③传统无膜法电解时,锰元素利用率偏低,与之相比,用阳离子交换膜可以提高锰元素的利用率,其原因是______。
(6)用滴定法测定某高锰酸钾产品的纯度,步骤如下:
已知:Na2C2O4 +H2SO4 =H2C2O4 +Na2SO4,5H2C2O4 +2MnO4-+6H+=2Mn2++10CO2↑+8H2O,摩尔质量:Na2C2O4 134g•mol-1、KMnO4 158g•mol-1。
ⅰ.称取ag产品,配成50mL溶液。
ⅱ.称取bgNa2C2O4,置于锥形瓶中,加蒸馏水使其溶解,再加入过量的硫酸。
ⅲ.将锥形瓶中溶液加热到75℃~80℃,恒温,用ⅰ中所配溶液滴定至终点,消耗溶液VmL(杂质不参与反应)。
滴定终点的现象为_______________,产品中KMnO4的质量分数的表达式为_____________。
-
软锰矿的主要成分是MnO2,还含有少量金属铁、镁、铝、锌、铜的化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上用软锰矿制备碳酸锰并回收硫酸铵,其主要流程如下:
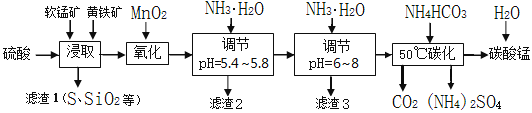
已知金属离子从开始形成氢氧化物沉淀,到沉淀时溶液的pH如下表:
| 金属离子 | Fe2+ | Fe3+ | Al3+ | Cu2+ | Mn2+ |
| 开始沉淀pH | 7.5 | 2.7 | 4.1 | 5.9 | 8.8 |
| 完全沉淀pH | 9.5 | 3.7 | 5.4 | 6.9 | 10.8 |
(1)提高浸出率的可采取的措施有_________。
A.适当升高温度 B.搅拌 C.加适量纯碱 D.加压
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,则浸取时发生的主要反应的化学方程式是____________________________________________。
(3)调节pH为5.4~5.8的目的是_____________________________________________。
(4)滤渣3的主要成分的化学式是_____________。
(5)50℃碳化过程发生反应的离子方程式是____________________________________。
-
(共7分)KMnO4是一种用途广泛的氧化剂,可由软锰矿(主要成分为MnO2)通过下列方法制备:①软锰矿与过量KOH、KClO3固体熔融生成K2MnO4;②溶解、过滤后将滤液酸化,使K2MnO4完全转化为MnO2和KMnO4;③滤去MnO2,将滤液浓缩、结晶得到深紫色的KMnO4产品。
(1)溶液酸化时,K2MnO4转变为MnO2和KMnO4的离子方程式是
;
(2)测定KMnO4产品的纯度可用标准Na2S2O3溶液进行滴定。
①配制250 mL0.1 mol/L标准Na2S2O3溶液,需准确称取Na2S2O3固体的质量为 g;
②取上述制得的KMnO4产品0.6000g,酸化后用0.1mol/L标准Na2S2O3溶液进行滴定,滴定至终点消耗Na2S2O3溶液20.00 ml。计算该KMnO4产品的纯度(请给出计算过程)。
 (有关离子方程式为:MnO4-+S2O32-+H+ SO42-+Mn2++H2O 未配平)
(有关离子方程式为:MnO4-+S2O32-+H+ SO42-+Mn2++H2O 未配平)











