-
附加题:(共10分)铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层,则 PbO2的酸性比CO2的酸性 (填“强”或“弱”)。
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为 。
(3)瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:
①2PbS(s)+3O2(g)=2PbO(s)+2SO2(g) △H= a kJ·mol-1
②PbS(s)+2PbO(s)=3Pb(s)+SO2(g) △H= b kJ·mol-1
③PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g) △H= c kJ·mol-1
反应3PbS(s)+ 6O2(g)=3PbSO4(s) ΔH= kJ ·mol-1(用含a,b ,c的代数式表示)。
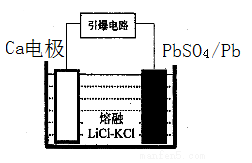
(4)引爆导弹、核武器的工作电源通常Ca/PbSO4热电池,其装置如图所示,该电池正极的电极反应式为 。
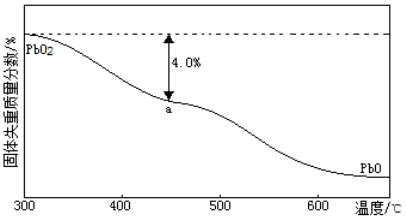
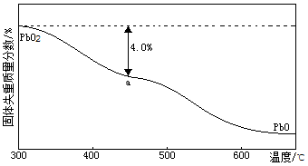
(5)PbO2在加热过程发生分解的失重曲线如下图所示,已知失重曲线上的a点为样品失重4.0%( )的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,则计算x= _和m:n=_ _。
)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,则计算x= _和m:n=_ _。
-
(1)地下钢管连接镁块是金属防腐措施中的________________________法。
(2)铅及其化合物可用于蓄电池,耐酸设备及X射线防护材料等。回答下列问题:
①铅是碳的同族元素,比碳多4个电子层。铅在元素周期表的位置为_______________________;铅的最高价氧化物对应水化物的酸性比碳酸的_______(填“强”或“弱”)。
②PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为___________________________。
③铅蓄电池放电时的正极反应式为__________________________________________ ,当电路中有2mol电子转移时,理论上两电极质量变化的差为_______ g。
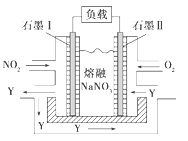
(3)NO2、O2和熔融NaNO3可制作燃料电池,其原理见下图,石墨Ⅰ为电池的________极;该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为__________________。
-
铅及其化合物可用于蓄电池、耐酸设备及X射线防护等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层,铅在周期表的位置为______周期第_____族。
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为_________________________
(3)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为_________________:铅蓄电池的两极分别为Pb、PbO2,电解质溶液为硫酸,放电时的反应为Pb+ PbO2+2H2SO4=2PbSO4+2H2O。写出负极发生的电极反应式为__________, 当电子转移2mol时正极增重________克。
-
铅及其化合物可用于蓄电池,耐酸设备及X射线防护材料等。回答下列问题:
(1)PbO2的酸性比CO2的酸性________(填“强”或“弱”)。
(2)Sn和Pb位于同一主族,同条件下Pb与同浓度稀盐酸却比Sn慢,猜测理由__________。
(3)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为_________________。
(4)铅蓄电池是最常兄的二次电池,其构造示意图如下。
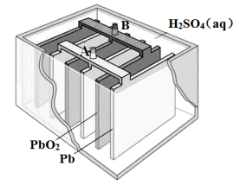
放电时的化学方程式为:Pb(s) + PbO2(s) + 2H2SO4(aq) = 2PbSO4(s) + 2H2O(1)
正极反应式是____________________,一段时间后,负极增重48克,转移电子_______mol。
(5) PbO2在加热过程发生分解的失重曲线如下图所示,己知失重曲线上的a点为样品失重4.0%(即 )的残留固体,若a点固体表示为PbOx或mPbO2·nPbO,列式计算x____值和m:n值__________。
)的残留固体,若a点固体表示为PbOx或mPbO2·nPbO,列式计算x____值和m:n值__________。
-
已知铅元素有+2价、+4价两种常用价态,铅及其化合物可用于耐酸设备及X射线防护等。
(1)我国古代炼丹中经常使用到红丹(用X表示),在一定条件下,与过量硝酸能发生非氧化还原反应:X+4HNO3===PbO2+2Pb(NO3)2+2H2O(已配平)。
①PbO2中铅元素的化合价是________,PbO2不是碱性氧化物,判断的依据是_________________________________________________。
②X的化学式是________。
(2)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为____________________________________________。
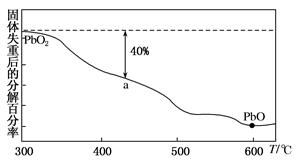
(3)PbO2在加热的过程中发生分解生成PbO和O2,其失重曲线如图所示,已知失重曲线上的a点为样品分解40%的残留固体。若a点固体组成表示为PbOx,则x=________。
-
含A元素的一种单质是一种重要的半导体材料,含A元素的一种化合物C可用于制造高性能的现代通讯材料—光导纤维,C与烧碱反应生成含A元素的化合物D。
(1)在元素周期表中,A位于第____族,与A同族但相对原子质量比A小的元素B的原子结构示意图为____________,A与B在原子的电子层结构上的相同点是______。
(2)易与C发生化学反应的酸是__________,反应的化学方程式是_____________。
(3)将C与纯碱混合高温熔融时发生化学反应生成D,同时还生成B的最高价氧化物E;将少量的E通入D的水溶液中,生成含A的化合物F。
①分别写出生成D和F的化学反应方程式:_______________,_________________。
②要将纯碱高温熔化,下列坩埚中不可选用的是_________
A.普通玻璃坩埚  石英玻璃坩埚
石英玻璃坩埚  铁坩埚
铁坩埚
-
五种短周期元素A、B、C、D、E、F的原子序数依次增大,A和C同族,B和D 同族,C离子和B离子具有相同的电子层结构。A和B、D、E、F均能形成共价化合物。A和B形成的化合物在水中呈碱性。回答下列问题:
(1)五种元素中,原子半径最大的元素在周期表中的位置:__________________,非金属性最强的元素其原子结构示意图为:__________________________;
(2)能说明E、F非金属性强弱的事实是___________________(用一个化学方程式举例);
(3)用电子式表示C、E元素组成的化合物的形成过程:____________________________;
(4)由A和B、D、E、F所形成的共价化合物中,热稳定性最差的是_______(用化学式表示);
(5)D在不充足的F中燃烧,生成的主要产物的结构式为_________________________;
(6)A和F形成的化合物与A和B形成的化合物反应,产物的电子式为_________________,其中存在的化学键类型为___________________________;
(7)写出F的同主族短周期元素的单质与水反应的化学方程式___________________________。
-
砷(As)是第四周期第VA族的元素,能形成多种化合物。回答下列问题:
(1)同族元素的同类物质结构相似,AsH3的电子式为_______。
(2)已知H3AsO3溶于水后的电离方程式为As3++30H- H3AsO3
H3AsO3 3H++AsO33-。H3AsO3中砷的化合价为______;若分别向上述平衡体系中加人稀硫酸、NaOH 溶液,则生成的正盐的化学式分别为______、_____。
3H++AsO33-。H3AsO3中砷的化合价为______;若分别向上述平衡体系中加人稀硫酸、NaOH 溶液,则生成的正盐的化学式分别为______、_____。
(3)已知I2、AsO33-、I-、AsO43-之间存在如下转化:I2 + AsO33-+2OH- 2I-+AsO43-+H2O。为验证该反应具有可逆性,某同学将等物质的量浓度的碘水与Na3AsO3溶液按体积比为V1: V2的比例混合(另加入适量的碱)。当V1_____V2(填“>”或“<”) 时,只用_____就可以确定该反应具有可逆性。
2I-+AsO43-+H2O。为验证该反应具有可逆性,某同学将等物质的量浓度的碘水与Na3AsO3溶液按体积比为V1: V2的比例混合(另加入适量的碱)。当V1_____V2(填“>”或“<”) 时,只用_____就可以确定该反应具有可逆性。
(4)常温下,将浓度均为2a mol·L-1的KI、Na3AsO4 溶液等体积混合后,溶液存在如下可逆反应:2I-(aq)+AsO43-(aq)+H2O(1) I2(aq)+AsO33-(aq)+2OH-(aq),通过调整溶液的pH(加适量碱)来控制反应进行的方向。下图是反应中c ( AsO33-)与时间t的关系图:
I2(aq)+AsO33-(aq)+2OH-(aq),通过调整溶液的pH(加适量碱)来控制反应进行的方向。下图是反应中c ( AsO33-)与时间t的关系图:
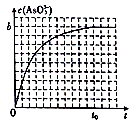
① 反应达到平衡后,向溶液中加人少量固体NaOH,则重新达到平衡后,溶液中AsO43-的转化率______(填“增大”、“减小”或 “不变”) , c(OH-)__________(填“增大”、“减小”或“不变”)。
② 若t0时刻,溶液的Ph=8,则该反应的平衡常数K=__________。
(5)若使2I-(aq)+AsO43-(aq)+H2O(1) I2(aq)+AsO33-(aq)+2OH-(aq)以原电池的方式进行,则正极的电极反应式为___________。
I2(aq)+AsO33-(aq)+2OH-(aq)以原电池的方式进行,则正极的电极反应式为___________。
-
目前我们手里把玩的许多新奇电子设备,都是由一些自然界含量稀少的稀有元素提供电能的。下列4种元素中,常用于手机电池的稀有金属元素是
A. 硫 B. 碲 C. 锂 D. 钠
-
目前我们手里把玩的许多新奇电子设备,都是由一些自然界含量稀少的稀有元素提供电能的。下列4种元素中,常用于手机电池的稀有金属元素是
A.硫 B.碲 C.锂 D.钠

 )的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,则计算x= _和m:n=_ _。
)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,则计算x= _和m:n=_ _。




