-
用铜和硫酸铜、银和硝酸银溶液设计一个原电池,电池的总反应的离子方程式是________
负极反应式是________;
正极反应式是:________.高二化学填空题中等难度题查看答案及解析
-
(6分)用铜和硫酸铜、银和硝酸银溶液设计一个原电池,电池的总反应的离子方程式是________
负极反应式是________;
正极反应式是:________
高二化学填空题简单题查看答案及解析
-
用铜、银和硝酸银溶液设计一个原电池,下列对该原电池的判断正确的是
A.铜作负极被氧化 B.银为正极被还原
C.正极反应为:Ag+ + e-=Ag D.NO3-向正极移动
高二化学选择题简单题查看答案及解析
-
如图所示,某同学设计一个燃料电池并探究氯碱工业原理和电解CuSO4溶液,其中乙装置中X为阳离子交换膜。
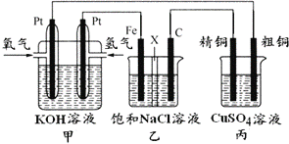
根据要求回答相关问题:
(1)通入氧气的电极为___(填“正极”或“负极”),负极的电极反应式为___。
(2)铁电极为___(填“阳极”或“阴极”),石墨电极(C)的电极反应式为___。
(3)乙装置中电解的总反应的离子方程式为___。
(4)若在标准状况下,有1.12L氧气参加反应,丙装置中阴极增重的质量为___。
高二化学综合题中等难度题查看答案及解析
-
下面能够构成原电池及电极反应式正确的是
A.Fe、Cu、浓硝酸溶液,负极反应式为:Fe-2e-==Fe2+
B.Al、Cu、稀硫酸,负极反应式为:Cu-2e-==Cu2+
C.Al、Mg、NaOH溶液,负极反应式为:Al+4OH--3e-==AlO2-+2H2O
D.Zn、Cu、乙醇,负极反应式为:Zn-2e-==Zn2+
高二化学选择题中等难度题查看答案及解析
-
某原电池总反应离子方程式为2Fe3++Fe=3Fe2+,能实现该反应的原电池是( )
A. 正极为铜,负极为铁,电解质溶液为氯化铁溶液
B. 正极为铜,负极为铁,电解质溶液为硝酸亚铁溶液
C. 正极为铁,负极为锌,电解质溶液为硫酸铁溶液
D. 正极为银,负极为铁,电解质溶液为硫酸铜溶液
高二化学选择题中等难度题查看答案及解析
-
某电池总反应的离子方程式为:2Fe3++Fe=3Fe2+,不能实现该反应的原电池是
A.正极为铜,负极为铁,电解液为氯化铁溶液
B.正极为石墨,负极为铁,电解液为硝酸铁溶液
C.正极为银,负极为铁,电解液为硫酸铁溶液
D.正极为铁,负极为锌,电解液为硫酸铁溶液
高二化学选择题中等难度题查看答案及解析
-
可以将氧化还原反应2H2+O2
2H2O设计成原电池。
(1)利用氢气和氧气、氢氧化钾溶液构成燃料电池,则负极通的气体应是 ,正极通的气体就是 ,电极反应为:正极 ,负极 。
(2)如果把KOH改为稀硫酸作电解质,则电极反应为:正极: ,负极: 。
(3)(1)和(2)的电解质溶液不同,反应进行后,其溶液的pH各有何变化? 。
(4)如把H2改为甲烷,KOH溶液作电解质溶液,则电极反应为:正极: ,负极: 。
高二化学填空题中等难度题查看答案及解析
-
按要求填空:
(1)将过量的氨水加入氯化铝溶液的离子方程式_____;
(2)浓硝酸久置后会略显黄色,可用方程式表示为_____;
(3)用KOH作电解质溶液,氢氧燃料电池负极反应式为_____;
(4)用方程式表示氯化铵溶液呈酸性原因_____。
高二化学填空题简单题查看答案及解析
-
下列说法正确的是 ( )
A.所有化学反应都能设计成原电池
B.原电池工作时,溶液中阳离子向负极移动,盐桥中阳离子向正极移动
C.在原电池中,负极材料活泼性一定比正极材料强
D.原电池放电时,电流方向由正极沿导线流向负极
高二化学单选题简单题查看答案及解析