-
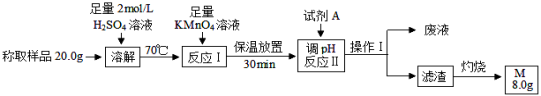
(14分)某化学小组拟利用下列流程测定某草酸亚铁样品(含有少量草酸,不含结晶水和其他杂质)中FeC2O4的含量。
已知几种氢氧化物开始沉淀和完全沉淀的pH如下表所示
| Fe2+ | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
试回答下列问题:
(1)用2 mol/L H2SO4溶液溶解草酸亚铁样品而不用蒸馏水直接溶解的原因是 ,加热至70℃左右,立即用KMnO4溶液滴定至终点。发生反应的离子方程式为2MnO4- + 5H2C2O4 +6H+ =2Mn2+ + 10CO2↑+ 8H2O和 。
(2)保温放置30min的目的是 。
(3)证明反应Ⅰ完全的实验操作或现象为 。
(4)已知常温下Fe(OH)3的Ksp=1.1×10-36,废液中c(Fe3+)= mol·L-1。
(5)灼烧充分的标志是 。
(6)样品中FeC2O4的含量为 。
-
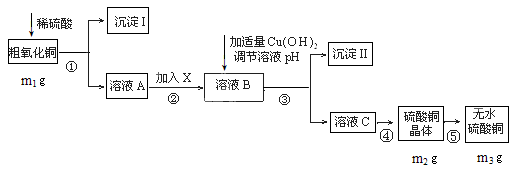
(12分)某粗氧化铜样品中含少量氧化亚铁及不溶于酸的杂质,某化学兴趣小组利用该样品制取胆矾晶体,测定胆矾晶体中结晶水的含量,并计算样品中氧化铜的含量,设计了如下方案进行实验。
查阅资料知Fe3+、Cu2+、Fe2+在水溶液中形成氢氧化物沉淀的pH范围如下:
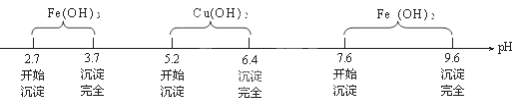
请回答下列问题:
(1)在整个实验过程中,下列仪器中不可能用到的是__________(填编号)。
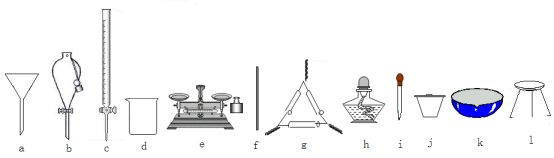
(2)物质X应选用_________(填字母)。
a.氢氧化钠 b.双氧水 c.铁粉 d.高锰酸钾
(3)为保证沉淀Ⅱ沉淀完全,操作③中溶液pH的调节范围为 。
(4)操作④的步骤有 、冷却结晶、 、自然干燥。
(5)在测定所得胆矾(CuSO4·xH2O)中结晶水x值的实验过程中:称量操作至少进行__ 次若测定结果x值偏大,可能的原因是_______________。
a.加热温度过高
b.胆矾晶体的颗粒较大
c.加热后放在空气中冷却
d.加热胆矾晶体时有晶体从坩埚中溅出
(6)该小组一位同学根据实验结果求出样品中CuO的质量分数为 ,另一位同学不同意,其原因是 。
,另一位同学不同意,其原因是 。
-
某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。
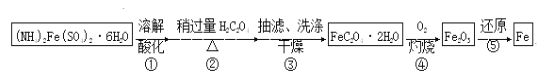
已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;H2C2O4易溶于水,溶解度随温度升高而增大。
请回答:
(1)下列操作或描述正确的是________。
A.步骤②,H2C2O4稍过量主要是为了抑制Fe2+水解
B.步骤③,采用热水洗涤可提高除杂效果
C.步骤③,母液中的溶质主要是(NH4)2SO4和H2C2O4
D.步骤③,如果在常压下快速干燥,温度可选择略高于100℃
(2)如图装置,经过一系列操作完成步骤③中的抽滤和洗涤。请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只需考虑一次):

开抽气泵→a→b→d→________→c→关抽气泵。
a.转移固液混合物;b.关活塞A;c.开活塞A;d.确认抽干;e.加洗涤剂洗涤
抽滤和普通过滤相比,优点是___________________________________________。
(3) 称取一定量的FeC2O4·2H2O试样,用硫酸溶解,
采用KMnO4滴定法测定,折算结果如下:
| n(Fe2+)/mol | n( )/mol )/mol | 试样中FeC2O4·2H2O的质量分数 |
| 9.80×10ˉ4 | 9.80×10ˉ4 | 0.980 |
由表中数据推测试样中最主要的杂质是____________________。
(4)实现步骤④必须用到的两种仪器是____________________
(供选仪器:a.烧杯;b.坩埚;c.蒸馏烧瓶;d.高温炉;e.表面皿;f.锥形瓶);
该步骤的化学方程式是______________________________________。
(5)为实现步骤⑤,不宜用碳粉还原Fe2O3,理由是________________________________。
-
某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。
已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;常温下H2C2O4为晶体,易溶于水,溶解度随温度升高而增大。

请回答:
(1)步骤②,发生反应的离子方程式____________________________;该步骤H2C2O4稍过量主要是为了_________________。
(2)下列操作或描述正确的是_______________。
A.步骤①,酸化主要是为了抑制Fe2+水解
B.步骤③,如果采用冷水洗涤可提高除杂效果
C.步骤③,如果在常压下快速干燥,温度可选择略高于100℃
(3)称取一定量的FeC2O4·2H2O试样,用硫酸溶解,采用KMnO4滴定法测定,折算结果如下:
| n(Fe2+)/mol | n(C2O42-)·mol-1 | 试样中FeC2O4·2H2O的质量分数 |
| 9.80×10-4 | 9.80×10-4 | 0.98 |
由表中数据推测试样中最主要的杂质是_________________。
(4)实现步骤④必须用到的两种仪器是_________(供选仪器如下)
a.坩埚;b.烧杯;c.蒸馏烧瓶;d.锥形瓶;e.表面皿:f.高温炉
该步骤的化学方程式是______________________________________________。
-
某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。
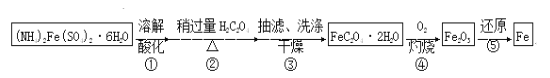
已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;H2C2O4易溶于水,溶解度随温度升高而增大。
请回答:
(1)下列操作或描述正确的是________。
A.步骤②,H2C2O4稍过量主要是为了抑制Fe2+水解
B.步骤③,采用热水洗涤可提高除杂效果
C.步骤③,母液中的溶质主要是(NH4)2SO4和H2C2O4
D.步骤③,如果在常压下快速干燥,温度可选择略高于100℃
(2)如图装置,经过一系列操作完成步骤③中的抽滤和洗涤。请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只需考虑一次):

开抽气泵→a→b→d→________→c→关抽气泵。
a.转移固液混合物;b.关活塞A;c.开活塞A;d.确认抽干;e.加洗涤剂洗涤
抽滤和普通过滤相比,优点是___________________________________________。
(3) 称取一定量的FeC2O4·2H2O试样,用硫酸溶解,
采用KMnO4滴定法测定,折算结果如下:
| n(Fe2+)/mol | n( )/mol )/mol | 试样中FeC2O4·2H2O的质量分数 |
| 9.80×10ˉ4 | 9.80×10ˉ4 | 0.980 |
由表中数据推测试样中最主要的杂质是____________________。
(4)实现步骤④必须用到的两种仪器是____________________
(供选仪器:a.烧杯;b.坩埚;c.蒸馏烧瓶;d.高温炉;e.表面皿;f.锥形瓶);
该步骤的化学方程式是______________________________________。
(5)为实现步骤⑤,不宜用碳粉还原Fe2O3,理由是________________________________。
-
某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。
已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;常温下H2C2O4为晶体,易溶于水,溶解度随温度升高而增大。

请回答:
(1)步骤②,发生反应的离子方程式____________________________;该步骤H2C2O4稍过量主要是为了_________________。
(2)下列操作或描述正确的是_______________。
A.步骤①,酸化主要是为了抑制Fe2+水解
B.步骤③,如果采用冷水洗涤可提高除杂效果
C.步骤③,如果在常压下快速干燥,温度可选择略高于100℃
(3)称取一定量的FeC2O4·2H2O试样,用硫酸溶解,采用KMnO4滴定法测定,折算结果如下:
| n(Fe2+)/mol | n(C2O42-)·mol-1 | 试样中FeC2O4·2H2O的质量分数 |
| 9.80×10-4 | 9.80×10-4 | 0.98 |
由表中数据推测试样中最主要的杂质是_________________。
(4)实现步骤④必须用到的两种仪器是_________(供选仪器如下)
a.坩埚;b.烧杯;c.蒸馏烧瓶;d.锥形瓶;e.表面皿:f.高温炉
该步骤的化学方程式是______________________________________________。
-
某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4·2H2O),进一步制备高纯度还原铁粉。
已知:FeC2O4·2H2O难溶于水,150℃开始失结晶水;常温下H2C2O4为晶体,易溶于水,溶解度随温度升高而增大。

请回答:
(1)步骤②,发生反应的离子方程式____________________________;该步骤H2C2O4稍过量主要是为了_________________。
(2)下列操作或描述正确的是_______________。
A.步骤①,酸化主要是为了抑制Fe2+水解
B.步骤③,如果采用冷水洗涤可提高除杂效果
C.步骤③,如果在常压下快速干燥,温度可选择略高于100℃
(3)称取一定量的FeC2O4·2H2O试样,用硫酸溶解,采用KMnO4滴定法测定,折算结果如下:
| n(Fe2+)/mol | n(C2O42-)·mol-1 | 试样中FeC2O4·2H2O的质量分数 |
| 9.80×10-4 | 9.80×10-4 | 0.98 |
由表中数据推测试样中最主要的杂质是_________________。
(4)实现步骤④必须用到的两种仪器是_________(供选仪器如下)
a.坩埚;b.烧杯;c.蒸馏烧瓶;d.锥形瓶;e.表面皿:f.高温炉
该步骤的化学方程式是______________________________________________。
-
(14分)
绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:______________、_______________。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。
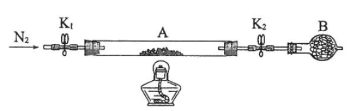
①仪器B的名称是____________________。
②将下列实验操作步骤正确排序___________________(填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
③根据实验记录,计算绿矾化学式中结晶水数目x=________________(列式表示)。若实验时按a、d次序操作,则使x__________(填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。
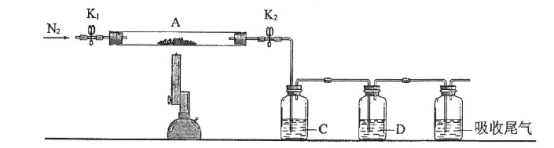
①C、D中的溶液依次为_________(填标号)。C、D中有气泡冒出,并可观察到的现象分别为_______________。
a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式_____________________。
-
为充分利用资源,变废为宝,实验室里利用废铁屑制取硫酸亚铁铵[(NH4)2Fe(SO4)2•6H2O]。某兴趣小组以废铁屑制得硫酸亚铁铵后,按下列流程制备二水合草酸亚铁(FeC2O4•2H2O),进一步制备高纯度还原铁粉。
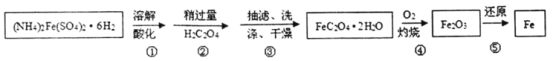
已知:FeC2O4•2H2O难溶于水,150℃开始失结晶水:H2C2O4易溶于水,溶解度随温度升高而增大。
请回答:
(1)步骤②中,H2C2O4稍过量主要原因是_________________。
(2)为了提高步骤③得到的FeC2O4•2H2O的纯度,宜用_________________(填热水、冷水或无水乙醇)洗涤,检验洗涤是否干净的操作是_________________。
(3)实现步骤④必须用到的两种仪器是_________________(供选仪器:a.烧杯;b. 坩埚;c.蒸馏烧瓶;d.高温炉;e.表面皿;f.锥形瓶):
(4)为实现步骤⑤,不宜用碳粉还原Fe2O3, 理由是_________________。
(5)硫酸亚铁铵是重要的工业原料,其溶解性如表所示:
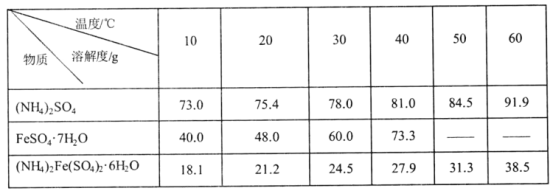
(注意:高于73.3℃,FeSO4•7H2O发生分解)
以铁屑(有油污)、硫酸、硫酸较为原料,补充制取硫酸亚铁铵晶体的实验方案:将铁屑置于锥形瓶中,_________________冷却,过滤,用蒸馏水洗涤铁屑至中性,将铁屑置于锥形瓶中,_________________至铁屑完全溶解,_________________,冷却结晶,用无水乙醇洗涤2-3次,低温干操。[实验中必须使用的试剂:铁屑、1.0mol•L-1的Na2CO3溶液、3.0mol•L-1的H2SO4溶液,饱和(NH4)2SO4溶液]
-
草酸亚铁晶体是一种淡黄色粉末,常用于照相显影剂及制药工业,也是电池材料的制备原料。某化学兴趣小组对草酸亚铁晶体的一些性质进行探究。
(1)甲组同学用图13所示装置测定草酸亚铁晶体(FeC2O4·xH2O)中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为ag。将样品装入石英玻璃管中,再次将装置称重,记为b g。按图连接好装置进行实验。
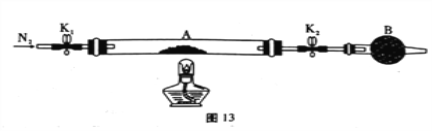
a.打开K1和K2,缓缓通入N2;
b.点燃酒精灯加热;
c.熄灭酒精灯;
d.冷却至室温;
e.关闭K1和K2;
f.称重A;
g.重复上述操作,直至A恒重,记为cg。
①仪器B的名称是____________________。
②根据实验记录,计算草酸亚铁晶体化学式中的x =____________(列式表示);若实验时a、b次序对调,会使x值______________ (填“偏大” “无影响”或“偏小”)。
(2)乙组同学为探究草酸亚铁的分解产物,将(1)中已恒重的装置A接入图14所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后装置A中残留固体为黑色粉末。
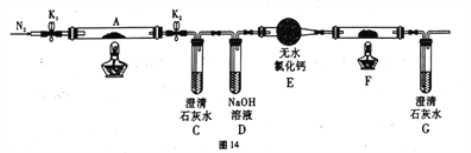
①装置C、G中的澄清石灰水均变浑浊,说明分解产物中有_______________(填化学式)。
②装置F中盛放的物质是:______________________ (填化学式)。
③将装置A中的残留固体溶于稀盐酸,无气泡,滴入KSCN溶液无血红色,说明分解产物中有:_________________ (填化学式)。
④写出草酸亚铁(FeC2O4)分解的化学方程式:______________________。
















