-
某主族元素的原子,M 层上有一个半充满的亚层(即该亚层的每个轨道只有1个电子),这种原子的质子数
A. 只能是7 B. 只能是15 C. 是11或15 D. 是11或13
高二化学单选题简单题查看答案及解析
-
某主族元素原子,M层上有一个能级的原子轨道半充满,该原子的质子数是
A.只能是7 B.只能是15 C.是11或15 D.是11或13
高二化学选择题中等难度题查看答案及解析
-
某主族元素的原子,M层上有一个半充满的电子层,这种原子的质子数是( )
A.只能是7
B.只能是15
C.是11或15
D.是11或13高二化学选择题中等难度题查看答案及解析
-
某主族元素原子,其M能层上有一个半充满的能级,该原子的质子数
A. 只能是11 B. 只能是24 C. 可能是29 D. 可能是11或15
高二化学选择题简单题查看答案及解析
-
某主族元素的原子,M层上有一个半充满的能级,这种原子的质子数是( )
A.只能是7 B.只能是15 C.是11或15 D.是11或13
高二化学单选题简单题查看答案及解析
-
(22分) A B C D E是前四周期元素,且原子序数依次增大。A的原子核中只有一个质子;B原子外围电子排布nS n nP n ;D原子核外有2个电子层,S轨道电子总数和P轨道电子总数相等 ;E 2+ 的M能层上各能级的电子数之比为1:3:3 请回答下列问题:
(1)E原子基态电子排布式________
(2)这五种元素中电负性最大的是________(填元素符号,下同)第一电离能最小的是________
(3)化合物EBC2中阴离子是BC22-,和BC2 2- 互为等电子体的分子有C2D和________,由此可知BC2 2- 的空间构型是________。
(4)由A C两元素形成一种10电子分子X,写出X的电子式________
X可与多种金属离子形成配合物。钴有两种化学式均为Co(X)5BrSO4的配合物,且配位数均为6,则它们分别溶于水时电离出的阳离子的化学式可能是________和________;
(5)A C两元素还能形成一种离子化合物,写出该化合物化学式 ________ ;你认为该化合物中除了离子键外还存在化学键是________;该化合物溶于水有气体产生,写出反应化学方程式________
高二化学填空题中等难度题查看答案及解析
-
有A、B、C、D、E五种元素。其相关信息如下:
元素
相关信息
A
A元素的一种原子没有中子,只有一个质子
B
B是电负性最大的元素
C
C的基态原子2p轨道有三个未成对电子
D
D为主族元素,且与E同周期,其最外层上有两个运动状态不同的电子
E
E能形成砖红色(红色)的E2O和EO两种氧化物
回答下列问题。
(1)写出E元素原子基态时M层的电子排布式 。
(2)C元素单质分子中含有δ和π键的键数之比为 。
(3)解释在水中的溶解度C7H15OH比乙醇低的原因是: 。
(4)A、C、E三种元素可形成:E(CA3)42+配离子,其中存在的化学键类型有 (填序号)。
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若 E(CA3)42+具有对称的空间构型.且当 E(CA3)42+中的两个CA3分子被两个Cl取代时.能得到两种不同结构的产物,则 E(CA3)42+的空间构型为 (填序号)。
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(5)三硫化四磷是黄绿色针状结晶,其结构如图所示。
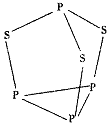
三硫化四磷分子中P原子采取____杂化,与PO3-互为等电子体的化合物分子的化学式为________。用NA表示阿伏加德罗常数的数值,0.1mol三硫化四磷分子中含有的孤电子对数为_________。
高二化学填空题简单题查看答案及解析
-
某主族元素原子,其M能层上有一个半充满的能级,该原子的质子数
A.只能是11 B.只能是24 C. 可能是29 D. 可能是11或15
高二化学选择题中等难度题查看答案及解析
-
某主族元素原子,其M能层上有一个半充满的能级,该原子的质子数 ( )
A.只能是11 B.可能是24 C. 可能是29 D. 可能是11或15
高二化学选择题简单题查看答案及解析
-
X是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y基态原子的3p轨道上有2个未成对电子。元素Z的原子最外层电子数是其内层的3倍。回答下列问题:
(1)单质X的晶体类型为____________,其中X原子的配位数为______________。
(2)已知元素Y可与元素Z的相对原子质量只差为16,则元素Y基态原子的外围电子排布图为_____________,其同周期元素中,第一电离能最大的是______(写元素符号)。元素Y的含氧酸中,酸性最强的是___________________(写化学式),该酸根离子的立体构型为_________________。
(3)Z的氢化物在乙醇中的溶解度大于Y的氢化物,其原因是______________________。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为______________________。
(5)X与Y形成的一种化合物的立方晶胞如图所示。该化合物的化学式为____________,已知此晶体的密度为ρg·cm–3,阿伏加德罗常数为NA,则此晶胞中X与Y的最近距离是______________cm。(写出计算式,不要求计算结果。)
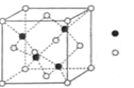
高二化学推断题困难题查看答案及解析