(1)写出实验时烧杯中观察到的一项现象______.
(2)充分反应后天平指针会______(填“偏左”、“偏右”、“不发生偏转”之一),理由是______.
(3)恰好完全反应时,计算所得溶液的质量.(计算结果保留到0.01g)
九年级化学解答题中等难度题

九年级化学解答题中等难度题
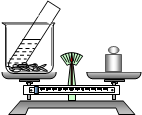
(6分)某兴趣小组为验证质量守恒定律,取5g铜锌混合物放入烧杯中,向试管内加入20g溶质质量分数为24.5%的稀硫酸,调节天平至平衡(如图所示),然后将稀硫酸倒入烧杯中(试管不取出),恰好完全反应,试根据要求回答下列问题:

⑴写出实验时烧杯中观察到的一项现象________ 。
⑵充分反应后天平指针会________(填“偏左”、“偏右”、“不发生偏转”之一),理由是________。
⑶恰好完全反应时,计算所得溶液的质量。(保留到0.01g)
九年级化学计算题中等难度题查看答案及解析

九年级化学解答题中等难度题查看答案及解析
(7分)某兴趣小组为了验证质量守恒定律,在烧杯中盛有20g溶质质量分数为20%的氢氧化钠溶液试管内装有20g硫酸铜溶液,如图所示,放于天平上称量,此时天平平衡。然后将试管内药品倒入烧杯内(试管不取出),恰好完全反应,试根据要求,回答下列问题:
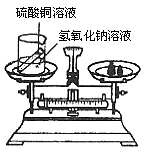
(1)写出实验过程中观察到的一项实验现象:________________________________________________。
(2)反应结束后,天平指针会__________ (填“偏左”“偏右”“不发生偏转”之一)。
(3)试计算恰好完全反应时所得不饱和溶液的质量。(精确到0.1g)
九年级化学计算题困难题查看答案及解析
(7分)某兴趣小组为了验证质量守恒定律,在烧杯中盛有20g溶质质量分数为20%的氢氧化钠溶液试管内装有20g硫酸铜溶液,如图所示,放于天平上称量,此时天平平衡。然后将试管内药品倒入烧杯内(试管不取出),恰好完全反应,
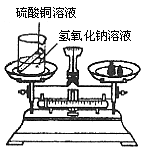
试根据要求,回答下列问题:
(1)写出实验过程中观察到的一项实验现象: ________________________________________________。
(2)反应结束后,天平指针会__________ (填“偏左”“偏右”“不发生偏转”之一)。
(3)试计算恰好完全反应时所得不饱和溶液的质量。(精确到0.1g)
九年级化学计算题困难题查看答案及解析
某同学为验证质量守恒定律,向烧杯中加入40克溶质质量分数为20%的硫酸铜溶液,另取两只试管,向其中一只试管中加入一定质量的氢氧化钠溶液,向另一只试管中加入足量的稀硫酸.
第一步:如图所示,将试管放入烧杯中并在天平上称重.
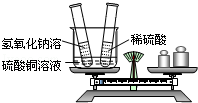
第二步:先将氢氧化钠溶液倒入烧杯中,能观察到的现象是 ________ ;随后再将足量的稀硫酸倒入烧杯中,能观察到的现象是 .
第三步:将两只试管放回烧杯中,并将烧杯重新放在天平的左盘上,你能观察到天平指针 ________ (填“偏左”、“偏右”或“保持不变”).
若使硫酸铜溶液与氢氧化钠溶液恰好完全反应,计算参加反应的氢氧化钠溶液中溶质的质量.
九年级化学探究题困难题查看答案及解析
氧化亚铜Cu2O可用于生产船底防污漆,防止海生物对船舶设备的污损.现将Cu2O和Cu的固体混合物20g放入烧杯中,加入质量分数为24.5%的稀硫酸50g,恰好完全反应.已知:。计算:
(1)所加稀硫酸中溶质的质量为__________g。
(2)原混合物中Cu2O与Cu的质量比(写出计算过程,结果用最简整数比表示)。___
(3)在图中画出向20gCu2O和Cu的固体混合物中逐滴加入24.5%的稀硫酸至过量,固体中铜元素的质量分数的变化曲线图,并标明必要的数据。_____

(4)氧化亚铜可用原理制备。
①反应过程中产生SO2可循环利用,因此应该选用________溶液来吸收它。
②反应过程中溶液pH将________(选填“变大”“变小”或“不变”),因此制备过程,要控制溶液的酸碱度,因为如果反应时溶液pH过小,会导致产品下降,原因是____________。
九年级化学计算题困难题查看答案及解析
氧化亚铜(Cu2O)可用于生产船底防污漆,防止海生物对船舶设备的污损。现将Cu2O和Cu的固体混合物20g放入烧杯中,加入质量分数为24.5%的稀硫酸50g,恰好完全反应。已知:Cu2O+H2SO4═CuSO4+Cu+H2O.计算:
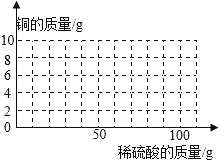
(1)所加稀硫酸中溶质的质量为_____g。
(2)原混合物中Cu2O与Cu的质量比_____(写出计算过程,结果用最简整数比表示)
(3)在图中画出向20g Cu2O和Cu的固体混合物中逐滴加入24.5%的稀硫酸至过量,铜的质量变化曲线_____。
九年级化学计算题困难题查看答案及解析
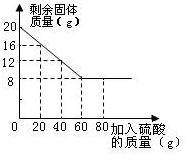
九年级化学解答题中等难度题查看答案及解析
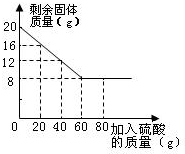
九年级化学解答题中等难度题查看答案及解析
九年级化学解答题中等难度题查看答案及解析