-
(12分)在密闭容器中充有10mol CO与20mol H2,在催化剂作用下反应生成甲醇:
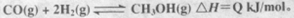 CO的转化率与温度、压强的关系如图所示。
CO的转化率与温度、压强的关系如图所示。
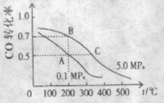
(1)若A、B两点表示在某时刻达到的平衡状态。将混合气体加热至200℃,自反应开始达到平衡状态A点所需要的时间为a min,容器体积为b L。反应达A点时此过程的反应速率为v(CO)=________mol/(L·min),则该温度下的平衡常数KA=________。B点时容器的体积VB=________b L (填“>”、“<”或“=”)。此反应的反应热
△H=________0(填“>”或“<”)
(2)若A、C两点分别表示某温度、压强下达到的平衡状态。则自反应开始达到平衡状态所需要的时间tA tC(填“>”、“<”或“=”)
(3)在不改变反应物用量情况下,为提高CO转化率可采取的措施是________(写出一种方法即可)
-
密闭容器中充有10 mol CO与20 mol H2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g) CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如下图所示。下列说法正确的是( )
CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如下图所示。下列说法正确的是( )
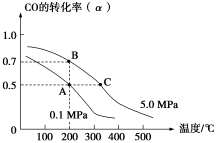
A.若A、B两点表示在某时刻达到的平衡状态,此时A、B两点时容器中,n(A)总∶n(B)总=4∶5
B.若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA<tC
C.设B、C两点的平衡常数分别为KB、KC,则KB<KC
D.在不改变反应物用量的情况下,降温、加压、将甲醇从混合体系中分离出来均可提高CO的转化率
-
密闭容器中充有10mol CO与20mol H2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g)  CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如下图所示。下列说法正确的是
CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如下图所示。下列说法正确的是
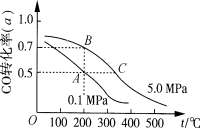
A. A、B两点表示在某时刻达到平衡状态,此时A、B两点时容器中,n(A)总∶n(B)总= 4∶5
B. A、C两点都表示达到平衡状态,则自反应开始到达平衡状态所需的时间tA<tC
C. 设B、C两点的平衡常数分别为KB、KC,则KB<KC
D. 在不改变反应物用量的情况下,降温、加压、将甲醇从混合体系中分离出来均可提高CO的转化率
-
密闭容器中充有10molCO与20molH2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g)⇌CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如图所示。下列说法正确的是( )
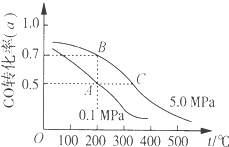
A.若A、B两点表示在某时刻达到的平衡状态,则A、B两点时容器内总气体的物质的量,n(A):n(B)=4:5
B.若A、C两点都表示已达到的平衡状态,则从反应开始至到达平衡状态所需的时间tA>tC
C.设B、C两点的平衡常数分别为KB、KC,则KB<KC
D.在不改变反应物用量的情况下,采取降温、减压或将甲醇从混合体系中分离出来均可提高CO的转化率
-
甲醇是一种可再生能源,具有广泛的开发和应用前景。在容积为2L的密闭容器中充入lmol CO与2molH2在催化剂作用下反应生成甲醇: , CO
, CO
平衡转化率与温度、压强的关系如意图所示;
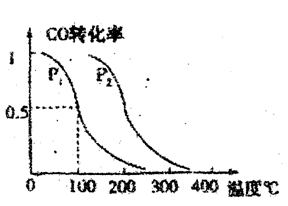
(1) Pl____P2(填大于、小于或等于)
(2) 若Pl为1标准大气压,反应温度为100℃,此条件下反应达到平衡:
①达到平衡所需的时间为5min,用H2表示的平均反应速率为________。
②反应的平衡常数K=________。
③平衡时,测得其能量的变化量为akJ。则该反应的热化学方程式是:
________。
(3) 恒容恒温情况下,再增加lmol CO与2molH2,达到新平衡时.CO的转化率________.
(填“增大”、“减小”或“不变”),平衡常数____。(填“增大”、“减小”或“不变”)
(4) 为了寻找一定催化剂下合成甲醇的适宜温度条件,某同学设计了一组实验,该实验中应控制的不变量是。
-
(1)汽车尾气中的 NO和CO可在催化剂作用下生成无污染的气体而除去。在密闭容器中充入10 mol CO和8 mol NO发生反应,测得平衡时NO的体积分数与温度、压强的关系如图。
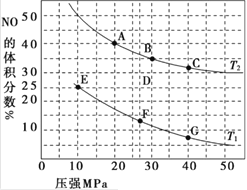
①已知该反应在较低温度下能自发进行,则反应 2NO(g)+2CO(g) N2(g)+2CO2 (g),ΔH______0(填“>” “=”或“<”)。
N2(g)+2CO2 (g),ΔH______0(填“>” “=”或“<”)。
②该反应达到平衡后,为同时提高反应速率和CO的转化率,可采取的措施有______ (填字母序号)
a.改用高效催化剂 b.缩小容器的体积 c.增加 NO 的浓度 d.升高温度
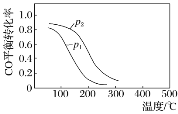
(2)在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2,将一定比例的O2、NH3 和NOx的混合气体匀速通入装有催化剂M的反应器中反应,反应相同时间,NOx的去除率随反应温度的变化曲线如图所示。

解释在50 ℃~150 ℃范围内随温度升高,NOx 的去除率迅速上升的原因是_______
(3)NH3催化还原氮氧化物技术是目前应用最广泛的烟气脱氮技术:4NH3(g)+6NO(g)  5N2(g)+6H2O(g) ΔH<0。密闭容器中,在相同时间内,在催化剂 A作用下脱氮率随温度变化如图所示。
5N2(g)+6H2O(g) ΔH<0。密闭容器中,在相同时间内,在催化剂 A作用下脱氮率随温度变化如图所示。
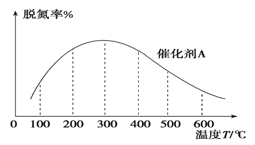
现改用催化能力稍弱的催化剂B进行实验,请在上图中画出在催化剂 B作用下的脱氮率随温度变化的曲线_________(不考虑温度对催化剂活性的影响)。
(4)某研究小组利用反应:C(s)+2NO(g) N2(g)+CO2(g) △ H= -34.0 kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得 NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) △ H= -34.0 kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得 NO的转化率随温度的变化如图所示:
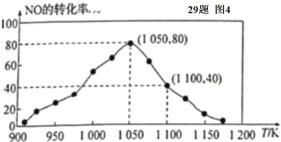
①由图可知,在 1050 K 前,反应中 NO的转化率随温度升髙而增大,其原因为____________; 在 1100 K 时,N2的体积分数为____________。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作 Kp )。在 1050 K、1.1×106 Pa 时,该反应的化学平衡常数 Kp=____________(已知:气体分压(P分) =气体总压(Pa)×体积分数)
-
(1).用合成气生成甲醇的反应:CO(g)+2H2(g)  CH3OH(g) ΔH,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200 ℃时n(H2)随时间的变化如下表所示:
CH3OH(g) ΔH,在10 L恒容密闭容器中按物质的量之比1∶2充入CO和H2,测得CO的平衡转化率与温度和压强的关系如下图所示,200 ℃时n(H2)随时间的变化如下表所示:
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8.0 | 5.4 | 4.0 | 4.0 |
①ΔH________(填“>”“<”或“= ”)0。
②写出一条可同时提高反应速率和CO转化率的措施:________________________。
③下列说法正确的是________(填字母)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强p1<p2
④0~3 min内用CH3OH表示的反应速率v(CH3OH)=__________________。
⑤ 200 ℃时,该反应的平衡常数K=________。向上述200 ℃达到平衡的恒容密闭容器中再加入2 mol CO、2 mol H2、2 mol CH3OH,保持温度不变,则化学平衡________(填“正向”“逆向”或“不”)移动。
-
在压强为0.1 MPa、10L恒容的密闭容器中, 将2 mol CO与 5 mol H2的混合气体在
催化剂作用下能生成甲醇:CO(g) + 2H2(g) CH3OH(g) △H<0 请回答下列问题:
CH3OH(g) △H<0 请回答下列问题:
(1)①该反应的熵变ΔS 0(填“>”、“<”或“=”)。
②若温度T1 >T2,则平衡常数K(T1) K(T2)(填“大于”、“小于”或“等于”)
③下列措施既可加快反应速率又可增加甲醇产率的是 ;
A.升高温度 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入2 mol CO和5 mol H2
④下列可说明反应已达到化学平衡状态的是________;
A.v生成(CH3OH)=v消耗(CO) B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变 D.CO与H2浓度比不再变化
(2)若温度T2时,5min后反应达到平衡,CO的转化率为75%,则:
①平衡时体系总的物质的量为 mol;
②反应的平衡常数K= ;
③反应在0-5min区间的平均反应速率v(H2)= 。
-
Ⅰ.CO可用于合成甲醇。在压强为0.1MPa条件下,在体积为bL的密闭容器中充入a mol CO和2a mol H2,在催化剂作用下合成甲醇:
CO(g)+2H2(g) CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
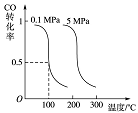
(1)该反应属于 反应(填“吸热”或“放热”)。
(2)100℃时,该反应的平衡常数:K= (用a、b 的代数式表示)。
(3)在温度和容积不变的情况下,再向平衡体系中充入a mol CO,2a mol H2,达到平衡时CO转化率 (填“增大”“不变”或“减小”)
Ⅱ.T ℃时,纯水中c(OH-)为10-6 mol·L-1,则该温度时
(1)将pH=3 的H2SO4溶液与pH=10的NaOH溶液按体积比9:2 混合,所得混合溶液的pH为 。
(2)若1体积pH1=a的某强酸溶液与10体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 。
Ⅲ. 在25mL的氢氧化钠溶液中逐滴加入0.2 mol/ L醋酸溶液,滴定曲线如图所示。
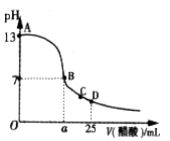
(1)该氢氧化钠溶液浓度为________________。
(2)在B点,a_________12.5 mL(填“<”“>”或“=”)。若由体积相等的氢氧化钠溶液和醋酸溶液混合且恰好呈中性,则混合前c(NaOH) c(CH3COOH)
(3)在D点,溶液中离子浓度大小关系为_____________________。
-
工业上以乙苯催化脱氢制取苯乙烯的反应如下:
 (g)
(g)
 (g) + H2(g)
(g) + H2(g)
现将x mol乙苯蒸气通入体积可变的密闭容器中反应,维持体系总压强p总恒定。在某催化剂作用下,乙苯的平衡转化率随温度变化如图所示。已知:气体分压(p分)= 气体总压(p总)× 体积分数。
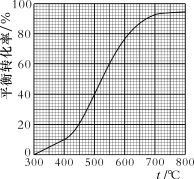
不考虑副反应,下列说法正确的是
A. 400℃时,向体系中通入水蒸气,v(正)、v(逆) 均减小,且乙苯转化率降低
B. 500℃时,向体系中通入乙苯、苯乙烯、氢气各0.1x mol,平衡不移动
C. 550℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp= × p总
× p总
D. 550℃时平衡体系中苯乙烯的体积分数是450℃时的3倍
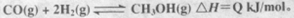 CO的转化率与温度、压强的关系如图所示。
CO的转化率与温度、压强的关系如图所示。











